Trắc nghiệm Bài 6: Nồng độ dung dịch Khoa học tự nhiên 8 Cánh diều có đáp án
Đề bài
Khối lượng NaOH có trong 300 m L dung dịch nồng độ 0,15 M là
-
A.
1,8 g.
-
B.
0,045 g.
-
C.
4,5g.
-
D.
0,125g.
Khối lượng H2O2 có trong 30 g dung dịch nồng độ 3%
-
A.
10 g.
-
B.
3 g.
-
C.
0,9 g.
-
D.
0,1 g.
Đồ thị sau cho biết ảnh hưởng của nhiệt độ đến độ tan của ba chất khác nhau trong nước.
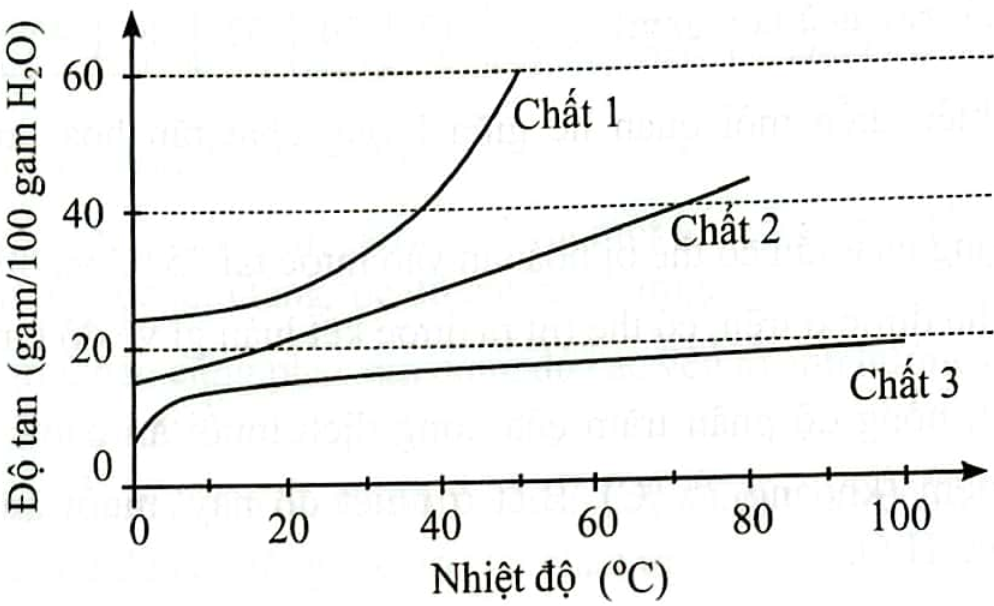
Nhận xét nào sau đây là đúng?
-
A.
Đối với chất 1, khi nhiệt độ tăng thì độ tan giảm.
-
B.
Độ tan của chất 2 ở 70oC gấp đôi ở 0 oC.
-
C.
Ở 20oC, độ tan của chất 1 gấp đôi chất 3.
-
D.
Độ tan của chất 3 ở 60 oC lớn hơn độ tan của chất 1 ở 20oC.
Rót 300ml nước vào bình có chứa sẵn 200ml sodium chloride 0,5M và lắc đều, thu được dung dịch sodium chloride mới. Nồng độ mol của dung dịch thu được là
-
A.
0,05 M
-
B.
0,10 M
-
C.
0,20 M
-
D.
0,30 M.
ở 25oC, 250 gam nước có thể hòa tan tối đa 80 gam KNO3, độ tan của KNO3 ở 25oC là
-
A.
32 gam/ 100 gam H2O
-
B.
36 gam/ 100 gam H2O
-
C.
80 gam/ 100 gam H2O
-
D.
40 gam/ 100 gam H2O
Công thức tính nồng độ phần trăm của dung dịch là
-
A.
\(C\% = \frac{{{m_{ct}}}}{{m{\,_{dd}}}}.100\% \)
-
B.
\({C_M} = \frac{{{n_{ct}}}}{{{V_{dd}}}}\)
-
C.
mdd = mdm + mct.
-
D.
m= n. M
Tại sao đun nóng dung dịch lại làm chất rắn tan nhanh hơn?
-
A.
Ở nhiệt độ cao, các hạt của chất rắn chuyển động chậm hơn, làm tăng số lần va chạm giữa các hạt chất của nước với bề mặt chất rắn, làm chất rắn tan nhanh hơn.
-
B.
Ở nhiệt độ cao, các hạt của chất rắn chuyển động nhanh hơn, làm tăng số lần va chạm giữa các hạt chất của nước với bề mặt chất rắn, làm chất rắn tan nhanh hơn.
-
C.
Ở nhiệt độ cao, các hạt của chất rắn chuyển động chậm hơn, làm giảm số lần va chạm giữa các hạt chất của nước với bề mặt chất rắn, làm chất rắn tan nhanh hơn.
-
D.
Ở nhiệt độ cao, các hạt của chất rắn chuyển động nhanh hơn, làm giảm số lần va chạm giữa các hạt chất của nước với bề mặt chất rắn, làm chất rắn tan nhanh hơn.
Kiểm tra tính tan của bột đá vôi (calcium carbonate) và muối ăn qua hai thí nghiệm sau:
- Thí nghiệm 1: Lấy một lượng nhỏ bột đá vôi, cho vào cốc nước cất, khuấy đều. Lọc lấy phần nước trong. Nhỏ vài giọt nước đó lên tấm kính sạch. Hơ tấm kính trên ngọn lửa đèn cồn đến khi nước bay hơi hết.
- Thí nghiệm 2: Thay bột đá vôi bằng muối ăn rồi làm như thí nghiệm 1.
Nhận xét nào sau đây là đúng?
-
A.
Mặt kính ở thí nghiệm 1 không xuất hiện hiện tượng gì.
-
B.
Mặt kính ở thí nghiệm 2 không xuất hiện gì.
-
C.
Mặt kính ở thí nghiệm 1 xuất hiện lớp chất rắn, màu trắng.
-
D.
Mặt kính ở thí nghiệm 2 xuất hiện lớp chất rắn, màu vàng.
Em rút ra được kết luận gì sau hai thí nghiệm trên?
-
A.
Bột đá vôi tan trong nước, muối ăn không tan trong nước.
-
B.
Bột đá vôi và muối ăn đều tan trong nước.
-
C.
Bột đá vôi và muối ăn đều không tan trong nước.
-
D.
Bột đá vôi không tan trong nước, muối ăn tan trong nước.
Cho 3 ống nghiệm, mỗi ống đựng 5ml nước cất, đánh số (1), (2), (3).
- Dùng các thìa giống nhau mỗi thìa xúc một trong các chất rắn dạng bột sau: urea (phân đạm), đường và bột phấn vào các ống nghiệm tương ứng và lắc đều.
- Ở ống (1), đến thìa thứ 5 thì urea không tan thêm được nữa, ta thấy bột rắn đọng lại ở đáy ống nghiệm.
- Hiện tượng tương tự ở ống (2) xảy ra khi cho đường đến thìa thứ 10; ở ống (3) thì từ thìa bột phấn đầu tiên đã không tan hết.
Trong các chất trên, chất nào có khả năng hòa tan trong nước tốt nhất?
-
A.
Bột phấn
-
B.
Urea
-
C.
Đường
-
D.
Tất cả các đáp án trên.
Trong các chất trên, chất nào có khả năng hòa tan trong nước kém nhất?
-
A.
Bột phấn
-
B.
Urea
-
C.
Đường
-
D.
Tất cả các đáp án trên.
Em hãy sắp xếp khả năng hòa tan trong nước của các chất tan trên theo thứ tự tăng dần?
-
A.
Urea, bột phấn, đường.
-
B.
Urea, đường, bột phấn.
-
C.
Bột phấn, urea, đường.
-
D.
Đường, urea, bột phấn.
Em hãy sắp xếp khả năng hòa tan trong nước của các chất tan trên theo thứ tự giảm dần?
-
A.
Đường, urea, bột phấn.
-
B.
Đường, bột phấn, urea.
-
C.
Bột phấn, đường, urea.
-
D.
Bột phấn, urea, đường.
Bột sắn dây là tinh bột thu được từ củ sắn dây, bột sắn dây là đồ uống giải khát có nhiều tác dụng đối với sức khỏe. Ngoài ra bột sắn dây còn là các vị thuốc, bài thuốc chữa được nhiều bệnh. Để thu được bột sắn dây, đầu tiên củ sắn dây được rửa sạch, cạo hết lớp vỏ bên ngoài rồi xay nhuyễn với nước, thu được hỗn hợp màu nâu.
Hỗn hợp này được thêm nước, khuấy kĩ rồi lọc nhiều lần qua các lớp vải để loại hết bã xơ và thu được phần nước lọc thô chứa tinh bột. Từ nước lọc thô, tiến hành đánh bột với bước cho ran và đợi lắng, sau đó chắt bỏ nước và thay nước. Quá trình này được lặp lại nhiều lần (khoảng 6 – 20 lần tùy nhu cầu sử dụng) với số lớp vải lọc tăng dần để tách bỏ hoàn toàn tạp chất và cho ra được lớp bột trắng tinh khiết. Tinh bột thu được sẽ được giàn mỏng ra lớp vải đặt trên dàn phơi bằng tre, để ráo nước. Sau đó, tinh bột sắn được đưa vào các tủ sấy chuyên dụng hoặc đem phơi nắng cho đến khi bột khô.

Hỗn hợp màu nâu sau khi xay nhuyễn củ sắn dây bao gồm những thành phần:
-
A.
nước, tinh bột sắn dây, bã sắn dây, tạp chất.
-
B.
tinh bột sắn dây, tạp chất.
-
C.
tinh bột sắn dây, tạp chất, bã sắn dây.
-
D.
nước, bã sắn dây, tạp chất.
Lớp vải lọc có tác dụng lọc bỏ bã sắn dây và các tạp chất. Vậy vải lọc có tác dụng tương tự như dụng cụ nào trong phòng thí nghiệm?
-
A.
Phễu lọc
-
B.
Giấy lọc
-
C.
Phễu chiết
-
D.
Đáp án A và B đúng.
Hỗn hợp nước lọc chứa tinh bột sắn dây thuộc loại nào sau đây?
-
A.
Nhũ tương
-
B.
Huyền phù
-
C.
Dung dịch
-
D.
Bọt
Ở 20oC, khi hòa tan 40 gam kali nitrat vào 95 gam nước thì được dung dịch bão hòa. Vậy ở 20oC, độ tan của kali nitrat là:
-
A.
40,1 gam.
-
B.
44,2 gam.
-
C.
42,1 gam.
-
D.
43,5 gam.
Độ tan của NaCl trong nước là 25°C là 36 gam. Khi mới hòa tan 15 gam NaCl vào 50 gam nước thì phải hòa tan thêm bao nhiêu gam NaCl để được dung dịch bão hòa?
-
A.
3 gam
-
B.
18 gam
-
C.
5 gam
-
D.
9 gam
Ở 20oC, hòa tan m gam KNO3 vào 95 gam nước thì được dung dịch bão hòa. Biết độ tan của KNO3 ở nhiệt độ 20oC là 42,105 gam. Giá trị của m là
-
A.
40.
-
B.
44.
-
C.
42
-
D.
43.
Tính độ tan của K2CO3 trong nước ở 20°C. Biết rằng ở nhiệt độ này hòa tan hết 45 gam muối trong 150 gam nước thì dung dịch bão hòa.
-
A.
20 gam
-
B.
45 gam
-
C.
30 gam
-
D.
12 gam
Hòa tan 2 mol NaCl vào nước ta thu được 4 lít dung dịch. Nồng độ mol/lít của dung dịch là
-
A.
1M.
-
B.
0,5M.
-
C.
0,1M.
-
D.
0,2M.
Làm bay hơi 20 gam nước từ dung dịch có nồng độ 15% thu được dung dịch có nồng độ 20%. Dung dịch ban đầu có khối lượng:
-
A.
90 gam.
-
B.
60 gam.
-
C.
70 gam.
-
D.
80 gam.
Dung dịch H2SO4 0,5M cho biết:
-
A.
Trong 1 lít dung dịch có hòa tan 0,5 mol H2SO4.
-
B.
Trong 1 lít dung môi có hòa tan 0,5 mol H2SO4.
-
C.
Trong 1 lít nước có hòa tan 0,5 mol H2SO4.
-
D.
Trong 1 lít nước có hòa tan 0,5 lít H2SO4.
Một bình đựng dung dịch có ghi “ dung dịch HCl 2M”. Phát biểu nào sau đây là đúng:
-
A.
Có 2 mol HCl trong 1 lít dung dịch.
-
B.
Có 2 gam HCl trong 1 lít dung dịch.
-
C.
Có 2 mol HCl trong 100 gam dung dịch.
-
D.
Có 2 gam HCl trong 100 gam dung dịch.
Để hoà tan m gam kẽm cần vừa đủ 50 gam dd HCl 7,3%. Khối lượng muối tạo thành sau phản ứng
-
A.
6,8 g
-
B.
12,5 g
-
C.
12,6 g
-
D.
28,9 g
Trộn 150g dung dịch NaOH có nồng độ 20% với 50g dung dịch NaOH có nồng độ 5%.
Tính nồng độ phần trăm của dung dịch thu được.
-
A.
12,8 %
-
B.
15,5 %
-
C.
12,6 %
-
D.
16,25 %
Lời giải và đáp án
Khối lượng NaOH có trong 300 m L dung dịch nồng độ 0,15 M là
-
A.
1,8 g.
-
B.
0,045 g.
-
C.
4,5g.
-
D.
0,125g.
Đáp án : A
Dựa vào tính nồng độ mol dung dịch.
Số mol NaOH: nNaOH = 0,3.0,15 = 0,045 (mol).
Khối lượng NaOH: mNaOH = 0,045.40 = 1,8 (gam).
Khối lượng H2O2 có trong 30 g dung dịch nồng độ 3%
-
A.
10 g.
-
B.
3 g.
-
C.
0,9 g.
-
D.
0,1 g.
Đáp án : C

⇒mct = mH2O2 = 30.3%100%= 0,9(g).
Đáp án: C
Đồ thị sau cho biết ảnh hưởng của nhiệt độ đến độ tan của ba chất khác nhau trong nước.

Nhận xét nào sau đây là đúng?
-
A.
Đối với chất 1, khi nhiệt độ tăng thì độ tan giảm.
-
B.
Độ tan của chất 2 ở 70oC gấp đôi ở 0 oC.
-
C.
Ở 20oC, độ tan của chất 1 gấp đôi chất 3.
-
D.
Độ tan của chất 3 ở 60 oC lớn hơn độ tan của chất 1 ở 20oC.
Đáp án : C
Ở 20oC, độ tan của chất 1 gấp đôi chất 3.
Rót 300ml nước vào bình có chứa sẵn 200ml sodium chloride 0,5M và lắc đều, thu được dung dịch sodium chloride mới. Nồng độ mol của dung dịch thu được là
-
A.
0,05 M
-
B.
0,10 M
-
C.
0,20 M
-
D.
0,30 M.
Đáp án : C
Nồng độ dung dịch = nV
Thể tích dung dịch là: 0,3 + 0,2 = 0,5 lít
n NaCl= 0,5 x 0,2 = 0,1 mol
Nồng độ mol của dung dịch thu được là: 0,1 : 0,5 =0,2 M
Đáp án: C
ở 25oC, 250 gam nước có thể hòa tan tối đa 80 gam KNO3, độ tan của KNO3 ở 25oC là
-
A.
32 gam/ 100 gam H2O
-
B.
36 gam/ 100 gam H2O
-
C.
80 gam/ 100 gam H2O
-
D.
40 gam/ 100 gam H2O
Đáp án : A
Độ tan của một chất là số gam chất đó tan được trong 100 gam dung môi
Độ tan của chất ở 250C : (100 x 80): 250=32 gam
Đáp án: A
Công thức tính nồng độ phần trăm của dung dịch là
-
A.
\(C\% = \frac{{{m_{ct}}}}{{m{\,_{dd}}}}.100\% \)
-
B.
\({C_M} = \frac{{{n_{ct}}}}{{{V_{dd}}}}\)
-
C.
mdd = mdm + mct.
-
D.
m= n. M
Đáp án : A
Công thức tính nồng độ phần trăm của dd: \(C\% = \frac{{{m_{ct}}}}{{m{\,_{dd}}}}.100\% \)
Tại sao đun nóng dung dịch lại làm chất rắn tan nhanh hơn?
-
A.
Ở nhiệt độ cao, các hạt của chất rắn chuyển động chậm hơn, làm tăng số lần va chạm giữa các hạt chất của nước với bề mặt chất rắn, làm chất rắn tan nhanh hơn.
-
B.
Ở nhiệt độ cao, các hạt của chất rắn chuyển động nhanh hơn, làm tăng số lần va chạm giữa các hạt chất của nước với bề mặt chất rắn, làm chất rắn tan nhanh hơn.
-
C.
Ở nhiệt độ cao, các hạt của chất rắn chuyển động chậm hơn, làm giảm số lần va chạm giữa các hạt chất của nước với bề mặt chất rắn, làm chất rắn tan nhanh hơn.
-
D.
Ở nhiệt độ cao, các hạt của chất rắn chuyển động nhanh hơn, làm giảm số lần va chạm giữa các hạt chất của nước với bề mặt chất rắn, làm chất rắn tan nhanh hơn.
Đáp án : B
Ở nhiệt độ cao, các hạt của chất rắn chuyển động nhanh hơn, làm tăng số lần va chạm giữa các hạt chất của nước với bề mặt chất rắn, làm chất rắn tan nhanh hơn.
Kiểm tra tính tan của bột đá vôi (calcium carbonate) và muối ăn qua hai thí nghiệm sau:
- Thí nghiệm 1: Lấy một lượng nhỏ bột đá vôi, cho vào cốc nước cất, khuấy đều. Lọc lấy phần nước trong. Nhỏ vài giọt nước đó lên tấm kính sạch. Hơ tấm kính trên ngọn lửa đèn cồn đến khi nước bay hơi hết.
- Thí nghiệm 2: Thay bột đá vôi bằng muối ăn rồi làm như thí nghiệm 1.
Nhận xét nào sau đây là đúng?
-
A.
Mặt kính ở thí nghiệm 1 không xuất hiện hiện tượng gì.
-
B.
Mặt kính ở thí nghiệm 2 không xuất hiện gì.
-
C.
Mặt kính ở thí nghiệm 1 xuất hiện lớp chất rắn, màu trắng.
-
D.
Mặt kính ở thí nghiệm 2 xuất hiện lớp chất rắn, màu vàng.
Đáp án: A
- Mặt trên tấm kính ở thí nghiệm 1 không xuất hiện hiện tượng gì.
- Mặt trên tấm kính ở thí nghiệm 2 xuất hiện lớp chất rắn, màu trắng.
Em rút ra được kết luận gì sau hai thí nghiệm trên?
-
A.
Bột đá vôi tan trong nước, muối ăn không tan trong nước.
-
B.
Bột đá vôi và muối ăn đều tan trong nước.
-
C.
Bột đá vôi và muối ăn đều không tan trong nước.
-
D.
Bột đá vôi không tan trong nước, muối ăn tan trong nước.
Đáp án: D
Bột đá vôi không tan trong nước, muối ăn tan trong nước.
Cho 3 ống nghiệm, mỗi ống đựng 5ml nước cất, đánh số (1), (2), (3).
- Dùng các thìa giống nhau mỗi thìa xúc một trong các chất rắn dạng bột sau: urea (phân đạm), đường và bột phấn vào các ống nghiệm tương ứng và lắc đều.
- Ở ống (1), đến thìa thứ 5 thì urea không tan thêm được nữa, ta thấy bột rắn đọng lại ở đáy ống nghiệm.
- Hiện tượng tương tự ở ống (2) xảy ra khi cho đường đến thìa thứ 10; ở ống (3) thì từ thìa bột phấn đầu tiên đã không tan hết.
Trong các chất trên, chất nào có khả năng hòa tan trong nước tốt nhất?
-
A.
Bột phấn
-
B.
Urea
-
C.
Đường
-
D.
Tất cả các đáp án trên.
Đáp án: C
Ở ống (2) khi cho đường đến thìa thứ 10 mới thấy có chất rắn đọng lại dưới đáy ống nghiệm => Khả năng hòa tan trong nước của đường là tốt nhất.
Trong các chất trên, chất nào có khả năng hòa tan trong nước kém nhất?
-
A.
Bột phấn
-
B.
Urea
-
C.
Đường
-
D.
Tất cả các đáp án trên.
Đáp án: A
Ở ống (3) thì từ thìa bột phấn đầu tiên đã không tan hết => Khả năng hòa tan trong nước của bột phấn là kém nhất.
Em hãy sắp xếp khả năng hòa tan trong nước của các chất tan trên theo thứ tự tăng dần?
-
A.
Urea, bột phấn, đường.
-
B.
Urea, đường, bột phấn.
-
C.
Bột phấn, urea, đường.
-
D.
Đường, urea, bột phấn.
Đáp án: C
- Ở ống (1), đến thìa thứ 5 thì urea không tan thêm được nữa, ta thấy bột rắn đọng lại ở đáy ống nghiệm.
- Hiện tượng tương tự ở ống (2) xảy ra khi cho đường đến thìa thứ 10; ở ống (3) thì từ thìa bột phấn đầu tiên đã không tan hết.
=> Khả năng hòa tan của các chất tăng dần theo thứ tự: bột phấn < urea < đường.
Em hãy sắp xếp khả năng hòa tan trong nước của các chất tan trên theo thứ tự giảm dần?
-
A.
Đường, urea, bột phấn.
-
B.
Đường, bột phấn, urea.
-
C.
Bột phấn, đường, urea.
-
D.
Bột phấn, urea, đường.
Đáp án: A
- Ở ống (1), đến thìa thứ 5 thì urea không tan thêm được nữa, ta thấy bột rắn đọng lại ở đáy ống nghiệm.
- Hiện tượng tương tự ở ống (2) xảy ra khi cho đường đến thìa thứ 10; ở ống (3) thì từ thìa bột phấn đầu tiên đã không tan hết.
=> Khả năng hòa tan của các chất giảm dần theo thứ tự: đường > urea > bột phấn.
Bột sắn dây là tinh bột thu được từ củ sắn dây, bột sắn dây là đồ uống giải khát có nhiều tác dụng đối với sức khỏe. Ngoài ra bột sắn dây còn là các vị thuốc, bài thuốc chữa được nhiều bệnh. Để thu được bột sắn dây, đầu tiên củ sắn dây được rửa sạch, cạo hết lớp vỏ bên ngoài rồi xay nhuyễn với nước, thu được hỗn hợp màu nâu.
Hỗn hợp này được thêm nước, khuấy kĩ rồi lọc nhiều lần qua các lớp vải để loại hết bã xơ và thu được phần nước lọc thô chứa tinh bột. Từ nước lọc thô, tiến hành đánh bột với bước cho ran và đợi lắng, sau đó chắt bỏ nước và thay nước. Quá trình này được lặp lại nhiều lần (khoảng 6 – 20 lần tùy nhu cầu sử dụng) với số lớp vải lọc tăng dần để tách bỏ hoàn toàn tạp chất và cho ra được lớp bột trắng tinh khiết. Tinh bột thu được sẽ được giàn mỏng ra lớp vải đặt trên dàn phơi bằng tre, để ráo nước. Sau đó, tinh bột sắn được đưa vào các tủ sấy chuyên dụng hoặc đem phơi nắng cho đến khi bột khô.

Hỗn hợp màu nâu sau khi xay nhuyễn củ sắn dây bao gồm những thành phần:
-
A.
nước, tinh bột sắn dây, bã sắn dây, tạp chất.
-
B.
tinh bột sắn dây, tạp chất.
-
C.
tinh bột sắn dây, tạp chất, bã sắn dây.
-
D.
nước, bã sắn dây, tạp chất.
Đáp án: A
Đọc kỹ các thông tin đề bài cho.
Hỗn hợp màu nâu sau khi xay nhuyễn củ sắn dây bao gồm những thành phần nước, tinh bột sắn dây, bã sắn dây, tạp chất.
Lớp vải lọc có tác dụng lọc bỏ bã sắn dây và các tạp chất. Vậy vải lọc có tác dụng tương tự như dụng cụ nào trong phòng thí nghiệm?
-
A.
Phễu lọc
-
B.
Giấy lọc
-
C.
Phễu chiết
-
D.
Đáp án A và B đúng.
Đáp án: D
Lớp vải lọc có tác dụng lọc bỏ bã sắn dây và các tạp chất, nó có tác dụng như phễu lọc và giấy lọc trong phòng thí nghiệm.
Hỗn hợp nước lọc chứa tinh bột sắn dây thuộc loại nào sau đây?
-
A.
Nhũ tương
-
B.
Huyền phù
-
C.
Dung dịch
-
D.
Bọt
Đáp án: B
Hỗn hợp nước lọc chứa tinh bột sắn dây thuộc loại huyền phù.
Ở 20oC, khi hòa tan 40 gam kali nitrat vào 95 gam nước thì được dung dịch bão hòa. Vậy ở 20oC, độ tan của kali nitrat là:
-
A.
40,1 gam.
-
B.
44,2 gam.
-
C.
42,1 gam.
-
D.
43,5 gam.
Đáp án : C
Ghi nhớ khái niệm độ tan của 1 chất
Độ tan của 1 chất là số gam chất đó hòa tan được trong 100 gam nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định
=> độ tan của kali nitrat trong 100 gam nước là: \(\frac{{100.40}}{{95}} = 42,1\,(gam)\)
Độ tan của NaCl trong nước là 25°C là 36 gam. Khi mới hòa tan 15 gam NaCl vào 50 gam nước thì phải hòa tan thêm bao nhiêu gam NaCl để được dung dịch bão hòa?
-
A.
3 gam
-
B.
18 gam
-
C.
5 gam
-
D.
9 gam
Đáp án : A
+) Khối lượng NaCl hòa tan vào 50 gam nước để tạo dd bão hòa: mct = m + 15
+) Áp dụng công thức tính độ tan: $S=\frac{{{m}_{ct}}}{{{m}_{dm}}}.100$ => mct => m
Gọi khối lượng NaCl cần hòa tan thêm là m
=> Khối lượng NaCl hòa tan vào 50 gam nước để tạo dd bão hòa là: mct = m + 15
Ta có: mdm = 50 gam
Áp dụng công thức tính độ tan: $S=\frac{{{m}_{ct}}}{{{m}_{dm}}}.100=>\frac{m+15}{50}.100=36\,$
=> m = 3 gam
Ở 20oC, hòa tan m gam KNO3 vào 95 gam nước thì được dung dịch bão hòa. Biết độ tan của KNO3 ở nhiệt độ 20oC là 42,105 gam. Giá trị của m là
-
A.
40.
-
B.
44.
-
C.
42
-
D.
43.
Đáp án : A
Công thức tính độ tan: $S=\frac{{{m}_{ct}}}{{{m}_{dm}}}.100=>{{m}_{ct}}=\frac{S.{{m}_{dm}}}{100}$
Công thức tính độ tan:
$S=\frac{{{m}_{ct}}}{{{m}_{dm}}}.100=>{{m}_{ct}}=\frac{S.{{m}_{dm}}}{100}=\frac{42,105.95}{100}=40 gam$
Tính độ tan của K2CO3 trong nước ở 20°C. Biết rằng ở nhiệt độ này hòa tan hết 45 gam muối trong 150 gam nước thì dung dịch bão hòa.
-
A.
20 gam
-
B.
45 gam
-
C.
30 gam
-
D.
12 gam
Đáp án : C
Áp dụng công thức tính độ tan: $S=\frac{{{m}_{ct}}}{{{m}_{dm}}}.100$
Hòa tan hết 45 gam muối trong 150 gam nước → dung dịch bão hòa
=> mct = 45 gam; mdm = 150 gam
Áp dụng công thức tính độ tan: $S=\frac{{{m}_{ct}}}{{{m}_{dm}}}.100=\frac{45}{150}.100=30\,gam$
Hòa tan 2 mol NaCl vào nước ta thu được 4 lít dung dịch. Nồng độ mol/lít của dung dịch là
-
A.
1M.
-
B.
0,5M.
-
C.
0,1M.
-
D.
0,2M.
Đáp án : B
áp dụng công thức tính nồng độ mol: CM = n: V
Nồng độ mol/lít của NaCl = nNaCl : Vdd = 2 : 4 = 0,5 (M)
Làm bay hơi 20 gam nước từ dung dịch có nồng độ 15% thu được dung dịch có nồng độ 20%. Dung dịch ban đầu có khối lượng:
-
A.
90 gam.
-
B.
60 gam.
-
C.
70 gam.
-
D.
80 gam.
Đáp án : D
Gọi khối lượng dung dịch ban đầu là m (g)
\(\begin{array}{l}C\% = \frac{{mc\tan }}{{m\,dd\,sau}}.100\% \\ = > 20\% = \frac{{0,15m}}{{m - 20}}.100\% \\ = > m = ?\,(gam)\end{array}\)
Gọi khối lượng dung dịch ban đầu là m (g)
Khối lượng chất tan ban đầu là: 0,15m (g)
Sau khi làm bay hơi 20 gam nước thì khối lượng dung dịch sau là: m – 20 (g)
Nồng độ phần trăm sau phản ứng:
\(\begin{array}{l}C\% = \frac{{mc\tan }}{{m\,dd\,sau}}.100\% \\ = > 20\% = \frac{{0,15m}}{{m - 20}}.100\% \\ = > m = 80\,(gam)\end{array}\)
Dung dịch H2SO4 0,5M cho biết:
-
A.
Trong 1 lít dung dịch có hòa tan 0,5 mol H2SO4.
-
B.
Trong 1 lít dung môi có hòa tan 0,5 mol H2SO4.
-
C.
Trong 1 lít nước có hòa tan 0,5 mol H2SO4.
-
D.
Trong 1 lít nước có hòa tan 0,5 lít H2SO4.
Đáp án : A
Dung dịch H2SO4 0,5M cho biết: Trong 1 lít dung dịch có hòa tan 0,5 mol H2SO4.
Một bình đựng dung dịch có ghi “ dung dịch HCl 2M”. Phát biểu nào sau đây là đúng:
-
A.
Có 2 mol HCl trong 1 lít dung dịch.
-
B.
Có 2 gam HCl trong 1 lít dung dịch.
-
C.
Có 2 mol HCl trong 100 gam dung dịch.
-
D.
Có 2 gam HCl trong 100 gam dung dịch.
Đáp án : A
Dựa vào kiến thức học về nồng độ mol trong sgk hóa 8 – trang 144
Dung dịch HCl 2M có nghĩa là có 2 mol HCl trong 1 lít dung dịch.
Để hoà tan m gam kẽm cần vừa đủ 50 gam dd HCl 7,3%. Khối lượng muối tạo thành sau phản ứng
-
A.
6,8 g
-
B.
12,5 g
-
C.
12,6 g
-
D.
28,9 g
Đáp án : A
Zn + 2HCl → ZnCl2 + H2
mHCl = (C% . mdd) : 100
= (50 . 7,3) : 100
= 3,65 gam
⟹ nHCl = 3,65:36,5
= 0,1 mol
Theo PTPƯ:
nZnCl2 = 1/2 . nHC l= 0,1 : 2 = 0,05 mol
⟹ mZnCl2 = 0,05 . 136= 6,8 gam
Trộn 150g dung dịch NaOH có nồng độ 20% với 50g dung dịch NaOH có nồng độ 5%.
Tính nồng độ phần trăm của dung dịch thu được.
-
A.
12,8 %
-
B.
15,5 %
-
C.
12,6 %
-
D.
16,25 %
Đáp án : D
Áp dụng công thức:
\(C\% = \frac{{{m_{ct}}}}{{{m_{dd}}}}.100\% .\)
- Khối lượng NaOH có trong 150g dung dịch 20%:
\({m_{ct(dd1)}} = \frac{{C\% .{m_{dd1}}}}{{100\% }} = \frac{{20.150}}{{100}} = 30(g).\)
- Khối lượng muối ăn có trong 50g dung dịch 5%:
\({m_{ct(dd2)}} = \frac{{C\% .{m_{dd2}}}}{{100\% }} = \frac{{5.50}}{{100}} = 2,5(g).\)
- mdd3 = 150 + 50 = 200(g).
- mct = 30 + 2,5 = 32,5(g).
Nồng độ phần trăm của dung dịch mới thu được là: 16,25%.
Luyện tập và củng cố kiến thức Bài 7: Tốc độ phản ứng và chất xúc tác với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 5: Tính theo phương trình hóa học với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 4: Mol và tỉ khối của chất khí với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 3: Định luật bảo toàn khối lượng. Phương trình hóa học với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 2: Phản ứng hóa học và năng lượng của phản ứng hóa học với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
Luyện tập và củng cố kiến thức Bài 1: Biến đổi vật lí và biến đổi hóa học với đầy đủ các dạng bài tập trắc nghiệm có đáp án và lời giải chi tiết
- Trắc nghiệm Bài 43: Khái quát về sinh quyển và các khu sinh học Khoa học tự nhiên 8 Cánh diều
- Trắc nghiệm Bài 42: Cân bằng tự nhiên và bảo vệ môi trường Khoa học tự nhiên 8 Cánh diều
- Trắc nghiệm Bài 41: Hệ sinh thái Khoa học tự nhiên 8 Cánh diều
- Trắc nghiệm Bài 40: Quần xã sinh vật Khoa học tự nhiên 8 Cánh diều
- Trắc nghiệm Bài 39: Quần thể sinh vật Khoa học tự nhiên 8 Cánh diều










Danh sách bình luận