Đề thi giữa kì 2 Hóa 10 - Chân trời sáng tạo - Đề số 4
Tổng hợp đề thi học kì 2 lớp 10 tất cả các môn - Chân trời sáng tạo
Toán - Văn - Anh - Lí - Hóa - Sinh - Sử - Địa...
Cho hai phương trình nhiệt hóa học sau:
Đề bài
Cho quá trình 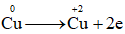 , đây là quá trình
, đây là quá trình
-
A.
oxi hóa.
-
B.
khử.
-
C.
nhận proton.
-
D.
tự oxi hóa – khử.
Cho hai phương trình nhiệt hóa học sau:
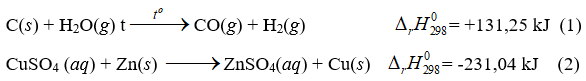
Trong hai phản ứng trên, phản ứng nào là thu nhiệt, phản ứng nào là tỏa nhiệt?
-
A.
Phản ứng (1) tỏa nhiệt và phản ứng (2) thu nhiệt.
-
B.
Cả 2 phản ứng đều tỏa nhiệt.
-
C.
Cả 2 phản ứng đều thu nhiệt.
-
D.
Phản ứng (1) thu nhiệt và phản ứng (2) tỏa nhiệt.
Phản ứng nào sau đây không phải là phản ứng oxi hóa – khử?
-
A.
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
-
B.
NaHCO3 → Na2CO3 + CO2 + H2O
-
C.
4Al + 3O2 → 2Al2O3
-
D.
CH4 → C + 2H2
Phản ứng (quá trình) nào sau đây là phản ứng (quá trình) thu nhiệt?
-
A.
Nước hoá rắn.
-
B.
Quá trình chạy của con người.
-
C.
Khi CH4 đốt ở trong lò.
-
D.
Hoà tan KBr vào nước làm cho nước trở nên lạnh.
Nhiệt độ thường được chọn ở điều kiện chuẩn là ?
-
A.
20oC.
-
B.
25oC.
-
C.
24oC.
-
D.
22oC.
Trong phản ứng Cl2 + Ca(OH)2\( \to \) CaOCl2 + H2O. Khẳng định nào sau đây về Chlorine là đúng
-
A.
Là chất khử
-
B.
Là chất oxi hóa
-
C.
Là chất oxi hóa – chất khử
-
D.
Không thể hiện tính oxi hóa - Khử
Enthalpy tạo thành chuẩn (nhiệt tạo thành chuẩn) có kí hiệu là :
-
A.
\({\Delta _r}H_{298}^0\).
-
B.
\({\Delta _f}H_{298}^0\).
-
C.
\(\Delta S\).
-
D.
\(\Delta T\).
Chất oxy hoá còn gọi là chất
-
A.
chất bị khử
-
B.
chất bị oxy hoá
-
C.
Chất có tính khử
-
D.
chất đi khử.
Trong phản ứng thu nhiệt, sự so sánh nào sau đây đúng về \(\sum {{\Delta _f}H_{298}^0(c{\rm{d}})} \)và \(\sum {{\Delta _f}H_{298}^0(sp)} \)
-
A.
\(\sum {{\Delta _f}H_{298}^0({\rm{cd}})} = \sum {{\Delta _f}H_{298}^0(sp)} \).
-
B.
\(\sum {{\Delta _f}H_{298}^0({\rm{cd}})} > \sum {{\Delta _f}H_{298}^0(sp)} \).
-
C.
\(\sum {{\Delta _f}H_{298}^0({\rm{cd}})} \simeq \sum {{\Delta _f}H_{298}^0(sp)} \).
-
D.
\(\sum {{\Delta _f}H_{298}^0({\rm{cd}})} < \sum {{\Delta _f}H_{298}^0(sp)} \).
Số oxi hóa của nguyên tử S trong hợp chất SO2 là
-
A.
+2.
-
B.
. +4.
-
C.
+6.
-
D.
-1.
Khi tham gia các phản ứng đốt cháy nhiên liệu, oxygen đóng vai trò là
-
A.
chất khử.
-
B.
chất oxi hóa.
-
C.
acid.
-
D.
base.
-
A.
a ghép với 4, b ghép với 4, c ghép với 1 và d ghép với 3.
-
B.
a ghép với 4, b ghép với 1, c ghép với 3 và d ghép với 2.
-
C.
a ghép với 4, b ghép với 3, c ghép với 1 và d ghép với 2.
-
D.
a ghép với 1, b ghép với 4, c ghép với 2 và d ghép với 3.
Cho phản ứng hóa học: Fe + CuSO4 → FeSO4 + Cu. Trong phản ứng trên xảy ra
-
A.
sự khử Fe2+ và sự oxi hóa Cu.
-
B.
sự khử Fe2+ và sự khử Cu2+.
-
C.
sự oxi hóa Fe và sự oxi hóa Cu.
-
D.
sự oxi hóa Fe và sự khử Cu2+.
-
A.
–571,32 kJ.
-
B.
–856,98 kJ.
-
C.
–285,66 kJ.
-
D.
–1142,64 kJ.
Cho các phát biểu sau :
(1) Phản ứng phân huỷ Fe(OH)3(s) không cần cung cấp nhiệt độ liên tục.
(2) Số oxi hóa của hydrogen trong các hydride kim loại bằng +1.
(3) Trộn potassium chloride (KCl) vào nước là quá trình thu nhiệt.
(4) Phản ứng của Fe(OH)2 với dung dịch HNO3 loãng không có sự thay đổi số oxi hóa của Fe.
(5) Để giữ ấm cơ thể, trước khi lặn, người ta thường uống nước mắm cốt.
Số phát biểu đúng là
-
A.
2
-
B.
3
-
C.
5
-
D.
4
Trong các chất sau, chất nào bền nhất về nhiệt ở điều kiện chuẩn ? Biết nhiệt tạo thành chuẩn của HCl(g) bằng -92,31 kJ.mol-1.
-
A.
O2(g)
-
B.
N2(g)
-
C.
Ca(s)
-
D.
HCl(g)
Lời giải và đáp án
Cho quá trình 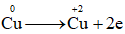 , đây là quá trình
, đây là quá trình
-
A.
oxi hóa.
-
B.
khử.
-
C.
nhận proton.
-
D.
tự oxi hóa – khử.
Đáp án : A
Dựa vào khái niệm chất khử, chất oxi hóa
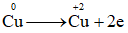 :
:
Cu nhường 2 electron => Cu là chất khử có quá trình oxi hóa
Đáp án A
Cho hai phương trình nhiệt hóa học sau:
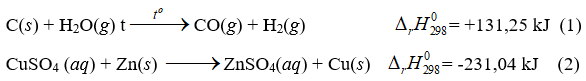
Trong hai phản ứng trên, phản ứng nào là thu nhiệt, phản ứng nào là tỏa nhiệt?
-
A.
Phản ứng (1) tỏa nhiệt và phản ứng (2) thu nhiệt.
-
B.
Cả 2 phản ứng đều tỏa nhiệt.
-
C.
Cả 2 phản ứng đều thu nhiệt.
-
D.
Phản ứng (1) thu nhiệt và phản ứng (2) tỏa nhiệt.
Đáp án : D
Dựa vào dấu của \(\Delta H\)
(1) có \(\Delta H\)> 0 => phản ứng thu nhiệt
(2) có \(\Delta H\)< 0 => phản ứng tỏa nhiệt
Đáp án D
Phản ứng nào sau đây không phải là phản ứng oxi hóa – khử?
-
A.
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
-
B.
NaHCO3 → Na2CO3 + CO2 + H2O
-
C.
4Al + 3O2 → 2Al2O3
-
D.
CH4 → C + 2H2
Đáp án : B
Dựa vào sự thay đổi số oxi hóa của các chất
NaHCO3 → Na2CO3 + CO2 + H2O chỉ có sự giảm xuống số oxi hóa của C
Đáp án B
Phản ứng (quá trình) nào sau đây là phản ứng (quá trình) thu nhiệt?
-
A.
Nước hoá rắn.
-
B.
Quá trình chạy của con người.
-
C.
Khi CH4 đốt ở trong lò.
-
D.
Hoà tan KBr vào nước làm cho nước trở nên lạnh.
Đáp án : D
Dựa vào khái niệm của phản ứng thu nhiệt, tỏa nhiệt
Hòa tan KBr vào nước làm cho nước trở nên lạnh hơn là phản ứng thu nhiệt
Đáp án D
Nhiệt độ thường được chọn ở điều kiện chuẩn là ?
-
A.
20oC.
-
B.
25oC.
-
C.
24oC.
-
D.
22oC.
Đáp án : B
Dựa vào điều kiện của phản ứng
Nhiệt độ thường được chọn là điều kiện chuẩn là 298K tương đương 25oC
Đáp án B
Trong phản ứng Cl2 + Ca(OH)2\( \to \) CaOCl2 + H2O. Khẳng định nào sau đây về Chlorine là đúng
-
A.
Là chất khử
-
B.
Là chất oxi hóa
-
C.
Là chất oxi hóa – chất khử
-
D.
Không thể hiện tính oxi hóa - Khử
Đáp án : C
Dựa vào sự thay đổi số oxi hóa của chất
Cl2 vừa tăng vừa giảm số oxi hóa => chlorine đóng vai trò là chất oxi hóa – khử
Đáp án C
Enthalpy tạo thành chuẩn (nhiệt tạo thành chuẩn) có kí hiệu là :
-
A.
\({\Delta _r}H_{298}^0\).
-
B.
\({\Delta _f}H_{298}^0\).
-
C.
\(\Delta S\).
-
D.
\(\Delta T\).
Đáp án : B
Enthalpy tạo thành chuẩn có kí hiệu \({\Delta _f}H_{298}^0\)
Đáp án B
Chất oxy hoá còn gọi là chất
-
A.
chất bị khử
-
B.
chất bị oxy hoá
-
C.
Chất có tính khử
-
D.
chất đi khử.
Đáp án : A
Chất oxy hóa là chất nhận electron
Chất oxy hóa được gọi là chất bị khử
Đáp án A
Trong phản ứng thu nhiệt, sự so sánh nào sau đây đúng về \(\sum {{\Delta _f}H_{298}^0(c{\rm{d}})} \)và \(\sum {{\Delta _f}H_{298}^0(sp)} \)
-
A.
\(\sum {{\Delta _f}H_{298}^0({\rm{cd}})} = \sum {{\Delta _f}H_{298}^0(sp)} \).
-
B.
\(\sum {{\Delta _f}H_{298}^0({\rm{cd}})} > \sum {{\Delta _f}H_{298}^0(sp)} \).
-
C.
\(\sum {{\Delta _f}H_{298}^0({\rm{cd}})} \simeq \sum {{\Delta _f}H_{298}^0(sp)} \).
-
D.
\(\sum {{\Delta _f}H_{298}^0({\rm{cd}})} < \sum {{\Delta _f}H_{298}^0(sp)} \).
Đáp án : D
Dựa vào dấu của phản ứng thu nhiệt
Phản ứng thu nhiệt có \({\Delta _r}H_{298}^0\)= \(\sum {{\Delta _f}H_{298}^0(sp)} \)- \(\sum {{\Delta _f}H_{298}^0(c{\rm{d}})} \)> 0
=> \(\sum {{\Delta _f}H_{298}^0(sp)} \)>\(\sum {{\Delta _f}H_{298}^0(c{\rm{d}})} \)
Đáp án D
Số oxi hóa của nguyên tử S trong hợp chất SO2 là
-
A.
+2.
-
B.
. +4.
-
C.
+6.
-
D.
-1.
Đáp án : B
Dựa vào quy tắc xác định số oxi hóa của nguyên tử
Số oxi hóa của S trong SO2 là +4
Đáp án B
Khi tham gia các phản ứng đốt cháy nhiên liệu, oxygen đóng vai trò là
-
A.
chất khử.
-
B.
chất oxi hóa.
-
C.
acid.
-
D.
base.
Đáp án : B
Dựa vào số oxi hóa của oxygen
Oxygen đóng vai trò là chất oxi hóa
Đáp án B
-
A.
a ghép với 4, b ghép với 4, c ghép với 1 và d ghép với 3.
-
B.
a ghép với 4, b ghép với 1, c ghép với 3 và d ghép với 2.
-
C.
a ghép với 4, b ghép với 3, c ghép với 1 và d ghép với 2.
-
D.
a ghép với 1, b ghép với 4, c ghép với 2 và d ghép với 3.
Đáp án : B
Dựa vào khái niệm của phản ứng tỏa nhiệt, phản ứng thu nhiệt
a) Trong phản ứng thu nhiệt, dấu của \(\Delta H\)dương vì năng lượng của hệ chất phản ứng nhỏ hơn năng lượng của hệ sản phẩm
b) Trong phản ứng tỏa nhiệt có sự giải phóng năng lượng
c) Trong phản ứng tỏa nhiệt, \(\Delta H\)có dấu âm vì năng lượng của hệ chất phản ứng lớn hơn năng lượng của hệ chất sản phẩm
d) Trong phản ứng thu nhiệt có sự hấp thụ năng lượng
Đáp án B
Cho phản ứng hóa học: Fe + CuSO4 → FeSO4 + Cu. Trong phản ứng trên xảy ra
-
A.
sự khử Fe2+ và sự oxi hóa Cu.
-
B.
sự khử Fe2+ và sự khử Cu2+.
-
C.
sự oxi hóa Fe và sự oxi hóa Cu.
-
D.
sự oxi hóa Fe và sự khử Cu2+.
Đáp án : D
Dựa vào sự thay đổi số oxi hóa của các chất
Trong phản ứng trên xảy ra sự oxi hóa Fe và sự khử Cu2+
Đáp án D
-
A.
–571,32 kJ.
-
B.
–856,98 kJ.
-
C.
–285,66 kJ.
-
D.
–1142,64 kJ.
Đáp án : B
Dựa vào \({\Delta _r}H_{298}^0\) (1)
Khi lấy gấp 3 lần khối lượng của các chất phản ứng thì \({\Delta _r}H_{298}^0\) = 3. -285,66 = -856,98 kJ
Đáp án B
Cho các phát biểu sau :
(1) Phản ứng phân huỷ Fe(OH)3(s) không cần cung cấp nhiệt độ liên tục.
(2) Số oxi hóa của hydrogen trong các hydride kim loại bằng +1.
(3) Trộn potassium chloride (KCl) vào nước là quá trình thu nhiệt.
(4) Phản ứng của Fe(OH)2 với dung dịch HNO3 loãng không có sự thay đổi số oxi hóa của Fe.
(5) Để giữ ấm cơ thể, trước khi lặn, người ta thường uống nước mắm cốt.
Số phát biểu đúng là
-
A.
2
-
B.
3
-
C.
5
-
D.
4
Đáp án : A
Dựa vào quá trình thu nhiệt, tỏa nhiệt
(1) sai vì cần cung cấp nhiệt độ liên tục
(2) sai, số oxi hóa của hydrogen trong hydride kim loại bằng -1
(3) đúng
(4) sai, Fe+2 tăng số oxi hóa
(5) đúng
Trong các chất sau, chất nào bền nhất về nhiệt ở điều kiện chuẩn ? Biết nhiệt tạo thành chuẩn của HCl(g) bằng -92,31 kJ.mol-1.
-
A.
O2(g)
-
B.
N2(g)
-
C.
Ca(s)
-
D.
HCl(g)
Đáp án : D
HCl(g) bền nhất ở điều kiện chuẩn
Đáp án D
a) Nhiệt lượng cần để đun sôi 30kg nước là: Q = m.C.T = 30 . 4200 . 80 = 10080000J = 10080 kJ
b) Cần cung cấp số kJ nhiệt từ đốt gas là: (10080 : 50400) : 80% = 0,25 kg
n khí = 9,916 : 24,79 = 0,4 mol
Gọi số mol NO và NO2 lần lượt là x và y
Ta có: x + y = 0,4 mol (1)
M khí = 19.2 = 38 => m khí = 38 . 0,4 = 15,2g => 30x + 46y = 15,2 (2)
Từ (1) và (2) ta có: x = y = 0,2 mol
Theo bảo toàn electron: 2n Cu = 3. n NO + n NO2 => n Cu = 0,4 mol => m Cu = 0,4 . 64 = 25,6g
Methane là thành phần chính của khí thiên nhiên. Xét phản ứng đốt cháy methane:
Dấu hiệu để nhận ra một phản ứng oxi hóa – khử là dựa trên sự thay đổi đại lượng nào sau đây của
Số oxi hóa của đơn chất luôn bằng
Phát biểu nào dưới đây không đúng?
Chromium có số oxi hóa +2 trong hợp chất nào sau đây?
>> Học trực tuyến Lớp 10 cùng thầy cô giáo giỏi tại Tuyensinh247.com, (Xem ngay) Cam kết giúp học sinh học tốt, bứt phá điểm 9,10 chỉ sau 3 tháng, làm quen kiến thức, định hướng luyện thi TN THPT, ĐGNL, ĐGTD ngay từ lớp 10
 |
 |
 |
 |
 |
 |
 |
 |











Danh sách bình luận