Bài 28. Sơ lược về phức chất trang 134, 135, 136 Hóa 12 Kết nối tri thức
Phức chất có trong một số thành phần quan trọng của sinh vật như hemoglobin, chất diệp lục,...
CH tr 134 MĐ
Trả lời câu hỏi Mở đầu trang 134 SGK Hóa 12 Kết nối tri thức
Phức chất có trong một số thành phần quan trọng của sinh vật như hemoglobin, chất diệp lục,... Một số phức chất có vai trò quan trọng trong điều trị bệnh ung thư. Vậy, phức chất là gì? Phức chất được hình thành như thế nào?
Phương pháp giải:
Nêu khái niệm phức chất và sự hình thành phức chất.
Lời giải chi tiết:
- Phức chất là hợp chất có chứa nguyên tử trung tâm (thường được kí hiệu là M) và các phối tử (thường được kí hiệu là L). Trong đó, nguyên tử trung tâm là cation kim loại hoặc nguyên tử kim loại liên kết với các phối tử. Phối tử là anion hoặc phân tử.
- Phức chất được hình thành nhờ sự cho cặp electron chưa liên kết của phối tử vào orbital trống của nguyên tử trung tâm.
CH tr 134 CH
Trả lời câu hỏi trang 134 SGK Hóa 12 Kết nối tri thức
Cho các phức chất sau: [Cu(H2O)]2+, [CoF]3-, [Ni(CO)4], [PtCl2(NH3)2].
a) Hãy chỉ ra phối tử và nguyên tử trung tâm trong mỗi phức chất trên.
b) Hãy cho biết số lượng phối tử có trong mỗi phức chất trên.
c) Hãy cho biết điện tích của mỗi phức chất trên.
Phương pháp giải:
Phức chất là hợp chất có chứa nguyên tử trung tâm (thường được kí hiệu là M) và các phối tử (thường được kí hiệu là L). Trong đó, nguyên tử trung tâm là cation kim loại hoặc nguyên tử kim loại liên kết với các phối tử. Phối tử là anion hoặc phân tử.
Lời giải chi tiết:
|
|
[Cu(H2O)6]2+ |
[CoF6]3- |
[Ni(CO)4] |
[PtCl2(NH3)2] |
|
Phối tử |
H2O |
\({{\rm{F}}^ - }\) |
CO |
\({\rm{C}}{{\rm{l}}^ - }\) |
|
NH3 |
||||
|
Nguyên tử trung tâm |
Cu2+ |
Co3- |
Ni |
\({\rm{P}}{{\rm{t}}^{2 + }}\) |
|
Số lượng phối tử |
6 |
6 |
4 |
4 |
|
Điện tích của phức chất |
+2 |
-3 |
0 |
0 |
CH tr 135 HĐ1
Trả lời câu hỏi Hoạt động 1 trang 135 SGK Hóa 12 Kết nối tri thức
Hãy xác định số lượng phối tử L trong phân tử hoặc ion phức chất ứng với mỗi dạng hình học ở Bảng 28.1.
Phương pháp giải:
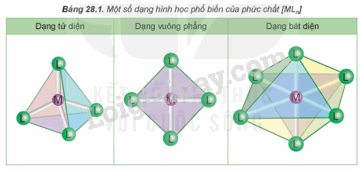
Lời giải chi tiết:
Dạng tứ diện có 4 phối tử L.
Dạng vuông phẳng có 4 phối tử L.
Dạng bát diện có 6 phối tử L.
CH tr 135 HĐ2
Trả lời câu hỏi Hoạt động 2 trang 135 SGK Hóa 12 Kết nối tri thức
Hãy dự đoán dạng hình học của phức chất [Cu(H2O)6]2+.
Phương pháp giải:

Lời giải chi tiết:
Dạng hình học của phức chất [Cu(H2O)6]2+ là dạng bát diện.
CH tr 136 CH1
Trả lời câu hỏi 1 trang 136 SGK Hóa 12 Kết nối tri thức
Cho các phức chất sau: [Ag(NH3)2]+ và [CoF6]3-.
Hãy chỉ ra nguyên tử trung tâm, phối tử và giải thích sự hình thành liên kết trong mỗi phức chất trên.
Phương pháp giải:
Liên kết hoá học giữa nguyên tử trung tâm M và phối tử L trong phức chất là liên kết cho - nhận, được hình thành nhờ sự cho cặp electron chưa liên kết của phối tử vào orbital trống của nguyên tử trung tâm.
Lời giải chi tiết:
|
|
Nguyên tử trung tâm |
Phối tử |
|
[Ag(NH3)2]+ |
Ag+ |
NH3 |
|
[CoF6]3- |
Co3+ |
\({{\rm{F}}^ - }\) |
- Sự hình thành liên kết trong phức chất [Ag(NH3)2]+ do phối tử NH3 cho cặp electron chưa liên kết vào AO trống của nguyên tử trung tâm Ag+.
- Sự hình thành liên kết trong phức chất [CoF6]3-do phối tử \({{\rm{F}}^ - }\) cho cặp electron chưa liên kết vào AO trống của nguyên tử trung tâm Co3+.
CH tr 136 CH2
Trả lời câu hỏi 2 trang 136 SGK Hóa 12 Kết nối tri thức
Phức chất aqua của Ni2+ và Zn2+ đều có dạng hình học bát diện.
a) Viết công thức hoá học của mỗi phức chất aqua trên.
b) Mô tả sự hình thành liên kết giữa phối tử và nguyên tử trung tâm trong mỗi phức chất trên.
Phương pháp giải:
Sự hình thành phức chất aqua của một số ion kim loại chuyển tiếp: Trong dung dịch, các ion kim loại chuyển tiếp Mn+ thường nhận cặp electron chưa liên kết của H2O tạo thành liên kết cộng hoá trị kiểu cho - nhận, hình thành phức chất aqua. Hầu hết các phức chất aqua có dạng hình học bát diện ([M(H2O)6]n+).
Lời giải chi tiết:
a) Phức chất aqua của Ni2+ là [Ni(H2O)6]2+.
Phức chất aqua của Zn2+ là [Zn(H2O)6]2+.
b) - Trong dung dịch, ion Ni2+ nhận cặp electron chưa liên kết của H2O tạo thành liên kết cộng hoá trị kiểu cho - nhận, hình thành phức chất aqua là [Ni(H2O)6]2+.
- Trong dung dịch, ion Zn2+ nhận cặp electron chưa liên kết của H2O tạo thành liên kết cộng hoá trị kiểu cho - nhận, hình thành phức chất aqua là [Zn(H2O)6]2+.
Luyện Bài Tập Trắc nghiệm Hóa 12 - Kết nối tri thức - Xem ngay
Các bài khác cùng chuyên mục
- Lý thuyết Một số tính chất và ứng dụng của phức chất - Hóa 12 Kết nối tri thức
- Lý thuyết Sơ lược về phức chất - Hóa 12 Kết nối tri thức
- Lý thuyết Đại cương về kim loại chuyển tiếp dãy thứ nhất - Hóa 12 Kết nối tri thức
- Lý thuyết Nguyên tố nhóm IIA - Hóa 12 Kết nối tri thức
- Lý thuyết Nguyên tố nhóm IA - Hóa 12 Kết nối tri thức













Danh sách bình luận