Bài 20. Kim loại trong tự nhiên và phương pháp tách kim loại trang 94, 95, 96 Hóa 12 Kết nối tri thức
Trong tự nhiên, các kim loại (trừ vàng, bạc và platinum)
CH tr 94
Trả lời câu hỏi Mở đầu trang 94 SGK Hóa 12 Kết nối tri thức
Trong tự nhiên, các kim loại (trừ vàng, bạc và platinum) thường tồn tại dưới dạng hợp chất trong quặng. Làm thế nào để tách kim loại ra khỏi quặng?
Phương pháp giải:
Nêu các phương pháp tách kim loại.
Lời giải chi tiết:
Để tách các kim loại ra khỏi quặng, người ta sử dụng các phương pháp sau:
- Điện phân nóng chảy để tách các kim loại hoạt động mạnh.
- Nhiệt luyện, điện phân dung dịch, thủy luyện để tách các kim loại hoạt động trung bình, yếu.
CH tr 95 CH1
Trả lời câu hỏi 1 trang 95 SGK Hóa 12 Kết nối tri thức
a) Hãy cho biết những kim loại nào tồn tại ở dạng đơn chất trong tự nhiên.
b) Hãy tìm hiểu và cho biết một số mỏ quặng kim loại quan trọng ở Việt Nam.
Phương pháp giải:
a) Trong tự nhiên, hầu hết các kim loại tồn tại ở dạng hợp chất (oxide, muối,...) trong quặng, chỉ một số kim loại kém hoạt động như vàng, bạc, platinum,... được tìm thấy dưới dạng đơn chất.
b) Tìm hiểu về một số mỏ quặng kim loại quan trọng ở Việt Nam thông qua internet.
Lời giải chi tiết:
a) Những kim loại tồn tại ở dạng đơn chất trong tự nhiên: vàng, bạc, platinum,…
b) Các mỏ quặng kim loại quan trong ở Việt Nam:
- Quặng bauxite: Đăk Nông, Lâm Đồng, Đồng Nai,…
- Quặng zinc blende: Thái Nguyên.
- Quặng chalcopyrite: Cao Bằng, Lạng Sơn, Quảng Ninh,…
CH tr 95 HĐ
Trả lời câu hỏi Hoạt động trang 95 SGK Hóa 12 Kết nối tri thức
Hãy tìm hiểu quá trình điện phân Al2O3 nóng chảy và thực hiện các yêu cầu sau:
1. Nêu vai trò của cryolite trong quá trình điện phân.
2. Tại sao sau một thời gian, cần phải thay cực dương của bình điện phân. Viết các phương trình hoá học để giải thích.
Phương pháp giải:
- Những kim loại hoạt động hoá học mạnh như K, Na, Ca, Mg, Al,... được điều chế bằng phương pháp điện phân nóng chảy các hợp chất của chúng (oxide, muối chloride).
- Nguyên tắc điện phân nóng chảy:
• Tại cathode (điện cực âm): xảy ra quá trình khử ion dương.
• Tại anode (điện cực dương): xảy ra quá trình oxi hoá ion âm.
Lời giải chi tiết:
1. Vai trò của cryolite trong quá trình điện phân:
- Hỗn hợp cryolite nóng chảy ở khoảng 900 °C, làm giảm nhiệt độ nóng chảy của Al2O3, giúp tiết kiệm năng lượng hơn.
- Cryolite có tính dẫn điện tốt hơn Al2O3 nóng chảy, làm tăng khả năng dẫn điện.
- Cryolite có khối lượng riêng nhỏ hơn nhôm, nổi lên trên và ngăn cản Al nóng chảy không bị oxi hoá trong không khí.
2. Quá trình điện phân Al2O3 diễn ra như sau:
- Cathode (-): \({\rm{A}}{{\rm{l}}^{{\rm{3 + }}}} + 3{\rm{e}} \to {\rm{Al}}\)
- Anode (+): \(2{{\rm{O}}^{2 - }} \to {{\rm{O}}_2} + 4{\rm{e}}\)
Phương trình hóa học: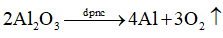
Thùng điện phân có cực âm (cathode) là tấm than chì ở đáy thùng. Cực dương (anode) là những khối than chì. Khí oxygen sinh ra ở cực dương đốt cháy dần dần than chì sinh ra CO2: 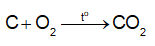
Do vậy sau một thời gian, cần phải thay cực dương của bình điện phân.
CH tr 95 CH2
Trả lời câu hỏi 2 trang 95 SGK Hóa 12 Kết nối tri thức
a) Hãy cho biết những kim loại nào thường được điều chế bằng phương pháp điện phân nóng chảy. Giải thích.
b) Hãy viết các quá trình xảy ra trên các điện cực và phương trình hoá học của phản ứng khi điện phân nóng chảy muối ăn.
Phương pháp giải:
a) Những kim loại hoạt động hoá học mạnh như K, Na, Ca, Mg, Al,... được điều chế bằng phương pháp điện phân nóng chảy các hợp chất của chúng (oxide, muối chloride).
b) Nguyên tắc điện phân nóng chảy:
• Tại cathode (điện cực âm): xảy ra quá trình khử ion dương.
• Tại anode (điện cực dương): xảy ra quá trình oxi hoá ion âm.
Lời giải chi tiết:
a) Những kim loại hoạt động hoá học mạnh như K, Na, Ca, Mg, Al,... được điều chế bằng phương pháp điện phân nóng chảy các hợp chất của chúng (oxide, muối chloride).
Không một chất hoá học nào có thể khử được các ion kim loại kiềm thành kim loại. Do đó ta phải sử dụng phương pháp điện phân để điều chế kim loại kiềm. Phương pháp điện phân dùng năng lượng của dòng điện để gây ra sự biến đổi hoá học, đó là phản ứng oxi hoá – khử. Trong sự điện phân, tác nhân khử là cực (−) mạnh hơn nhiều lần tác nhân khử là chất hoá học. Vì vậy, bằng phương pháp điện phân, người ta có thể điều chế được hầu hết các kim loại, kể cả những kim loại có tính khử mạnh nhất.
b) - Các quá trình xảy ra khi điện phân nóng chảy muối ăn:
+ Cathode (-): \({\rm{N}}{{\rm{a}}^{\rm{ + }}} + 1{\rm{e}} \to {\rm{Na}}\)
+ Anode (+): \(2{\rm{C}}{{\rm{l}}^ - } \to {\rm{C}}{{\rm{l}}_2} + 2{\rm{e}}\)
- Phương trình hóa học: 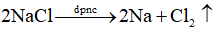
CH tr 96 CH
Trả lời câu hỏi trang 96 SGK Hóa 12 Kết nối tri thức
Hãy kể tên một số kim loại được điều chế bằng phương pháp nhiệt luyện.
Phương pháp giải:
Phương pháp nhiệt luyện:
- Nguyên tắc: Khử các oxide kim loại ở nhiệt độ cao bằng chất khử như C, CO,...
- Những kim loại có độ hoạt động trung bình, yếu như Zn, Fe, Sn, Pb, Cu,... thường được điều chế bằng phương pháp nhiệt luyện.
Lời giải chi tiết:
Phương pháp nhiệt luyện dùng để điều chế các kim loại có độ hoạt động trung bình, yếu như zinc (Zn), iron (Fe), tin (Sn), lead (Pb), copper (Cu),...
CH tr 96 HĐ
Trả lời câu hỏi Hoạt động trang 96 SGK Hóa 12 Kết nối tri thức
Quan sát Hình 20.2 và thực hiện các yêu cầu sau:
1. Cho biết điện cực nào là điện cực dương, điện cực nào là điện cực âm.
2. Hãy viết các quá trình xảy ra trên các điện cực và phương trình hoá học của phản ứng điện phân dung dịch CuSO4.
Phương pháp giải:
Nguyên tắc điện phân dung dịch: ở cathode, ưu tiên điện phân chất có tính oxi hoá mạnh hơn; ở anode, ưu tiên điện phân chất có tính khử mạnh hơn.
Lời giải chi tiết:
1. Điện cực có lớp màu đỏ đồng bám vào (bên phải) là điện cực âm, điện cực còn lại là điện cực dương.
2. Xét sơ đồ điện phân:
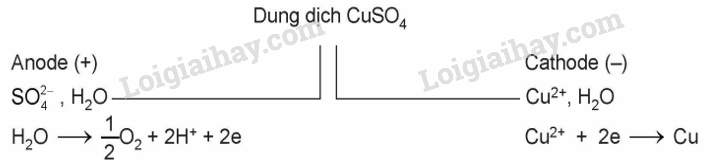
- Phương trình hóa học của phản ứng điện phân: 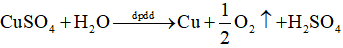
CH tr 98
Trả lời câu hỏi Hoạt động trang 98 SGK Hóa 12 Kết nối tri thức
Em hãy tìm hiểu, trình bày nhu cầu sử dụng và thực tiễn tái chế sắt, nhôm, đồng ở Việt Nam.
Phương pháp giải:
Sử dụng thông tin trang 97 sách giáo khoa học tìm hiểu qua internet.
Lời giải chi tiết:
- Tái chế sắt: Phần lớn sắt tái chế được sử dụng để sản xuất thép. Sắt thép tái chế được sử dụng trong các lĩnh vực xây dựng, sản xuất ô tô,...
- Tái chế nhôm: Nhôm tái chế được sử dụng trong các lĩnh vực như xây dựng, sản xuất ô tô, xe máy, xe đạp, thiết bị điện tử,... Hiện nay, khoảng 75% tổng lượng nhôm từng được sản xuất vẫn đang được sử dụng.
- Tái chế đồng: Đồng tái chế được sử dụng trong nhiều lĩnh vực như làm vật liệu xây dựng, phương tiện giao thông, dụng cụ nấu ăn, nhạc cụ, dây dẫn điện,...
- Bài 21. Hợp kim trang 99, 100, 101 Hóa 12 Kết nối tri thức
- Bài 22. Sự ăn mòn kim loại trang 102, 103, 104 Hóa 12 Kết nối tri thức
- Bài 23. Ôn tập chương 6 trang 107 Hóa 12 Kết nối tri thức
- Bài 19. Tính chất vật lí và tính chất hóa học của kim loại trang 89, 90, 91 Hóa 12 Kết nối tri thức
- Bài 18. Cấu tạo và liên kết trong tinh thể kim loại trang 87 Hóa 12 Kết nối tri thức
>> Xem thêm
Luyện Bài Tập Trắc nghiệm Hóa 12 - Kết nối tri thức - Xem ngay
Các bài khác cùng chuyên mục
- Lý thuyết Một số tính chất và ứng dụng của phức chất - Hóa 12 Kết nối tri thức
- Lý thuyết Sơ lược về phức chất - Hóa 12 Kết nối tri thức
- Lý thuyết Đại cương về kim loại chuyển tiếp dãy thứ nhất - Hóa 12 Kết nối tri thức
- Lý thuyết Nguyên tố nhóm IIA - Hóa 12 Kết nối tri thức
- Lý thuyết Nguyên tố nhóm IA - Hóa 12 Kết nối tri thức













Danh sách bình luận