Đề thi học kì 2 Hóa 12 Kết nối tri thức - Đề số 2
Trong mạng tinh thể kim loại, liên kết kim loại được hình thành do
Đề bài
Trong mạng tinh thể kim loại, liên kết kim loại được hình thành do
-
A.
sự góp chung electron của các nguyên tử kim loại cạnh nhau.
-
B.
lực hút tĩnh điện giữa các electron hóa trị ở các nút mạng với các ion dương kim loại chuyển động
tự do.
-
C.
lực hút tĩnh điện giữa các electron hóa trị tự do với các ion dương kim loại chuyển động tự do trong toàn bộ mạng tinh thể.
-
D.
lực hút tĩnh điện giữa các electron hóa trị tự do với các ion dương kim loại ở các nút mạng.
Cấu hình electron nguyên tử của ba nguyên tố X, Y, Z lần lượt là ls22s22p63s2, ls22s22p63s23p64s1, ls22s22p63s1. Nếu xếp theo chiều tăng dần tính kim loại thì cách sắp xếp nào sau đây đúng
-
A.
X < Z < Y.
-
B.
X ≤ Y ≤ Z.
-
C.
Z < X < Y.
-
D.
Y < Z < X.
Ở điều kiện chuẩn có các phản ứng xảy ra theo phương trình hóa học sau:
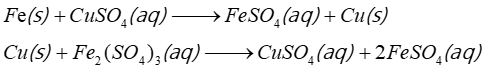
Các phản ứng trên diễn ra là do
-
A.
\(E_{C{u^{2 + }}/Cu}^0\)>\(E_{F{{\rm{e}}^{2 + }}/F{\rm{e}}}^0\)>\(E_{F{{\rm{e}}^{3 + }}/F{{\rm{e}}^{2 + }}}^0\).
-
B.
\(E_{C{u^{2 + }}/Cu}^0\)>\(E_{F{{\rm{e}}^{3 + }}/F{{\rm{e}}^{2 + }}}^0\)>\(E_{F{{\rm{e}}^{2 + }}/F{\rm{e}}}^0\).
-
C.
\(E_{F{{\rm{e}}^{2 + }}/F{\rm{e}}}^0\)>\(E_{F{{\rm{e}}^{3 + }}/F{{\rm{e}}^{2 + }}}^0\)>\(E_{C{u^{2 + }}/Cu}^0\).
-
D.
\(E_{F{{\rm{e}}^{3 + }}/F{{\rm{e}}^{2 + }}}^0\)>\(E_{C{u^{2 + }}/Cu}^0\)>\(E_{F{{\rm{e}}^{2 + }}/F{\rm{e}}}^0\).
Cho bột Fe vào dung dịch gồm AgNO3 và Cu(NO3)2. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X gồm hai muối và chất rắn Y gồm hai kim loại. Hai muối trong X và hai kim loại trong Y lần lượt là:
-
A.
Cu(NO3)2; Fe(NO3)2 và Cu; Fe.
-
B.
Cu(NO3)2; Fe(NO3)2 và Ag; Cu.
-
C.
Fe(NO3)2; Fe(NO3)3 và Cu; Ag.
-
D.
Cu(NO3)2; AgNO3 và Cu; Ag.
Thành phần chính của quặng pyrite là
-
A.
ZnS.
-
B.
FeS2.
-
C.
CuFeS2.
-
D.
Fe2O3.
Có thể thu được kim loại nào trong số các kim loại sau: Cu, Na, Ca, Al bằng cả ba phương pháp điều chế kim loại phổ biến?
-
A.
Na.
-
B.
Ca.
-
C.
Cu.
-
D.
Al.
Cho các phát biểu về tách kim loại;
(1) Đồng có thể được tách từ copper(II) oxide bằng cách nung nóng.
(2) Trong phương pháp điện phân nóng chảy aluminium oxide, có thể thu được nhôm nóng chảy ở điện cực âm của bình điện phân.
(3) Kẽm có thể được tách từ zinc oxide bằng cách nung nóng zinc oxide với carbon.
Các phát biểu đúng là
-
A.
(1) và (2).
-
B.
(1) và (3).
-
C.
(2) và (3).
-
D.
(1), (2) và (3).
Kim loại cơ bản trong duralumin và thép lần lượt là
-
A.
aluminium và magnesium.
-
B.
aluminium và iron.
-
C.
magnesium và iron.
-
D.
zinc và iron.
Sự ăn mòn kim loại
-
A.
là sự phá hủy kim loại hoặc hợp kim do các chất điện li trong môi trường.
-
B.
chính là sự ăn mòn dung dịch chất điện li.
-
C.
diễn ra trong dung dịch chất điện li.
-
D.
là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường, trong đó kim loại bị oxi hóa.
Kim loại Na, K thường được bảo quản trong
-
A.
dầu hoả.
-
B.
phenol.
-
C.
ethanol.
-
D.
bình hút ẩm.
Sodium hydroxide (hay xút ăn da) là chất rắn, không màu, dễ nóng chảy, hút ẩm mạnh, tan nhiều trong nước và tỏa ra một lượng nhiệt lớn. Công thức của sodium hydroxide là
-
A.
NaOH.
-
B.
Ca(OH)2.
-
C.
NaHCO3.
-
D.
Na2CO3.
Làm muối là nghề phổ biến tại nhiều vùng ven biển Việt Nam. Một hộ gia đình tiến hành làm muối trên ruộng chứa 200 000 L nước biển. Giả thiết 1 L nước biển có chứa 30 gam NaCl và hiệu suất quá trình làm muối thành phẩm đạt 60%. Khối lượng muối hộ gia đình thu được là:
-
A.
1200 kg.
-
B.
3600 kg.
-
C.
6000 kg.
-
D.
10000 kg.
Nước cứng có tính cứng tạm thời thường chứa các ion như
-
A.
Ca2+, Mg2+, SO42-, Cl-.
-
B.
Ca2+, Mg2+, HCO3-.
-
C.
Ca2+, Ba2+, Cl-.
-
D.
Ca2+, Mg2+, SO42-.
Phát biểu nào sau đây là đúng?
-
A.
Trong hợp chất, các kim loại nhóm IIA đều có số oxi hoá +2.
-
B.
Các kim loại nhóm IIA đều có mạng tinh thể lập phương tâm khối.
-
C.
Các hydroxide của kim loại nhóm IIA đều dễ tan trong nước.
-
D.
Trong nhóm IIA, tính khử của các kim loại giảm dần từ Be đến Ba.
Ion R3+ có số electron giống nguyên tử M. Biết rằng ion M3+ có cấu hình electron giống Ca2+. Biết Ca(Z = 20). Trong các nhận định sau:
(a) Cấu hình electron của Ca là 1s2 2s22p6 3s23p63d2.
(b) Cấu hình electron của M3+ là 1s2 2s22p6 3s23p6.
(c) Cấu hình electron của M là 1s2 2s22p6 3s23p63d3.
(d) Cấu hình electron của R3+ là 1s2 2s22p6 3s23p63d3.
Tổng số nhận định đúng là
-
A.
1
-
B.
2
-
C.
3
-
D.
4
Cho 50 mL dung dịch FeSO4 chưa rõ nồng độ vào bình tam giác, tiến hành chuẩn độ với dung dịch KMnO4 0,02 M trong môi trường acid. Kết thúc chuẩn độ tiêu tốn hết 12,0 mL dung dịch KMnO4 0,02 M. Nồng độ mol của dung dịch FeSO4 là
-
A.
0,024 M.
-
B.
0,24 M.
-
C.
2,4 M.
-
D.
0,0024 M.
Mô tả nào không đúng khi nói về phức chất [Zn(OH)4]2-?
-
A.
Có điện tích -2.
-
B.
Nguyên tử trung tâm là Zn2+.
-
C.
Phối tử là H2O.
-
D.
Số phối tử là 4.
Nhỏ vài giọt dung dịch NaCl vào ống nghiệm chứa dung dịch AgNO3, thu được kết tủa trắng AgCl Tiếp tục nhỏ vào ống nghiệm dung dịch NH3 đến dư thấy kết tủa tan, chứng tỏ phức chất [Ag(NH3)2]+ đã được tạo thành. Dấu hiệu của phản ứng tạo phức trên dựa vào:
-
A.
Sự ngưng tụ.
-
B.
Sự biến đổi màu sắc
-
C.
Sự hoà tan.
-
D.
Thay đổi nhiệt độ sôi.
Thả một đinh sắt nặng m1 gam đã được đánh sạch bề mặt vào cốc chứa dung dịch copper(II) sulfate màu xanh. Sau một thời gian thấy toàn bộ lượng đồng sinh ra đã bám vào “đinh sắt” (thực chất là phần đinh sắt chưa phản ứng). Lấy “đinh sắt” ra khỏi cốc dung dịch, sấy khô, đem cân được m2 gam. Mỗi phát biểu sau đây là đúng hay sai?
a) Phản ứng diễn ra là:
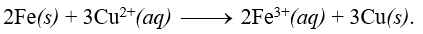
b) Màu xanh của dung dịch copper(II) sulfate nhạt dần.
c) So sánh, thu được kết quả m2 < m1.
d) Nếu thay đinh sắt ban đầu bằng thanh kẽm thì màu xanh của dung dịch không thay đổi.
Trong không khí ẩm, các vật dụng, thiết bị làm bằng gang, thép rất dễ bị ăn mòn và bị phá huỷ ở điều kiện thường. Phát biểu sau đây đúng hay sai khi nói về sự ăn mòn của gang, thép carbon trong không khí ẩm?
a) Gang, thép carbon bị phá huỷ chủ yếu do ăn mòn điện hoá học.
b) Gang, thép là hợp kim của Fe, Zn và C
c) Khi để trong không khí ẩm, trên bề mặt gang và thép xuất hiện vô số pin điện hoá.
d) Các electron của sắt (iron) được chuyển trực tiếp cho oxygen trong không khí.
Trong tự nhiên, nguyên tố Calcium không tồn tại ở dạng đơn chất mà tồn tại ở dạng hợp chất, hợp chất có nhiều trong tự nhiên chứa Ca là Calcium carbonate, có nhiều trong đá vôi, san hô, vỏ trứng, cua ... Sau khi nung đá vôi người ta thu được vôi sống ( CaO ), cho vôi sống vào nước dư thì phản ứng xảy ra rất mạnh, thu được vôi tôi chứa Ca(OH)2. Thực tế dung dịch chứa Ca(OH)2 luôn có phần màu trắng lắng xuống phía dưới và phần dung dịch phía trên gọi là nước vôi trong. Các sản phẩm ở trên đều có nhiều ứng dụng trong đời sống.
a) Nguyên tố Ca không tồn tại trong tự nhiên ở dạng đơn chất là do nó hoạt động hóa học rất mạnh.
b) Ca(OH)2 là base tan vô hạn trong nước ở điều kiện thường.
c) Khi thực hiện phản ứng tôi vôi giữa CaO với H2O, giá trị \({\Delta _r}H_{298}^o\) của phản ứng là rất nhỏ.
d) Để bảo quản trứng được lâu, người ta có thể ngâm qua trứng trong dung dịch nước vôi trong loãng rồi để khô vỏ trứng.
. Trong thành phần của một loại phèn sắt có muối Fe2(SO4)3 và một loại phèn nhôm có muối Al2(SO4)3. Kí hiệu chung của hai muối sulfate trên là M2(SO4)3. Khi hoà tan hoàn toàn phèn sắt hoặc phèn nhôm vào nước có một số quá trình quan trọng sau:
M2(SO4)3(aq) → 2M3+(aq) + 3SO42-(aq) (1)
M3+(aq) + 6H2O(l) → [M(OH2)6]3+(aq) (2)
[M(OH2)6]3+(aq) + mH2O(l) ⥦ [M(OH)m(OH2)6-m](3-m)+(aq hoặc s) + mH3O+ (aq) (3)
a) Phức chất [M(OH2)6]3+ có dạng hình học vuông phẳng.
b) Phức chất không tan, sinh ra ở quá trình (3), ứng với m = 2.
c) Sau khi dùng phèn chua thì pH của nước sẽ giảm so với ban đầu.
d) Một ứng dụng của phèn chua trong lọc nước là tác nhân để kết dính các hạt lơ lửng trong nước bị đục, loại bỏ tạp chất, giúp làm trong nước.
Cho các nguyên tử có cấu hình electron như sau :
1) 1s22s22p63s2 2) 1s22s22p1 3) 1s22s22p63s23p63d64s2
4) 1s22s22p5 5) 1s22s22p63s23p64s1 6) 1s2
Trong số các nguyên tử ở trên, có bao nhiêu nguyên tử là kim loại ?
Cho các phát biểu:
(1) Hợp kim được sử dụng trong đời sống và sản xuất phổ biến hơn so với kim loại.
(2) Kim loại A có nhiệt độ nóng chảy cao hơn kim loại B, nhiệt độ nóng chảy của hợp kim A-B luôn cao hơn nhiệt độ nóng chảy của B
(3) Tính chất hoá học của hợp kim thường tương tự tính chất của các kim loại thành phần.
(4) Hợp kim có thể cứng hơn rất nhiều các kim loại tạo nên nó.
(5) Hợp kim thường khó bị oxi hoá hơn các đơn kim loại thành phần.
Hãy liệt kê các phát biểu đúng theo số thứ tự tăng dần? (Ví dụ: 12, 135, 1234,…..)
Để lợp nhà, các tấm tôn (thép mỏng mạ kẽm) được gắn với nhau bởi các đinh thép. Theo thời gian, các tấm tôn bị ăn mòn.
(1) Vị trí đóng đinh thép dễ xảy ra ăn mòn hơn các vị trí khác.
(2) Tấm tôn bị ăn mòn từ trong ra ngoài do thép bị ăn mòn trước kẽm.
(3) Sắt trong tấm tôn không bị ăn mòn theo thời gian.
(4) Lớp tráng kẽm bị ăn mòn trước.
Số nhận định đúng ?
Tại một nhà máy, quặng bauxite được đun nóng với dung dịch NaOH 20% ở nhiệt độ 170°C – 180°C để chuyển hoá Al2O3 thành muối dễ tan theo phương trình hoá học:
Al2O3 + 2NaOH → 2NaAlO2 + H2O
Để hoà tan 1 tấn Al2O3 trong quặng bauxite cần dùng ít nhất bao nhiêu tấn dung dịch NaOH 20%? (Làm tròn kết quả đến phần trăm).
Cho các chất gồm [Ag(NH3)2]OH, [Ag(NH3)2]+, Na2[CuCl4], [CuCl4]2-, NaF, HNO3, NH3, NH4+, CH3–CO–CH3, CH3COONa. Trong các chất trên có bao nhiêu chất có liên kết cộng hoá trị theo kiểu cho – nhận?
Hemoglobin là thành phần cấu tạo nên hồng cầu trong các mạch máu. Mỗi phân tử hemoglobin chứa 4 heme B. Mỗi heme B là phức chất với nguyên tử trung tâm là sắt (iron). Heme B kết hợp thêm một phân tử oxygen thông qua đường hô hấp để vận chuyển dưỡng khí đến mô. Mỗi lần đến mô, một phân tử hemoglobin có thể đem đến cho mô tối đa bao nhiêu nguyên tử oxygen?
Lời giải và đáp án
Trong mạng tinh thể kim loại, liên kết kim loại được hình thành do
-
A.
sự góp chung electron của các nguyên tử kim loại cạnh nhau.
-
B.
lực hút tĩnh điện giữa các electron hóa trị ở các nút mạng với các ion dương kim loại chuyển động
tự do.
-
C.
lực hút tĩnh điện giữa các electron hóa trị tự do với các ion dương kim loại chuyển động tự do trong toàn bộ mạng tinh thể.
-
D.
lực hút tĩnh điện giữa các electron hóa trị tự do với các ion dương kim loại ở các nút mạng.
Đáp án : D
Dựa vào khái niệm liên kết kim loại.
Trong mạng tinh thể kim loại, liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron hoá trị tự do với các ion dương kim loại ở các nút mạng.
Đáp án D
Cấu hình electron nguyên tử của ba nguyên tố X, Y, Z lần lượt là ls22s22p63s2, ls22s22p63s23p64s1, ls22s22p63s1. Nếu xếp theo chiều tăng dần tính kim loại thì cách sắp xếp nào sau đây đúng
-
A.
X < Z < Y.
-
B.
X ≤ Y ≤ Z.
-
C.
Z < X < Y.
-
D.
Y < Z < X.
Đáp án : A
Các kim loại có số electron lớp ngoài cùng là 1,2,3.
X có tính khử yếu nhất vì thuộc nhóm IIA trong đó Z, Y đều thuộc IA, theo xu hướng biến đổi tính kim loại giảm dần.
Z, Y thuộc cùng một nhóm nên Z có tính khử mạnh hơn Y.
Thứ tự theo chiều tăng dần tính kim loại là X < Z < Y.
Đáp án A
Ở điều kiện chuẩn có các phản ứng xảy ra theo phương trình hóa học sau:
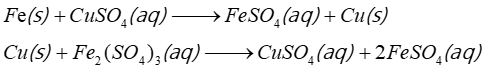
Các phản ứng trên diễn ra là do
-
A.
\(E_{C{u^{2 + }}/Cu}^0\)>\(E_{F{{\rm{e}}^{2 + }}/F{\rm{e}}}^0\)>\(E_{F{{\rm{e}}^{3 + }}/F{{\rm{e}}^{2 + }}}^0\).
-
B.
\(E_{C{u^{2 + }}/Cu}^0\)>\(E_{F{{\rm{e}}^{3 + }}/F{{\rm{e}}^{2 + }}}^0\)>\(E_{F{{\rm{e}}^{2 + }}/F{\rm{e}}}^0\).
-
C.
\(E_{F{{\rm{e}}^{2 + }}/F{\rm{e}}}^0\)>\(E_{F{{\rm{e}}^{3 + }}/F{{\rm{e}}^{2 + }}}^0\)>\(E_{C{u^{2 + }}/Cu}^0\).
-
D.
\(E_{F{{\rm{e}}^{3 + }}/F{{\rm{e}}^{2 + }}}^0\)>\(E_{C{u^{2 + }}/Cu}^0\)>\(E_{F{{\rm{e}}^{2 + }}/F{\rm{e}}}^0\).
Đáp án : D
Dựa vào ý nghĩa của thế điện cực của kim loại.
Fe khử được Cu2+, Cu khử được Fe3+ nên \(E_{F{{\rm{e}}^{3 + }}/F{{\rm{e}}^{2 + }}}^0\)>\(E_{C{u^{2 + }}/Cu}^0\)>\(E_{F{{\rm{e}}^{2 + }}/F{\rm{e}}}^0\).
Đáp án D
Cho bột Fe vào dung dịch gồm AgNO3 và Cu(NO3)2. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X gồm hai muối và chất rắn Y gồm hai kim loại. Hai muối trong X và hai kim loại trong Y lần lượt là:
-
A.
Cu(NO3)2; Fe(NO3)2 và Cu; Fe.
-
B.
Cu(NO3)2; Fe(NO3)2 và Ag; Cu.
-
C.
Fe(NO3)2; Fe(NO3)3 và Cu; Ag.
-
D.
Cu(NO3)2; AgNO3 và Cu; Ag.
Đáp án : B
Dựa vào tính chất hoá học của kim loại.
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
Vì thu được dung dịch X gồm 2 muối nên Cu(NO3)2 còn dư, chất rắn Y gồm Cu và Ag.
Đáp án B
Thành phần chính của quặng pyrite là
-
A.
ZnS.
-
B.
FeS2.
-
C.
CuFeS2.
-
D.
Fe2O3.
Đáp án : B
Dựa vào kim loại trong tự nhiên.
Thành phần chính của quặng pyrite là FeS2.
Đáp án B
Có thể thu được kim loại nào trong số các kim loại sau: Cu, Na, Ca, Al bằng cả ba phương pháp điều chế kim loại phổ biến?
-
A.
Na.
-
B.
Ca.
-
C.
Cu.
-
D.
Al.
Đáp án : C
Phương pháp điều chế kim loại: điện phân nóng chảy, nhiệt luyện, thuỷ luyện, điện phân dung dịch.
Cu là kim loại trung bình yếu nên có thể điều chế bằng nhiều phương pháp.
Đáp án C
Cho các phát biểu về tách kim loại;
(1) Đồng có thể được tách từ copper(II) oxide bằng cách nung nóng.
(2) Trong phương pháp điện phân nóng chảy aluminium oxide, có thể thu được nhôm nóng chảy ở điện cực âm của bình điện phân.
(3) Kẽm có thể được tách từ zinc oxide bằng cách nung nóng zinc oxide với carbon.
Các phát biểu đúng là
-
A.
(1) và (2).
-
B.
(1) và (3).
-
C.
(2) và (3).
-
D.
(1), (2) và (3).
Đáp án : C
Dựa vào phương pháp tách kim loại.
(1) sai, không thu được Cu khi đun nóng CuO.
(2) đúng.
(3) đúng
Đáp án C
Kim loại cơ bản trong duralumin và thép lần lượt là
-
A.
aluminium và magnesium.
-
B.
aluminium và iron.
-
C.
magnesium và iron.
-
D.
zinc và iron.
Đáp án : B
Dựa vào thành phần của hợp kim.
Kim loại cơ bản trong duralumin và thép lần lượt là Al và Fe.
Đáp án B
Sự ăn mòn kim loại
-
A.
là sự phá hủy kim loại hoặc hợp kim do các chất điện li trong môi trường.
-
B.
chính là sự ăn mòn dung dịch chất điện li.
-
C.
diễn ra trong dung dịch chất điện li.
-
D.
là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường, trong đó kim loại bị oxi hóa.
Đáp án : D
Dựa vào khái niệm sự ăn mòn kim loại.
Sự ăn mòn kim loại là sự phá huỷ kim loại hoặc hợp kim do tác dụng của các chất trong môi trường, trong đó kim loại bị oxi hoá.
Đáp án D
Kim loại Na, K thường được bảo quản trong
-
A.
dầu hoả.
-
B.
phenol.
-
C.
ethanol.
-
D.
bình hút ẩm.
Đáp án : A
Dựa vào tính chất hoá học của kim loại.
Kim loại Na, K thường được bảo quản trong dầu hoả.
Đáp án A
Sodium hydroxide (hay xút ăn da) là chất rắn, không màu, dễ nóng chảy, hút ẩm mạnh, tan nhiều trong nước và tỏa ra một lượng nhiệt lớn. Công thức của sodium hydroxide là
-
A.
NaOH.
-
B.
Ca(OH)2.
-
C.
NaHCO3.
-
D.
Na2CO3.
Đáp án : A
Dựa vào hợp chất nhóm IA.
Sodium hydroxide có công thức NaOH.
Đáp án A
Làm muối là nghề phổ biến tại nhiều vùng ven biển Việt Nam. Một hộ gia đình tiến hành làm muối trên ruộng chứa 200 000 L nước biển. Giả thiết 1 L nước biển có chứa 30 gam NaCl và hiệu suất quá trình làm muối thành phẩm đạt 60%. Khối lượng muối hộ gia đình thu được là:
-
A.
1200 kg.
-
B.
3600 kg.
-
C.
6000 kg.
-
D.
10000 kg.
Đáp án : B
Tính khối lượng NaCl trong 200 000L nước biển.
Khối lượng muối ăn thành phẩm là: 200 000 . 30 . 60% = 3600000g = 3600kg
Đáp án B
Nước cứng có tính cứng tạm thời thường chứa các ion như
-
A.
Ca2+, Mg2+, SO42-, Cl-.
-
B.
Ca2+, Mg2+, HCO3-.
-
C.
Ca2+, Ba2+, Cl-.
-
D.
Ca2+, Mg2+, SO42-.
Đáp án : B
Dựa vào phân loại nước cứng.
Nước cứng có tính cứng tạm thời thường chứa các ion như Ca2+, Mg2+, HCO3-.
Đáp án B.
Phát biểu nào sau đây là đúng?
-
A.
Trong hợp chất, các kim loại nhóm IIA đều có số oxi hoá +2.
-
B.
Các kim loại nhóm IIA đều có mạng tinh thể lập phương tâm khối.
-
C.
Các hydroxide của kim loại nhóm IIA đều dễ tan trong nước.
-
D.
Trong nhóm IIA, tính khử của các kim loại giảm dần từ Be đến Ba.
Đáp án : A
Dựa vào tính chất của hợp chất nhóm IIA.
Trong hợp chất, các kim loại nhóm IIA đều có số oix hoá +2.
Đáp án A
Ion R3+ có số electron giống nguyên tử M. Biết rằng ion M3+ có cấu hình electron giống Ca2+. Biết Ca(Z = 20). Trong các nhận định sau:
(a) Cấu hình electron của Ca là 1s2 2s22p6 3s23p63d2.
(b) Cấu hình electron của M3+ là 1s2 2s22p6 3s23p6.
(c) Cấu hình electron của M là 1s2 2s22p6 3s23p63d3.
(d) Cấu hình electron của R3+ là 1s2 2s22p6 3s23p63d3.
Tổng số nhận định đúng là
-
A.
1
-
B.
2
-
C.
3
-
D.
4
Đáp án : B
Dựa vào đặc điểm cấu hình của các nguyên tử và ion.
(a) sai, Cấu hình electron của Ca là 1s2 2s22p6 3s23p64s2.
(b) đúng
(c) sai, cấu hình của M là 1s2 2s22p6 3s23p63d3.
(d) đúng.
Đáp án B
Cho 50 mL dung dịch FeSO4 chưa rõ nồng độ vào bình tam giác, tiến hành chuẩn độ với dung dịch KMnO4 0,02 M trong môi trường acid. Kết thúc chuẩn độ tiêu tốn hết 12,0 mL dung dịch KMnO4 0,02 M. Nồng độ mol của dung dịch FeSO4 là
-
A.
0,024 M.
-
B.
0,24 M.
-
C.
2,4 M.
-
D.
0,0024 M.
Đáp án : A
Dựa vào phương pháp chuẩn độ FeSO4.
n KMnO4 = 12.0,02 = 0,24 mmol.
10FeSO4 + 18H2SO4 + 2KMnO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 18H2O
1,2 ← 0,24
CM FeSO4 = 1,2 : 50 = 0,024M.
Đáp án A
Mô tả nào không đúng khi nói về phức chất [Zn(OH)4]2-?
-
A.
Có điện tích -2.
-
B.
Nguyên tử trung tâm là Zn2+.
-
C.
Phối tử là H2O.
-
D.
Số phối tử là 4.
Đáp án : C
Dựa vào cấu tạo của phức chất.
Phối tử trong phức [Zn(OH)4]2- là OH-
Đáp án C
Nhỏ vài giọt dung dịch NaCl vào ống nghiệm chứa dung dịch AgNO3, thu được kết tủa trắng AgCl Tiếp tục nhỏ vào ống nghiệm dung dịch NH3 đến dư thấy kết tủa tan, chứng tỏ phức chất [Ag(NH3)2]+ đã được tạo thành. Dấu hiệu của phản ứng tạo phức trên dựa vào:
-
A.
Sự ngưng tụ.
-
B.
Sự biến đổi màu sắc
-
C.
Sự hoà tan.
-
D.
Thay đổi nhiệt độ sôi.
Đáp án : C
Dựa vào hiện tượng của phản ứng.
Khi nhỏ dung dịch NH3 vào kết tủa thấy kết tủa tan dần chứng tỏ đã có sự tạo thành phức chất.
Đáp án C
Thả một đinh sắt nặng m1 gam đã được đánh sạch bề mặt vào cốc chứa dung dịch copper(II) sulfate màu xanh. Sau một thời gian thấy toàn bộ lượng đồng sinh ra đã bám vào “đinh sắt” (thực chất là phần đinh sắt chưa phản ứng). Lấy “đinh sắt” ra khỏi cốc dung dịch, sấy khô, đem cân được m2 gam. Mỗi phát biểu sau đây là đúng hay sai?
a) Phản ứng diễn ra là:
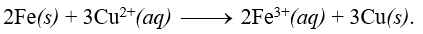
b) Màu xanh của dung dịch copper(II) sulfate nhạt dần.
c) So sánh, thu được kết quả m2 < m1.
d) Nếu thay đinh sắt ban đầu bằng thanh kẽm thì màu xanh của dung dịch không thay đổi.
a) Phản ứng diễn ra là:
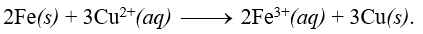
b) Màu xanh của dung dịch copper(II) sulfate nhạt dần.
c) So sánh, thu được kết quả m2 < m1.
d) Nếu thay đinh sắt ban đầu bằng thanh kẽm thì màu xanh của dung dịch không thay đổi.
Dựa vào nguyên tắc hoạt động của pin.
a) sai, phản ứng diễn ra là: 
b) đúng
c) sai, kết quả thu được m2 > m1 do khối lượng Cu sinh ra lớn hơn lượng Fe bị hoà tan.
d) sai, hiện tượng phản ứng tương tự.
Trong không khí ẩm, các vật dụng, thiết bị làm bằng gang, thép rất dễ bị ăn mòn và bị phá huỷ ở điều kiện thường. Phát biểu sau đây đúng hay sai khi nói về sự ăn mòn của gang, thép carbon trong không khí ẩm?
a) Gang, thép carbon bị phá huỷ chủ yếu do ăn mòn điện hoá học.
b) Gang, thép là hợp kim của Fe, Zn và C
c) Khi để trong không khí ẩm, trên bề mặt gang và thép xuất hiện vô số pin điện hoá.
d) Các electron của sắt (iron) được chuyển trực tiếp cho oxygen trong không khí.
a) Gang, thép carbon bị phá huỷ chủ yếu do ăn mòn điện hoá học.
b) Gang, thép là hợp kim của Fe, Zn và C
c) Khi để trong không khí ẩm, trên bề mặt gang và thép xuất hiện vô số pin điện hoá.
d) Các electron của sắt (iron) được chuyển trực tiếp cho oxygen trong không khí.
Dựa vào sự ăn mòn kim loại.
a) đúng, vì gang, thép có đủ 2 điện cực.
b) sai, gang thép là hợp kim của Fe, C.
c) đúng
d) sai, các electron của sắt được chuyển trực tiếp cho carbon.
Trong tự nhiên, nguyên tố Calcium không tồn tại ở dạng đơn chất mà tồn tại ở dạng hợp chất, hợp chất có nhiều trong tự nhiên chứa Ca là Calcium carbonate, có nhiều trong đá vôi, san hô, vỏ trứng, cua ... Sau khi nung đá vôi người ta thu được vôi sống ( CaO ), cho vôi sống vào nước dư thì phản ứng xảy ra rất mạnh, thu được vôi tôi chứa Ca(OH)2. Thực tế dung dịch chứa Ca(OH)2 luôn có phần màu trắng lắng xuống phía dưới và phần dung dịch phía trên gọi là nước vôi trong. Các sản phẩm ở trên đều có nhiều ứng dụng trong đời sống.
a) Nguyên tố Ca không tồn tại trong tự nhiên ở dạng đơn chất là do nó hoạt động hóa học rất mạnh.
b) Ca(OH)2 là base tan vô hạn trong nước ở điều kiện thường.
c) Khi thực hiện phản ứng tôi vôi giữa CaO với H2O, giá trị \({\Delta _r}H_{298}^o\) của phản ứng là rất nhỏ.
d) Để bảo quản trứng được lâu, người ta có thể ngâm qua trứng trong dung dịch nước vôi trong loãng rồi để khô vỏ trứng.
a) Nguyên tố Ca không tồn tại trong tự nhiên ở dạng đơn chất là do nó hoạt động hóa học rất mạnh.
b) Ca(OH)2 là base tan vô hạn trong nước ở điều kiện thường.
c) Khi thực hiện phản ứng tôi vôi giữa CaO với H2O, giá trị \({\Delta _r}H_{298}^o\) của phản ứng là rất nhỏ.
d) Để bảo quản trứng được lâu, người ta có thể ngâm qua trứng trong dung dịch nước vôi trong loãng rồi để khô vỏ trứng.
Dựa vào tính chất hoá học của nhóm IIA.
a) đúng
b) sai, Ca(OH)2 tan một phần trong nước ở điều kiện thường.
c) sai, phản ứng toả nhiệt mạnh.
d) đúng, vì có hiện tượng vôi hoá vỏ trứng khiến trứng bảo quản được lâu hơn.
. Trong thành phần của một loại phèn sắt có muối Fe2(SO4)3 và một loại phèn nhôm có muối Al2(SO4)3. Kí hiệu chung của hai muối sulfate trên là M2(SO4)3. Khi hoà tan hoàn toàn phèn sắt hoặc phèn nhôm vào nước có một số quá trình quan trọng sau:
M2(SO4)3(aq) → 2M3+(aq) + 3SO42-(aq) (1)
M3+(aq) + 6H2O(l) → [M(OH2)6]3+(aq) (2)
[M(OH2)6]3+(aq) + mH2O(l) ⥦ [M(OH)m(OH2)6-m](3-m)+(aq hoặc s) + mH3O+ (aq) (3)
a) Phức chất [M(OH2)6]3+ có dạng hình học vuông phẳng.
b) Phức chất không tan, sinh ra ở quá trình (3), ứng với m = 2.
c) Sau khi dùng phèn chua thì pH của nước sẽ giảm so với ban đầu.
d) Một ứng dụng của phèn chua trong lọc nước là tác nhân để kết dính các hạt lơ lửng trong nước bị đục, loại bỏ tạp chất, giúp làm trong nước.
a) Phức chất [M(OH2)6]3+ có dạng hình học vuông phẳng.
b) Phức chất không tan, sinh ra ở quá trình (3), ứng với m = 2.
c) Sau khi dùng phèn chua thì pH của nước sẽ giảm so với ban đầu.
d) Một ứng dụng của phèn chua trong lọc nước là tác nhân để kết dính các hạt lơ lửng trong nước bị đục, loại bỏ tạp chất, giúp làm trong nước.
Dựa vào phản ứng xảy ra khi cho phèn chua vào nước.
a) sai, có dạng hình bát diện.
b) sai, phức chất không tan ứng với m = 0.
c) đúng
d) đúng
Cho các nguyên tử có cấu hình electron như sau :
1) 1s22s22p63s2 2) 1s22s22p1 3) 1s22s22p63s23p63d64s2
4) 1s22s22p5 5) 1s22s22p63s23p64s1 6) 1s2
Trong số các nguyên tử ở trên, có bao nhiêu nguyên tử là kim loại ?
Các kim loại thường có 1,2,3 electron lớp ngoài cùng.
1), 2), 5) là cấu hình electron lớp ngoài cùng.
Đáp án: 3.
Cho các phát biểu:
(1) Hợp kim được sử dụng trong đời sống và sản xuất phổ biến hơn so với kim loại.
(2) Kim loại A có nhiệt độ nóng chảy cao hơn kim loại B, nhiệt độ nóng chảy của hợp kim A-B luôn cao hơn nhiệt độ nóng chảy của B
(3) Tính chất hoá học của hợp kim thường tương tự tính chất của các kim loại thành phần.
(4) Hợp kim có thể cứng hơn rất nhiều các kim loại tạo nên nó.
(5) Hợp kim thường khó bị oxi hoá hơn các đơn kim loại thành phần.
Hãy liệt kê các phát biểu đúng theo số thứ tự tăng dần? (Ví dụ: 12, 135, 1234,…..)
Dựa vào tính chất hoá học của hợp kim.
(1), (3), (4), (5) đúng
(2) sai vì tuỳ vào loại hợp kim.
Đáp án: 1345.
Để lợp nhà, các tấm tôn (thép mỏng mạ kẽm) được gắn với nhau bởi các đinh thép. Theo thời gian, các tấm tôn bị ăn mòn.
(1) Vị trí đóng đinh thép dễ xảy ra ăn mòn hơn các vị trí khác.
(2) Tấm tôn bị ăn mòn từ trong ra ngoài do thép bị ăn mòn trước kẽm.
(3) Sắt trong tấm tôn không bị ăn mòn theo thời gian.
(4) Lớp tráng kẽm bị ăn mòn trước.
Số nhận định đúng ?
Dựa vào sự ăn mòn kim loại.
(1) đúng
(2) sai, kẽm bị ăn mòn trước thép
(3) sai, sắt có bị ăn mòn nếu tấm kẽm bị ăn mòn hết.
(4) đúng.
Đáp án: 2
Tại một nhà máy, quặng bauxite được đun nóng với dung dịch NaOH 20% ở nhiệt độ 170°C – 180°C để chuyển hoá Al2O3 thành muối dễ tan theo phương trình hoá học:
Al2O3 + 2NaOH → 2NaAlO2 + H2O
Để hoà tan 1 tấn Al2O3 trong quặng bauxite cần dùng ít nhất bao nhiêu tấn dung dịch NaOH 20%? (Làm tròn kết quả đến phần trăm).
Tính số mol Al2O3, từ phương trình tính được số mol NaOH.
n Al2O3 = \(\frac{1}{{102}}\)tấn mol
theo phương trình: n NaOH = 2 n Al2O3 = \(\frac{2}{{102}}\)tấn mol
m dung dịch NaOH = \(\frac{{\frac{2}{{102}}.40}}{{20\% }}\)= 3,92 tấn
Đáp án: 3,92.
Cho các chất gồm [Ag(NH3)2]OH, [Ag(NH3)2]+, Na2[CuCl4], [CuCl4]2-, NaF, HNO3, NH3, NH4+, CH3–CO–CH3, CH3COONa. Trong các chất trên có bao nhiêu chất có liên kết cộng hoá trị theo kiểu cho – nhận?
Các phức chất thường có liên kết cộng hoá trị theo kiểu cho – nhận.
[Ag(NH3)2]OH, [Ag(NH3)2]+, Na2[CuCl4], [CuCl4]2-, HNO3, NH4+.
Đáp án: 6
Hemoglobin là thành phần cấu tạo nên hồng cầu trong các mạch máu. Mỗi phân tử hemoglobin chứa 4 heme B. Mỗi heme B là phức chất với nguyên tử trung tâm là sắt (iron). Heme B kết hợp thêm một phân tử oxygen thông qua đường hô hấp để vận chuyển dưỡng khí đến mô. Mỗi lần đến mô, một phân tử hemoglobin có thể đem đến cho mô tối đa bao nhiêu nguyên tử oxygen?
Mỗi hemoglobin kết hợp với 1 phân tử oxygen.
4 heme B có thể đem đến cho mô tối đa 4 phân tử oxygen tương đương 8 nguyên tử oxygen.
Đáp án: 8
Cho phát biểu sau: “Phức chất đơn giản thường có một ...(1)...
Các rạn san hô và đá vôi có thành phần chính là:
Hợp chất Kn[Fe(CN)6], trong đó Fe có số oxi hóa +3. Giá trị của n bằng
Nhiệt độ nóng chảy của các kim loại nhóm IA từ Li đến Cs biến đổi như thế nào?










Danh sách bình luận