Đề thi học kì 2 Hóa 12 Kết nối tri thức - Đề số 1
Nhiệt độ nóng chảy của các kim loại nhóm IA từ Li đến Cs biến đổi như thế nào?
Đề bài
Nhiệt độ nóng chảy của các kim loại nhóm IA từ Li đến Cs biến đổi như thế nào?
-
A.
Tăng dần.
-
B.
Không đổi.
-
C.
Không có quy luật.
-
D.
Giảm dần.
Chromium được sử dụng để cắt thuỷ tinh có thể được giải thích dựa vào tính chất vật lí nào?
-
A.
Tính cứng.
-
B.
Tính dẫn điện.
-
C.
Tính dẻo.
-
D.
Tính dẫn nhiệt.
Chất nào dưới đây là thành phần chính của quặng hematite?
-
A.
Iron(II) oxide.
-
B.
Iron(III) oxide.
-
C.
Iron.
-
D.
Iron(II) sulfide.
Ở nhiệt độ thường, kim loại nào sau đây phản ứng chậm với nước?
-
A.
Mg.
-
B.
Ca .
-
C.
Sr .
-
D.
Ba.
Trong các mẫu nước cứng sau đây, nước cứng tạm thời là
-
A.
dung dich \({\rm{Ca}}{\left( {{\rm{HC}}{{\rm{O}}_3}} \right)_2}\).
-
B.
dung dịch \({\rm{MgS}}{{\rm{O}}_4}\).
-
C.
dung dịch \({\rm{CaC}}{{\rm{l}}_2}\).
-
D.
dung dịch \({\rm{Mg}}{\left( {{\rm{N}}{{\rm{O}}_3}} \right)_2}\).
Đặc điểm chung cấu hình electron của nguyên tử kim loại chuyển tiếp dãy thứ nhất là
-
A.
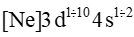
-
B.
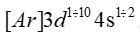
-
C.
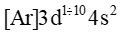
-
D.
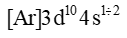
Nhúng thanh kẽm vào dung dịch chất nào sau đây sẽ xảy ra hiện tượng ăn mòn điện hoá?
-
A.
KCl .
-
B.
HCl .
-
C.
\({\rm{CuS}}{{\rm{O}}_4}\).
-
D.
\({\rm{MgC}}{{\rm{l}}_2}\).
Phương pháp chung để điều chế các kim loại \({\rm{Na}},{\rm{Ca}},{\rm{Al}}\) trong công nghiệp là
-
A.
điện phân dung dịch.
-
B.
điện phân nóng chảy.
-
C.
nhiệt luyện.
-
D.
thuỷ luyện.
Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường, tạo ra dung dịch có môi trường kiềm là
-
A.
Na, Ba, K.
-
B.
\({\rm{Be}},{\rm{Na}},{\rm{Ca}}\).
-
C.
\({\rm{Na}},{\rm{Fe}},{\rm{K}}\).
-
D.
\({\rm{Na}},{\rm{Cr}},{\rm{K}}\)
Trạng thái oxi hoá phổ biến của Fe và Mn tương ứng là
-
A.
\( + 2, + 3\) và \( + 2, + 4, + 7\).
-
B.
\( + 2, + 3\) và \( + 2, + 4, + 6\).
-
C.
\( + 2, + 3\) và \( + 2, + 6, + 7\).
-
D.
\( + 2, + 6\) và \( + 2, + 4, + 7\).
Khi đốt nóng tinh thể LiCl trong ngọn lửa đèn khí không màu thì tạo ra ngọn lửa có màu
-
A.
da cam.
-
B.
tím nhạt.
-
C.
vàng.
-
D.
đỏ tía.
Hợp chất nào sau đây vừa tác dụng được với dung dịch HCl , vừa tác dụng được với dung dịch NaOH ?
-
A.
\({\rm{NaHC}}{{\rm{O}}_3}\).
-
B.
NaCl .
-
C.
\({\rm{Ba}}{({\rm{OH}})_2}\).
-
D.
\({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\).
Khi đốt cháy kim loại Na trong bình chứa khí oxygen tạo thành sản phẩm là
-
A.
NaO .
-
B.
\({\rm{N}}{{\rm{a}}_2}{{\rm{O}}_2}\).
-
C.
\({\rm{N}}{{\rm{a}}_2}{\rm{O}}\).
-
D.
\({\rm{Na}}{{\rm{O}}_2}\).
Ở nơi tồn ứ rác thải, chất nào sau đây được các công nhân vệ sinh môi trường dùng để xử lí tạm thời nhằm sát trùng, diệt khuẩn, phòng chống dịch bệnh?
-
A.
Cát vàng.
-
B.
Than đá.
-
C.
Đá vôi.
-
D.
Vôi bột.
Nước cứng gây nhiều tác hại trong đời sống và sản xuất như đóng cặn đường ống dẫn nước, làm cho xà phòng có ít bọt khi giặt quần áo, làm giảm mùi vị thực phẩm khi nấu ăn. Nước cứng là nước có chứa nhiều các ion
-
A.
\({\rm{M}}{{\rm{g}}^{2 + }}\) và \({\rm{C}}{{\rm{a}}^{2 + }}\).
-
B.
\({\rm{N}}{{\rm{a}}^ + }\)và \({{\rm{K}}^ + }\).
-
C.
\({{\rm{F}}^ - }\)và \({\rm{C}}{{\rm{l}}^ - }\).
-
D.
\({\rm{SO}}_4^{2 - }\) và \({\rm{CO}}_3^{2 - }\).
Tiến hành các thí nghiệm sau:
(1) Sục khí \({\rm{C}}{{\rm{O}}_2}\) dư vào dung dịch \({\rm{Ca}}{({\rm{OH}})_2}\).
(2) Cho dung dịch NaOH dư vào dung dịch \({\rm{Ba}}{\left( {{\rm{HC}}{{\rm{O}}_3}} \right)_2}\).
(3) Đun sôi một mẫu nước có tính cứng tạm thời.
(4) Cho dung dịch \({\rm{KHS}}{{\rm{O}}_4}\) vào dung dịch \({\rm{Ba}}{({\rm{OH}})_2}\).
Khi kết thúc phản ứng, số thí nghiệm thu được kết tủa là
-
A.
1
-
B.
3
-
C.
2
-
D.
4
"Thép 304 " là một loại thép không gỉ được dùng phổ biến trong đời sống. Các kim loại chủ yếu tạo nên loại thép này bao gồm:
-
A.
Fe, C,Cr.
-
B.
Fe,Cu, Cr.
-
C.
Fe,Cr, Ni.
-
D.
Fe,C, Cr, Ni.
Trong ion phức chất [Co(NH3)6]3+, nguyên tử trung tâm là
-
A.
Co3+.
-
B.
N.
-
C.
H.
-
D.
NH3.
Các phương pháp để điều chế kim loại như sau:
a. Các kim loại đều có thể điều chế bằng phương pháp dùng CO khử oxide kim loại tương ứng.
b. Trong công nghiệp, kim loại Al chỉ có thể điều chế được bằng phương pháp điện phân.
c. Để tách Ag khỏi các tạp chất \({\rm{Fe}},{\rm{Cu}}\) ta có thể cho hỗn hợp vào dung dịch \({\rm{AgN}}{{\rm{O}}_3}\) dư.
d. Trong công nghiệp, kim loại Na được điều chế bằng cách điện phân dung dịch NaCl .
Tiến hành thí nghiệm kim loại tác dụng với dung dịch muối:
Chuẩn bị:
- Hoá chất: Đinh sắt đã được đánh sạch bề mặt, dung dịch copper (II) sulfate 1M.
- Dụng cụ: Cốc thủy tinh.
Tiến hành: Cho đinh sắt vào cốc thủy tinh chứa dung dịch copper (II) sulfate 1M.
a. Thấy có bọt khí thoát ra.
b. Thấy xuất hiện kết tủa màu xanh.
c. Thấy có lớp kim loại đồng bám vào đinh sắt, dung dịch nhạt màu dần.
d. Thanh sắt tan dần, có lớp kim loại đồng bám vào, dung dịch nhạt màu dần.
Những phát biểu khi nói về khả năng phản ứng của kim loại với sulfuric acid?
a. Chỉ các kim loại đứng trước H mới tham gia phản ứng với H2SO4 loãng.
b. Các kim loại sắt, nhôm, chromium phản ứng được với dung dịch sulfuric acid đặc ở nhiệt độ cao, không phản ứng với dung dịch sulfuric acid đặc, nguội do sulfuric acid đặc nguội đã oxi hóa bề mặt kim loại tạo thành màng oxide có tính trơ, làm cho các kim loại này bị thụ động.
c. Hiện tượng các kim loại sắt, nhôm, chromium không phản ứng với dung dịch sulfuric acid đặc, nguội được gọi là hiện tượng thụ động hóa, tương tự đối với nitric acid.
d. Có thể dùng dung dịch sulfuric acid loãng để phân biệt đoạn dây bạc và đoạn dây platium.
Có nhiều phương pháp để chống ăn mòn kim loại.
a) Phương pháp phủ sơn là một trong những cách phổ biến để bảo vệ kim loại.
b) Gắn tấm kẽm vào vỏ tàu biển giúp bảo vệ kim loại bằng cách tạo ra điện hóa.
c) Sử dụng thép không gỉ là phương pháp hiệu quả nhất trong mọi trường hợp để ngăn ngừa ăn mòn.
d) Giảm độ ẩm môi trường xung quanh có thể hạn chế ăn mòn kim loại.
Cho dãy các kim loại: Na, Cu, Fe, Ag, Zn. Số kim loại trong dãy phản ứng được với dung dịch HCl là ?
Cho phương trình hóa học của phản ứng sau:
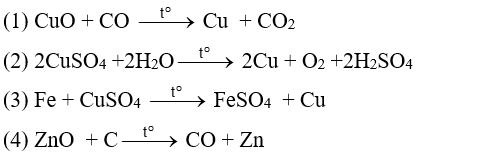
Liệt kê số phản ứng có thể được dùng để điều chế kim loại bằng phương pháp nhiệt luyện theo thứ tự giảm dần.
Thí nghiệm về sự tạo thành phức chất của Cu2+
Bước 1: Cho khoảng 1 mL dung dịch CuSO4 5% vào ống nghiệm (1). Cho tiếp 3 giọt dung dịch NaOH 10% vào ống nghiệm, lắc đều.
Bước 2: Nhỏ từ từ dung dịch NH3 10% vào ống nghiệm (1), vừa nhỏ vừa lắc đều đến khi kết tủa tan hoàn toàn.
Bước 3: Cho khoảng 1 mL dung dịch CuSO4 5% vào ống nghiệm (2). Nhỏ từ từ dung dịch HCl đặc vào ống nghiệm, vừa nhỏ vừa lắc đều đến khi dung dịch chuyển màu hoàn toàn.
Hiện tượng và viết phương trình hoá học của các phản ứng xảy ra như sau:
(1) Sau bước 1: Ống nghiệm (1) ban đầu xuất hiện kết tủa xanh.
(2) Sau bước 2: Khi cho từ từ dung dịch NH3 vào thì kết tủa xanh tan dần do tạo thành phức chất có màu xanh lam.
(3) Sau bước 2: Phương trình tạo thành phức chất có màu xanh lam là
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2.
(4) Sau bước 3: Ống nghiệm (2) Dung dịch chuyển từ màu xanh sang xanh lá, cuối cùng là màu vàng.
(5) Sau bước 3: Phương trình tạo thành phức chất có màu xanh lam là
CuSO4 + 4HCl → H2[CuCl4] + H2SO4
Có bao nhiêu phát biểu đúng?
Vàng (Au) đơn chất tồn tại trong tự nhiên ở trong quặng vàng thường có hàm lượng vàng thấp. Để thu hồi vàng từ quặng vàng, người ta nghiền quặng, hoà tan chúng vào dung dịch KCN và liên tục sục không khí vào. Vàng bị hoà tan tạo thành phức chất:
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l)→ 4K[Au(CN)2](aq) + 4KOH(aq) (1)
và sau đó kết tủa vàng bằng kẽm (Zn):
Zn(s) + 2K[Au(CN)2] (aq) → K2[Zn(CN)4](aq) + 2Au(s) (2)
Nếu dùng 13 kg KCN thì có thể tách được bao nhiêu kg vàng từ quặng theo chuỗi phản ứng trên? Giả thiết các chất khác trong quặng không phản ứng với KCN.
Một viên thực phẩm chức năng có khối lượng 250 mg chứa nguyên tố sắt (iron) ở dạng muối Fe(II) cùng một số chất khác. Kết quả kiểm nghiệm thấy lượng Fe(II) trong viên này phản ứng vừa đủ với 8,5 mL dung dịch KMnO4 0,04M. Phần trăm khối lượng của nguyên tố sắt trong viên thực phẩm chức năng trên là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
Lời giải và đáp án
Nhiệt độ nóng chảy của các kim loại nhóm IA từ Li đến Cs biến đổi như thế nào?
-
A.
Tăng dần.
-
B.
Không đổi.
-
C.
Không có quy luật.
-
D.
Giảm dần.
Đáp án : D
Dựa vào tính chất vật lí của nhóm IA.
Nhiệt độ nóng chảy của các kim loại IA từ Li đến Cs giảm dần.
Đáp án D
Chromium được sử dụng để cắt thuỷ tinh có thể được giải thích dựa vào tính chất vật lí nào?
-
A.
Tính cứng.
-
B.
Tính dẫn điện.
-
C.
Tính dẻo.
-
D.
Tính dẫn nhiệt.
Đáp án : A
Dựa vào tính chất hoá học của kim loại.
Cr được sử dụng để cắt thuỷ tinh do tính cứng của Cr.
Đáp án A
Chất nào dưới đây là thành phần chính của quặng hematite?
-
A.
Iron(II) oxide.
-
B.
Iron(III) oxide.
-
C.
Iron.
-
D.
Iron(II) sulfide.
Đáp án : B
Dựa vào trạng thái tự nhiên của kim loại.
Quặng hematite có chứa thành phần iron(III) oxide.
Đáp án B
Ở nhiệt độ thường, kim loại nào sau đây phản ứng chậm với nước?
-
A.
Mg.
-
B.
Ca .
-
C.
Sr .
-
D.
Ba.
Đáp án : A
Dựa vào tính chất hoá học của kim loại IIA.
Mg phản ứng chậm với nước ở nhiệt độ cao.
Đáp án A
Trong các mẫu nước cứng sau đây, nước cứng tạm thời là
-
A.
dung dich \({\rm{Ca}}{\left( {{\rm{HC}}{{\rm{O}}_3}} \right)_2}\).
-
B.
dung dịch \({\rm{MgS}}{{\rm{O}}_4}\).
-
C.
dung dịch \({\rm{CaC}}{{\rm{l}}_2}\).
-
D.
dung dịch \({\rm{Mg}}{\left( {{\rm{N}}{{\rm{O}}_3}} \right)_2}\).
Đáp án : A
Nước cứng tạm thời có chứa ion Ca2+, Mg2+, HCO3-
dung dich \({\rm{Ca}}{\left( {{\rm{HC}}{{\rm{O}}_3}} \right)_2}\)là mẫu nước cứng tạm thời.
đáp án A
Đặc điểm chung cấu hình electron của nguyên tử kim loại chuyển tiếp dãy thứ nhất là
-
A.
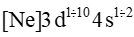
-
B.
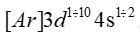
-
C.
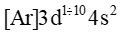
-
D.
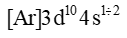
Đáp án : B
Dựa vào đặc điểm cấu hình electron của nguyên tử kim loại chuyển tiếp dãy thứ nhất.
Đặc điểm chung cấu hình electron của nguyên tử kim loại chuyển tiếp dãy thứ nhất là: 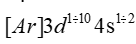
Đáp án B
Nhúng thanh kẽm vào dung dịch chất nào sau đây sẽ xảy ra hiện tượng ăn mòn điện hoá?
-
A.
KCl .
-
B.
HCl .
-
C.
\({\rm{CuS}}{{\rm{O}}_4}\).
-
D.
\({\rm{MgC}}{{\rm{l}}_2}\).
Đáp án : C
Dựa vào nguyên tắc xảy ra ăn mòn điện hoá.
Nhúng thanh kẽm vào dung dịch \({\rm{CuS}}{{\rm{O}}_4}\)sẽ xảy ra ăn mòn điện hoá.
Đáp án C
Phương pháp chung để điều chế các kim loại \({\rm{Na}},{\rm{Ca}},{\rm{Al}}\) trong công nghiệp là
-
A.
điện phân dung dịch.
-
B.
điện phân nóng chảy.
-
C.
nhiệt luyện.
-
D.
thuỷ luyện.
Đáp án : B
Các kim loại mạnh thường được điều chế bằng phương pháp điện phân nóng chảy.
Na, Ca, Al là các kim loại mạnh được điều chế bằng phương pháp điện phân nóng chảy.
Đáp án B
Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường, tạo ra dung dịch có môi trường kiềm là
-
A.
Na, Ba, K.
-
B.
\({\rm{Be}},{\rm{Na}},{\rm{Ca}}\).
-
C.
\({\rm{Na}},{\rm{Fe}},{\rm{K}}\).
-
D.
\({\rm{Na}},{\rm{Cr}},{\rm{K}}\)
Đáp án : A
Dựa vào tính chất hoá học của kim loại IA, IIA.
Na, Ba, K là các kim loại phản ứng với nước tạo dung dịch có môi trường kiềm.
Đáp án A
Trạng thái oxi hoá phổ biến của Fe và Mn tương ứng là
-
A.
\( + 2, + 3\) và \( + 2, + 4, + 7\).
-
B.
\( + 2, + 3\) và \( + 2, + 4, + 6\).
-
C.
\( + 2, + 3\) và \( + 2, + 6, + 7\).
-
D.
\( + 2, + 6\) và \( + 2, + 4, + 7\).
Đáp án : A
Dựa vào tính chất hoá học của kim loại chuyển tiếp dãy thứ nhất.
Trạng thái oxi hoá phổ biến của Fe và Mn tương ứng là: +2, +3 và +2, +4, +7.
Đáp án A
Khi đốt nóng tinh thể LiCl trong ngọn lửa đèn khí không màu thì tạo ra ngọn lửa có màu
-
A.
da cam.
-
B.
tím nhạt.
-
C.
vàng.
-
D.
đỏ tía.
Đáp án : D
Dựa vào màu ngọn lửa khi đốt cháy hợp chất IA.
LiCl cháy trong ngọn lửa đèn tạo màu đỏ tía.
Đáp án D
Hợp chất nào sau đây vừa tác dụng được với dung dịch HCl , vừa tác dụng được với dung dịch NaOH ?
-
A.
\({\rm{NaHC}}{{\rm{O}}_3}\).
-
B.
NaCl .
-
C.
\({\rm{Ba}}{({\rm{OH}})_2}\).
-
D.
\({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\).
Đáp án : A
Các hợp chất lưỡng tính vừa tác dụng với dung dịch HCl vừa tác dụng với dung dịch NaOH.
\({\rm{NaHC}}{{\rm{O}}_3}\) vừa tác dụng với HCl vừa tác dụng với NaOH.
Đáp án A
Khi đốt cháy kim loại Na trong bình chứa khí oxygen tạo thành sản phẩm là
-
A.
NaO .
-
B.
\({\rm{N}}{{\rm{a}}_2}{{\rm{O}}_2}\).
-
C.
\({\rm{N}}{{\rm{a}}_2}{\rm{O}}\).
-
D.
\({\rm{Na}}{{\rm{O}}_2}\).
Đáp án : B
Dựa vào tính chất hoá học của kim loại IA.
Khi đốt cháy kim loại Na trong bình giàu khí oxygen sẽ tạo thành sản phẩm peoxide Na2O2.
Đáp án B
Ở nơi tồn ứ rác thải, chất nào sau đây được các công nhân vệ sinh môi trường dùng để xử lí tạm thời nhằm sát trùng, diệt khuẩn, phòng chống dịch bệnh?
-
A.
Cát vàng.
-
B.
Than đá.
-
C.
Đá vôi.
-
D.
Vôi bột.
Đáp án : D
Dựa vào tính chất hoá học của hợp chất nhóm IIA.
Vôi bột có khả năng sát trùng, diệt khuẩn, phòng chống dịch bệnh
Đáp án D
Nước cứng gây nhiều tác hại trong đời sống và sản xuất như đóng cặn đường ống dẫn nước, làm cho xà phòng có ít bọt khi giặt quần áo, làm giảm mùi vị thực phẩm khi nấu ăn. Nước cứng là nước có chứa nhiều các ion
-
A.
\({\rm{M}}{{\rm{g}}^{2 + }}\) và \({\rm{C}}{{\rm{a}}^{2 + }}\).
-
B.
\({\rm{N}}{{\rm{a}}^ + }\)và \({{\rm{K}}^ + }\).
-
C.
\({{\rm{F}}^ - }\)và \({\rm{C}}{{\rm{l}}^ - }\).
-
D.
\({\rm{SO}}_4^{2 - }\) và \({\rm{CO}}_3^{2 - }\).
Đáp án : A
Dựa vào khái niệm của nước cứng.
Nước cứng là nước chứa nhiều các ion \({\rm{M}}{{\rm{g}}^{2 + }}\) và \({\rm{C}}{{\rm{a}}^{2 + }}\).
Tiến hành các thí nghiệm sau:
(1) Sục khí \({\rm{C}}{{\rm{O}}_2}\) dư vào dung dịch \({\rm{Ca}}{({\rm{OH}})_2}\).
(2) Cho dung dịch NaOH dư vào dung dịch \({\rm{Ba}}{\left( {{\rm{HC}}{{\rm{O}}_3}} \right)_2}\).
(3) Đun sôi một mẫu nước có tính cứng tạm thời.
(4) Cho dung dịch \({\rm{KHS}}{{\rm{O}}_4}\) vào dung dịch \({\rm{Ba}}{({\rm{OH}})_2}\).
Khi kết thúc phản ứng, số thí nghiệm thu được kết tủa là
-
A.
1
-
B.
3
-
C.
2
-
D.
4
Đáp án : B
Dựa vào tính chất hoá học của hợp chất nhóm IIA.
(1) không có kết tủa
(2) có kết tủa BaCO3.
(3) có kế tủa MgCO3 và CaCO3.
(4) Có kết tủa BaSO4.
Đáp án B
"Thép 304 " là một loại thép không gỉ được dùng phổ biến trong đời sống. Các kim loại chủ yếu tạo nên loại thép này bao gồm:
-
A.
Fe, C,Cr.
-
B.
Fe,Cu, Cr.
-
C.
Fe,Cr, Ni.
-
D.
Fe,C, Cr, Ni.
Đáp án : D
Dựa vào thành phần của hợp kim.
Thép 304 là loại thép không gỉ, gồm các kim loại chủ yếu Fe, C, Cr, Ni.
Đáp án D
Trong ion phức chất [Co(NH3)6]3+, nguyên tử trung tâm là
-
A.
Co3+.
-
B.
N.
-
C.
H.
-
D.
NH3.
Đáp án : A
Dựa vào khái niệm về phức chất.
Nguyên tử trung tâm là Co3+.
Đáp án A
Các phương pháp để điều chế kim loại như sau:
a. Các kim loại đều có thể điều chế bằng phương pháp dùng CO khử oxide kim loại tương ứng.
b. Trong công nghiệp, kim loại Al chỉ có thể điều chế được bằng phương pháp điện phân.
c. Để tách Ag khỏi các tạp chất \({\rm{Fe}},{\rm{Cu}}\) ta có thể cho hỗn hợp vào dung dịch \({\rm{AgN}}{{\rm{O}}_3}\) dư.
d. Trong công nghiệp, kim loại Na được điều chế bằng cách điện phân dung dịch NaCl .
a. Các kim loại đều có thể điều chế bằng phương pháp dùng CO khử oxide kim loại tương ứng.
b. Trong công nghiệp, kim loại Al chỉ có thể điều chế được bằng phương pháp điện phân.
c. Để tách Ag khỏi các tạp chất \({\rm{Fe}},{\rm{Cu}}\) ta có thể cho hỗn hợp vào dung dịch \({\rm{AgN}}{{\rm{O}}_3}\) dư.
d. Trong công nghiệp, kim loại Na được điều chế bằng cách điện phân dung dịch NaCl .
Các kim loại có mức độ hoạt động khác nhau sẽ có phương pháp điều chế khác nhau.
a) sai, Al không được điều chế bằng phương pháp nhiệt luyện.
b) đúng
c) đúng
d) sai, Na được điều chế bằng phương pháp điện phân nóng chảy.
Tiến hành thí nghiệm kim loại tác dụng với dung dịch muối:
Chuẩn bị:
- Hoá chất: Đinh sắt đã được đánh sạch bề mặt, dung dịch copper (II) sulfate 1M.
- Dụng cụ: Cốc thủy tinh.
Tiến hành: Cho đinh sắt vào cốc thủy tinh chứa dung dịch copper (II) sulfate 1M.
a. Thấy có bọt khí thoát ra.
b. Thấy xuất hiện kết tủa màu xanh.
c. Thấy có lớp kim loại đồng bám vào đinh sắt, dung dịch nhạt màu dần.
d. Thanh sắt tan dần, có lớp kim loại đồng bám vào, dung dịch nhạt màu dần.
a. Thấy có bọt khí thoát ra.
b. Thấy xuất hiện kết tủa màu xanh.
c. Thấy có lớp kim loại đồng bám vào đinh sắt, dung dịch nhạt màu dần.
d. Thanh sắt tan dần, có lớp kim loại đồng bám vào, dung dịch nhạt màu dần.
Dựa vào tính chất hoá học của kim loại.
a. sai, không có bọt khí thoát ra.
b. sai, kết tủa đỏ.
c. sai, thiếu hiện tượng sắt tan dần.
d. đúng.
Những phát biểu khi nói về khả năng phản ứng của kim loại với sulfuric acid?
a. Chỉ các kim loại đứng trước H mới tham gia phản ứng với H2SO4 loãng.
b. Các kim loại sắt, nhôm, chromium phản ứng được với dung dịch sulfuric acid đặc ở nhiệt độ cao, không phản ứng với dung dịch sulfuric acid đặc, nguội do sulfuric acid đặc nguội đã oxi hóa bề mặt kim loại tạo thành màng oxide có tính trơ, làm cho các kim loại này bị thụ động.
c. Hiện tượng các kim loại sắt, nhôm, chromium không phản ứng với dung dịch sulfuric acid đặc, nguội được gọi là hiện tượng thụ động hóa, tương tự đối với nitric acid.
d. Có thể dùng dung dịch sulfuric acid loãng để phân biệt đoạn dây bạc và đoạn dây platium.
a. Chỉ các kim loại đứng trước H mới tham gia phản ứng với H2SO4 loãng.
b. Các kim loại sắt, nhôm, chromium phản ứng được với dung dịch sulfuric acid đặc ở nhiệt độ cao, không phản ứng với dung dịch sulfuric acid đặc, nguội do sulfuric acid đặc nguội đã oxi hóa bề mặt kim loại tạo thành màng oxide có tính trơ, làm cho các kim loại này bị thụ động.
c. Hiện tượng các kim loại sắt, nhôm, chromium không phản ứng với dung dịch sulfuric acid đặc, nguội được gọi là hiện tượng thụ động hóa, tương tự đối với nitric acid.
d. Có thể dùng dung dịch sulfuric acid loãng để phân biệt đoạn dây bạc và đoạn dây platium.
Dựa vào tính chất hoá học của kim loại tác dụng với acid.
a. đúng
b. đúng
c. đúng
d. sai, vì Ag và Pt đều không phản ứng với H2SO4 loãng
Có nhiều phương pháp để chống ăn mòn kim loại.
a) Phương pháp phủ sơn là một trong những cách phổ biến để bảo vệ kim loại.
b) Gắn tấm kẽm vào vỏ tàu biển giúp bảo vệ kim loại bằng cách tạo ra điện hóa.
c) Sử dụng thép không gỉ là phương pháp hiệu quả nhất trong mọi trường hợp để ngăn ngừa ăn mòn.
d) Giảm độ ẩm môi trường xung quanh có thể hạn chế ăn mòn kim loại.
a) Phương pháp phủ sơn là một trong những cách phổ biến để bảo vệ kim loại.
b) Gắn tấm kẽm vào vỏ tàu biển giúp bảo vệ kim loại bằng cách tạo ra điện hóa.
c) Sử dụng thép không gỉ là phương pháp hiệu quả nhất trong mọi trường hợp để ngăn ngừa ăn mòn.
d) Giảm độ ẩm môi trường xung quanh có thể hạn chế ăn mòn kim loại.
Dựa vào các phương pháp chống ăn mòn kim loại.
a. đúng
b. đúng
c. sai, chỉ dùng thép không gỉ để bảo vệ các kim loại yếu hơn Fe.
d. đúng
Cho dãy các kim loại: Na, Cu, Fe, Ag, Zn. Số kim loại trong dãy phản ứng được với dung dịch HCl là ?
Dựa vào tính chất hoá học của kim loại.
Các kim loại Na, Fe, Zn tác dụng với HCl.
Đáp án 3
Dựa vào liên kết trong phức chất.
Liên kết giữa nguyên tử trung tâm và phối tử là liên kết cho – nhận.
Liên kết N – H, O – H trong phối tử là liên kết cho nhận nên có 7 liên kết cộng hoá trị.
Cho phương trình hóa học của phản ứng sau:
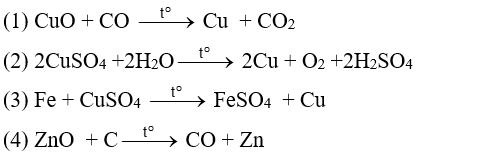
Liệt kê số phản ứng có thể được dùng để điều chế kim loại bằng phương pháp nhiệt luyện theo thứ tự giảm dần.
Phương pháp nhiệt luyện là phương pháp khử oxide kim loại trung bình yếu bằng chất khử.
14 là 2 phản ứng điều chế kim loại bằng phương pháp nhiệt luyện.
Thí nghiệm về sự tạo thành phức chất của Cu2+
Bước 1: Cho khoảng 1 mL dung dịch CuSO4 5% vào ống nghiệm (1). Cho tiếp 3 giọt dung dịch NaOH 10% vào ống nghiệm, lắc đều.
Bước 2: Nhỏ từ từ dung dịch NH3 10% vào ống nghiệm (1), vừa nhỏ vừa lắc đều đến khi kết tủa tan hoàn toàn.
Bước 3: Cho khoảng 1 mL dung dịch CuSO4 5% vào ống nghiệm (2). Nhỏ từ từ dung dịch HCl đặc vào ống nghiệm, vừa nhỏ vừa lắc đều đến khi dung dịch chuyển màu hoàn toàn.
Hiện tượng và viết phương trình hoá học của các phản ứng xảy ra như sau:
(1) Sau bước 1: Ống nghiệm (1) ban đầu xuất hiện kết tủa xanh.
(2) Sau bước 2: Khi cho từ từ dung dịch NH3 vào thì kết tủa xanh tan dần do tạo thành phức chất có màu xanh lam.
(3) Sau bước 2: Phương trình tạo thành phức chất có màu xanh lam là
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2.
(4) Sau bước 3: Ống nghiệm (2) Dung dịch chuyển từ màu xanh sang xanh lá, cuối cùng là màu vàng.
(5) Sau bước 3: Phương trình tạo thành phức chất có màu xanh lam là
CuSO4 + 4HCl → H2[CuCl4] + H2SO4
Có bao nhiêu phát biểu đúng?
Dựa vào các phản ứng xảy ra trong phức chất.
(1) đúng vì tạo ra kết tủa Cu(OH)2
(2) đúng, xảy ra phản ứng thay thế phối tử aqua bằng NH3.
(3) đúng
(4) đúng
(5) đúng
Đáp án 5
Vàng (Au) đơn chất tồn tại trong tự nhiên ở trong quặng vàng thường có hàm lượng vàng thấp. Để thu hồi vàng từ quặng vàng, người ta nghiền quặng, hoà tan chúng vào dung dịch KCN và liên tục sục không khí vào. Vàng bị hoà tan tạo thành phức chất:
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l)→ 4K[Au(CN)2](aq) + 4KOH(aq) (1)
và sau đó kết tủa vàng bằng kẽm (Zn):
Zn(s) + 2K[Au(CN)2] (aq) → K2[Zn(CN)4](aq) + 2Au(s) (2)
Nếu dùng 13 kg KCN thì có thể tách được bao nhiêu kg vàng từ quặng theo chuỗi phản ứng trên? Giả thiết các chất khác trong quặng không phản ứng với KCN.
Tính số mol KCN và dựa vào phương trình để tính số mol Au.
n KCN = 0,2 k.mol
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l)→ 4K[Au(CN)2](aq) + 4KOH(aq) (1)
0,2 → 0,1
Zn(s) + 2K[Au(CN)2] (aq) → K2[Zn(CN)4](aq) + 2Au(s) (2)
0,1 → 0,1
m Au = 0,1.197 = 19,7kg
Một viên thực phẩm chức năng có khối lượng 250 mg chứa nguyên tố sắt (iron) ở dạng muối Fe(II) cùng một số chất khác. Kết quả kiểm nghiệm thấy lượng Fe(II) trong viên này phản ứng vừa đủ với 8,5 mL dung dịch KMnO4 0,04M. Phần trăm khối lượng của nguyên tố sắt trong viên thực phẩm chức năng trên là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
Tính khối lượng Fe có trong viên thực phẩm. Dựa vào phản ứng chuẩn độ Fe2+ bằng KMnO4.
n KMnO4 = 8,5.0,04 = 0,34 mmol
\(\begin{array}{l}F{e^{2 + }} \to F{e^{3 + }} + 1{\rm{e}}\\M{n^{ + 7}} + 5{\rm{e}} \to M{n^{ + 2}}\end{array}\)
Bảo toản electron ta có: n Fe2+ = 5. n Mn+7 = 0,34.5 = 1,7 mmol
%Fe = \(\frac{{1,7.56}}{{250}}.100 = 38,08\% \approx 38,1\% \)
Trong mạng tinh thể kim loại, liên kết kim loại được hình thành do
Cho phát biểu sau: “Phức chất đơn giản thường có một ...(1)...
Các rạn san hô và đá vôi có thành phần chính là:
Hợp chất Kn[Fe(CN)6], trong đó Fe có số oxi hóa +3. Giá trị của n bằng










Danh sách bình luận