Đề thi học kì 2 Hóa 12 Kết nối tri thức - Đề số 4
Các rạn san hô và đá vôi có thành phần chính là:
Đề bài
Các rạn san hô và đá vôi có thành phần chính là:
-
A.
BaCO3
-
B.
CaCO3
-
C.
MgCO3
-
D.
K2CO3
Thực nghiệm xác định phức chất [Co(NH3)6]3+ có dạng hình học tứ diện. Mô tả nào sau đây không đúng ?
-
A.
điện tích của phức chất là +3.
-
B.
phức chất trên có 6 phối tử.
-
C.
nguyên tử trung tâm của phức chất là Co.
-
D.
điện tích của phức chất là 3+.
Trong y học, hợp chất được sử dụng để điều trị triệu chứng dư acid ở dạ dày là
-
A.
NaOH.
-
B.
Na2CO3.
-
C.
NaHCO3.
-
D.
K2SO4.
Nguyên tố kim loại nhóm IA có cấu hình e lớp ngoài cùng là
-
A.
ns1.
-
B.
ns2.
-
C.
ns2np1.
-
D.
1s1.
Kim loại không phản ứng với nước ở điều kiện thường là
-
A.
K.
-
B.
Ba.
-
C.
Cu.
-
D.
Ca.
Một mẫu nước giếng có chứa các ion: Ca2+; Cl-; NO3-; Mg2+; Na+. Cho dung dịch soda vào mẫu nước giếng trên, sau phản ứng thu được số chất kết tủa là
-
A.
2
-
B.
3
-
C.
1
-
D.
4
Để nhận biết sự có mặt có ion Ba2+ có trong dung dịch ta dùng dung dịch
-
A.
HCl.
-
B.
H2SO4.
-
C.
NaNO3.
-
D.
KCl.
Thạch cao, vôi tôi, vôi sống, đá vôi, apatite…là các nguyên liệu có thành phần chính là các hợp chất của nguyên tố
-
A.
Na.
-
B.
K.
-
C.
Ba.
-
D.
Ca.
Phát biểu nào sau đây đúng khi nói về kim loại chuyển tiếp dãy thứ nhất?
-
A.
Các kim loại thường có số oxi hoá là +1.
-
B.
Thường có khối lượng riêng lớn, cứng và khó nóng chảy.
-
C.
Đồng (copper) có tính dẫn điện kém hơn sắt.
-
D.
Các nguyên tố chuyển tiếp dãy thứ nhất đều thuộc nhóm IA và IIA.
Liên kết giữa phối tử và nguyên tử trung tâm trong phức chất là loại liên kết
-
A.
ion.
-
B.
cộng hoá trị do góp chung các cặp e.
-
C.
cả ion và cộng hoá trị.
-
D.
cho - nhận.
Thí nghiệm nào sau đây kết thúc phản ứng thu được kết tủa?
-
A.
Cho từ từ đến dư dung dịch NH3 vào dung dịch CuSO4, lắc đều.
-
B.
Sục từ từ đến dư khí CO2 vào dung dịch Ca(OH)2.
-
C.
Cho từ từ đến dư dung dịch CaCl2 vào dung dịch NaHCO3.
-
D.
Cho từ từ đến dư dung dịch AgNO3 vào dung dịch Fe(NO3)2.
Phát biểu nào sau đây sai?
-
A.
Các kim loại chuyển tiếp dãy thứ nhất đều có nhiệt độ nóng chảy cao dẫn điện tốt, dẫn nhiệt tốt, khối lượng riêng lớn và được ứng dụng rộng rãi trong thực tiễn
-
B.
Các kim loại chuyển tiếp dãy thứ nhất có xu hướng thể hiện nhiều trạng thái oxi hoá và tạo ra các hợp chất có màu sắc phong phú.
-
C.
Cấu hình electron của nguyên tử kim loại chuyển tiếp dãy thứ nhất đều có phân lớp 4s đã bão hoà.
-
D.
Phức chất [Co(NH3)6]3+ có nguyên tử trung tâm là Co3+ và phối tử là NH3
A, B, C là 3 muối chloride của kim loại kiềm. Để xác định A, B, C người ta tiến hành thí nghiệm như sau.
Bước 1: Nhúng dây platinum vào ống nghiệm chứa dung dịch bão hòa A.
Bước 2: Hơ nóng đầu dây trên ngọn lửa đèn khí Bunsen (khí gas).
Tiến hành thí nghiệm tương tự với dung dịch bão hoà B, C.
Màu ngọn lửa được ghi lại ở bảng sau:
|
Mẫu thử |
A |
B |
C |
|
Màu ngọn lửa |
đỏ tía |
tím nhạt |
vàng |
Cho các phát biểu sau:
(1) Ở bước 1 phải làm sạch dây kim loại giữa những lần thí nghiệm.
(2) Dung dịch ở bước 1 lẫn bất kỳ tạp chất chứa ion kim loại khác lẫn vào sẽ không ảnh hưởng đến kết quả của thí nghiệm.
(3) Có thể phân biệt các kim loại kiềm do khi đốt hợp chất của kim loại kiềm trên ngọn lửa không màu làm ngọn lửa có màu đặc trưng.
(4) A là KCl, B là NaCl, C là LiCl.
Số nhận định đúng là
-
A.
1
-
B.
2
-
C.
4
-
D.
3
Để xác định hàm lượng FeCO3 trong quặng Siderirte, người ta làm như sau: cân 0,6g mẫu quặng, chế hóa nó theo một quy trình hợp lí, thu được FeSO4 trong môi trường H2SO4 loãng. Chuẩn độ dung dịch thu được bằng dung dịch chuẩn KMnO4 0,025M thì dùng vừa hết 25,2ml. % theo khối lượng của FeCO3 là:
-
A.
12,18%
-
B.
24,26%
-
C.
60,9%
-
D.
30,45%
Cho các phát biểu sau:
(a) Nước chứa nhiều cation Ca2+ và Mg2+ là nước cứng.
(b) Nước cứng chia làm 3 loại: nước có tính cứng tạm thời, nước có tính cứng vĩnh cửu và nước có tính cứng toàn phần.
(c) Nước cứng gây nhiều tác hại cho sản xuất và đời sống.
(d) Hai phương pháp làm mềm nước cứng phổ biến là phương pháp kết tủa và phương pháp trao đổi ion.
(e) Phương pháp trao đổi ion làm giảm được cả tính cứng tạm thời và tính cứng vĩnh cửu.
Số phát biểu đúng là
-
A.
3
-
B.
2
-
C.
5
-
D.
4
Tiến hành thí nghiệm điều chế kim loại bằng cách dùng kim loại mạnh khử ion của kim loại yếu trong dung dịch theo các bước sau đây:
Bước 1: Đánh sạch gỉ một chiếc đinh sắt (iron) rồi thả vào dung dịch CuSO4.
Bước 2: Sau khoảng 10 phút, quan sát màu của chiếc đinh sắt (iron) và màu của dung dịch.
Phát biểu nào sau đây sai?
-
A.
Đinh sắt bị phủ một lớp màu đỏ.
-
B.
Màu xanh của dung dịch không đổi vì đó là màu của ion sulfate
-
C.
Màu xanh của dung dịch bị nhạt dần vì nồng độ ion Cu2+ giảm dần trong quá trình phản ứng.
-
D.
Màu đỏ trên đinh sắt (iron) là do copper sinh ra bám vào.
Theo TCVN 5502 : 2003, các mẫu nước có tổng nồng độ Ca2+ và Mg2+ lớn hơn 5.10-4 M là nước cứng. Cho dung dịch có nồng độ các ion như sau: Na+ (0,005 M), Ca2+ (0,001 M); Mg2+ (0,0005 M); Cl- (0,002 M, HCO3- (0,0035 M); SO42- (0,00125 M). Mẫu nước trên thuộc loại
-
A.
nước mềm.
-
B.
nước cứng tạm thời.
-
C.
nước cứng toàn phần.
-
D.
nước cứng vĩnh cửu.
Đơn chất, hợp chất kim loại nhóm IA không có tính chất nào sau đây:
-
A.
Là các kim loại mềm, nhẹ, có nhiệt độ nóng chảy và nhiệt độ sôi tăng từ lithium đến caesium.
-
B.
Có tính khử mạnh, tính khử tăng từ lithium đến caesium.
-
C.
Được bảo quản bằng cách ngâm trong dầu hoả khan hoặc bình khí hiếm.
-
D.
Có thể phân biệt nhờ màu ngọn lửa đặc trưng khi đốt chúng trên ngọn lửa đèn khí.
Thực hiện thí nghiệm như sau:
- Cho 2 mL dung dịch FeCl3 1M vào ống nghiệm (1) và 2 mL dung dịch CuSO4 1M vào ống nghiệm (2)
- Thêm tiếp vào mỗi ống nghiệm 2 – 3 giọt dung dịch NaOH 1M, lắc nhẹ.
a) Ống nghiệm (1) có kết tủa màu xanh lam, ống nghiệm (2) có kết tủa màu vàng.
b) Phản ứng xảy ra trong ống nghiệm (1) có phương trình ion thu gọn là: Fe3+ + 3OH- → Fe(OH)3.
c) Nếu cho NaOH dư vào cả hai ống nghiệm thì ống nghiệm (1) không thu được kết tủa, ống nghiệm (2) vẫn thu được kết tủa.
d) Nếu thay dung dịch NaOH bằng dung dịch Ba(OH)2 thì số chất kết tủa thu được vẫn không thay đổi.
Tiến hành thí nghiệm xác định hàm lượng iron (II) sulfate bằng phương pháp chuẩn độ thuốc tím trong môi trường sulfuric acid dư.
- Dùng pipette lấy 5,0 mL dung dịch FeSO4 cho vào bình tam giác; thêm tiếp khoảng 5 mL dung dịch H2SO4 10% (lấy bằng ống đong).
- Cho dung dịch KMnO4 vào burette, điều chỉnh thể tích dung dịch trong burette về mức 0.
- Mở khoá burette, nhỏ từng giọt dung dịch KMnO4 xuống bình tam giác, lắc đều.
a. Ban đầu dung dịch trong bình tam giác xuất hiện màu hồng rồi mất màu nhanh.
b. Cần sử dụng chất chỉ thị để nhận biết điểm kết thúc chuẩn độ.
c. Iron (II) sulfate là chất khử, thuốc tím là chất oxi hoá.
d. Chuẩn độ đến khi màu hồng tồn tại bền trong khoảng 20 giây thì dừng chuẩn độ.
Cắt mẫu sodium bằng hạt đậu xanh, làm sạch lớp dầu bằng giấy thấm dầu. Dùng kẹp gắp mẩu sodium cho vào cốc nước có nhỏ vài giọt phenolphthalein.
a) Mẫu Na phản ứng chạy trên mặt nước.
b) Phản ứng giải phóng khí hydrogen.
c) Cốc nước hoá hồng.
d) Phản ứng với nước thu nhiệt.
Y là hợp chất của calcium có nhiều ở dạng đá vôi, đá hoa,…Hợp chất Z có trong thành phần của không khí và thường dùng để chữa cháy, Biết rằng, Z được sinh ra khi cho Y phản ứng với dung dịch acid mạnh.
a) Chất Y và Z lần lượt là CaCO3 và N2.
b) Chất Y được sinh ra khi sục chất Z dư vào dung dịch Ca(OH)2.
c) Chất Y và Z đóng vai trò hình thành thạch nhũ trong hang động đá vôi.
d) Chất Y là nguyên liệu sản xuất NaHCO3 và Na2CO3 theo phương pháp Solvay.
Sodium carbonate (Na2CO3) là chất thường dùng để làm mềm nước cứng theo phương pháp kết tủa. Độ cứng của nước có thể tính theo số mg CaCO3 trong 1 lít nước, trong đó độ cứng không vượt quá 60mg.L-1 là nước mềm. Để xử lí một mẫu nước cứng vĩnh cửu có độ cứng a (mg CaCO3/L) người ta cho 1 lít dung dịch Na2CO3 0,020M vào 19 lít mẫu nước cứng, lắc đều, thu được kết tủa CaCO3 và nước mềm Y. Nồng độ Ca2+ và CO32- có trong mẫu nước mềm Y lần lượt là 5,00.10-4M và 8,93.10-6M. Giả thiết rằng, mẫu nước cứng chứa Ca2+ và các ion khác, các ion khác này không tham gia phản ứng, ion CO32- và ion Ca2+ không bị thuỷ phân trong nước. Tính giá trị của a (làm tròn đến hàng đơn vị).
Calcium oxide (CaO) còn được gọi là vôi sống, phần lớn được dùng làm vật liệu xây dựng. Ngoài ra, nó còn được dùng để làm chất hút ẩm trong công nghiệp, khử chua, tẩy uế….Có thể sản xuất vôi sống bằng cách nung đá vôi CaCO3 trong lò nung theo phương trình hoá học (1) như sau:
Phản ứng (1) là phản ứng thu nhiệt. Lượng nhiệt này được cung cấp từ quá trình đốt cháy hoàn toàn carbon trong lò nung theo phương trình hoá học (2):
C (graphite) + O2(g) → CO2(g) (2)
Xét các phản ứng ở điều kiện chuẩn, hiệu suất chuyển hoá calcium carbonate thành calcium oxide là 100%. Tính khối lượng calcium oxide sản xuất được (theo tấn, làm tròn đến hàng đơn vị) trong các quá trình trên khi đốt cháy hoàn toàn 28,8 tấn carbon (graphite). Biết có 90% nhiệt lượng toả ra từ phản ứng (2) được cung cấp cho phản ứng (1) và các giá trị nhiệt tạo thành (\({\Delta _f}H_{298}^o\)) ở các chất ở điều kiện chuẩn được cho trong bảng sau:
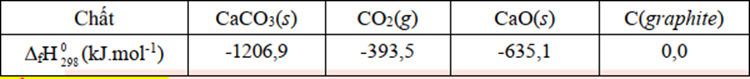
Tiến hành thí nghiệm xác định thành phần một chiếc đinh sắt (đã bị oxi hoá một phần thành gỉ sắt, Fe2O3.xH2O) theo các bước sau.
- Bước 1: Hoà tan toàn bộ đinh sắt trong dung dịch H2SO4 loãng (dùng gấp đôi lượng phản ứng, giả thiết Fe chỉ phản ứng với acid), thu được 250 mL dung dịch X.
- Bước 2: Nhỏ dung dịch BaCl2 dư vào cốc chứa 10,0 mL dung dịch X, thu được 0,8202 gam kết tủa trắng.
- Bước 3: Tiến hành chuẩn độ 10,0 mL dung dịch X bằng dung dịch KMnO4 0,02 M cần vừa đủ 12,80 mL.
Khối lượng của Fe2O3 ở đinh sắt ban đầu là bao nhiêu gam? (Làm tròn kết quả đến hàng phần mười)
Có bao nhiêu chất bị phân huỷ bởi nhiệt độ trong dãy các chất sau: Na2CO3, BaCO3, CaSO4, Ca(HCO3)2, Mg(NO3)2, NaHCO3.
Khi nói về hiện tượng gỉ (rỉ) sắt khi để gang, thép để trong không khí ẩm, một học sinh đã có phát biểu sau:
(1) Hiện tượng trên xảy ra chủ yếu do gang thép bị ăn mòn ăn mòn điện hóa.
(2) Khi bị ăn mòn điện hóa, nguyên tử Fe trong gang, thép đóng vai trò anode.
(3) Nguyên tử Fe đã bị khử thành cation Fe2+ theo quá trình Fe → Fe2+ + 2e.
(4) Nếu để gang thép trong không khí khô thì tốc độ rỉ sắt chậm hơn so với không khí ẩm
Liệt kê các phát biểu đúng theo thứ tự tăng dần.
Muối Nigari (MgCl2.6H2O) làm đông tụ nhanh sữa đậu nành thành đậu hũ. Làm lạnh 805 gam dung dịch bão hoà MgCl2 ở 60 °C xuống 10 °C thì có m gam tinh thể MgCl2.6H2O tách ra khỏi dung dịch bão hoà. Biết độ tan của MgCl2 trong nước ở 10 °C và 60 °C lần lượt là 52,9 gam là 61,0 gam. Tính giá trị của m.
Lời giải và đáp án
Các rạn san hô và đá vôi có thành phần chính là:
-
A.
BaCO3
-
B.
CaCO3
-
C.
MgCO3
-
D.
K2CO3
Đáp án : B
Dựa vào trạng thái tự nhiên của kim loại IIA.
Các rạn san hô và đá vôi có thành phần chính là CaCO3.
Đáp án B
Thực nghiệm xác định phức chất [Co(NH3)6]3+ có dạng hình học tứ diện. Mô tả nào sau đây không đúng ?
-
A.
điện tích của phức chất là +3.
-
B.
phức chất trên có 6 phối tử.
-
C.
nguyên tử trung tâm của phức chất là Co.
-
D.
điện tích của phức chất là 3+.
Đáp án : D
Dựa vào công thức của phức chất đã cho.
D sai vì điện tích được viết dấu trước số sau.
Đáp án D
Trong y học, hợp chất được sử dụng để điều trị triệu chứng dư acid ở dạ dày là
-
A.
NaOH.
-
B.
Na2CO3.
-
C.
NaHCO3.
-
D.
K2SO4.
Đáp án : C
Dựa vào ứng dụng của hợp chất nhóm IA.
Baking soda được sử dụng làm giảm chứng dư acid ở dạ dày: NaHCO3.
Đáp án C
Nguyên tố kim loại nhóm IA có cấu hình e lớp ngoài cùng là
-
A.
ns1.
-
B.
ns2.
-
C.
ns2np1.
-
D.
1s1.
Đáp án : A
Dựa vào đặc điểm cấu hình của nguyên tố kim loại nhóm IA.
Cấu hình electron lớp ngoài cùng của kim loại nhóm IA là: ns1.
Đáp án A
Kim loại không phản ứng với nước ở điều kiện thường là
-
A.
K.
-
B.
Ba.
-
C.
Cu.
-
D.
Ca.
Đáp án : C
ựa vào tính chất hoá học của kim loại IA.
Cu không phản ứng với nước ở điều kiện thường.
Đáp án C
Một mẫu nước giếng có chứa các ion: Ca2+; Cl-; NO3-; Mg2+; Na+. Cho dung dịch soda vào mẫu nước giếng trên, sau phản ứng thu được số chất kết tủa là
-
A.
2
-
B.
3
-
C.
1
-
D.
4
Đáp án : A
Soda có công thức Na2CO3 có thể dùng để làm mềm nước cứng.
Có 2 kết tủa thu được là CaCO3 và MgCO3.
Đáp án A
Để nhận biết sự có mặt có ion Ba2+ có trong dung dịch ta dùng dung dịch
-
A.
HCl.
-
B.
H2SO4.
-
C.
NaNO3.
-
D.
KCl.
Đáp án : B
Ba2+ có kết tủa với gốc SO42-.
Dùng H2SO4 để nhận biết sự có mặt của ion Ba2+.
Đáp án B
Thạch cao, vôi tôi, vôi sống, đá vôi, apatite…là các nguyên liệu có thành phần chính là các hợp chất của nguyên tố
-
A.
Na.
-
B.
K.
-
C.
Ba.
-
D.
Ca.
Đáp án : D
Dựa vào trạng thái tự nhiên của nhóm IIA.
Thạch cao, vôi sống, vôi tôi,… có thành phần chính là các hợp chất của nguyên tố calcium.
Đáp án D
Phát biểu nào sau đây đúng khi nói về kim loại chuyển tiếp dãy thứ nhất?
-
A.
Các kim loại thường có số oxi hoá là +1.
-
B.
Thường có khối lượng riêng lớn, cứng và khó nóng chảy.
-
C.
Đồng (copper) có tính dẫn điện kém hơn sắt.
-
D.
Các nguyên tố chuyển tiếp dãy thứ nhất đều thuộc nhóm IA và IIA.
Đáp án : B
Dựa vào tính chất của kim loại IA, IIA.
A sai, kim loại chuyển tiếp dãy thứ nhất có nhiều số oxi hoá.
B đúng
C. sai, đồng có tính dẫn điện tốt hơn sắt.
D. sai, các nguyên tố chuyển tiếp dãy thứ nhất thuộc nhóm B.
Đáp án B
Liên kết giữa phối tử và nguyên tử trung tâm trong phức chất là loại liên kết
-
A.
ion.
-
B.
cộng hoá trị do góp chung các cặp e.
-
C.
cả ion và cộng hoá trị.
-
D.
cho - nhận.
Đáp án : D
Dựa vào liên kết trong phức chất.
Liên kết giữa phối tử và nguyên tử trung tâm trong phức chất là loại liên kết cho – nhận.
Đáp án D
Thí nghiệm nào sau đây kết thúc phản ứng thu được kết tủa?
-
A.
Cho từ từ đến dư dung dịch NH3 vào dung dịch CuSO4, lắc đều.
-
B.
Sục từ từ đến dư khí CO2 vào dung dịch Ca(OH)2.
-
C.
Cho từ từ đến dư dung dịch CaCl2 vào dung dịch NaHCO3.
-
D.
Cho từ từ đến dư dung dịch AgNO3 vào dung dịch Fe(NO3)2.
Đáp án : D
Dựa vào tính chất hoá học của kim loại chuyển tiếp.
Khi cho từ từ đến dư dung dịch AgNO3 vào dung dịch Fe(NO3)2 thu được kết tủa Ag.
AgNO3 + Fe(NO3)2 → Fe(NO3)3 + Ag.
Đáp án D
Phát biểu nào sau đây sai?
-
A.
Các kim loại chuyển tiếp dãy thứ nhất đều có nhiệt độ nóng chảy cao dẫn điện tốt, dẫn nhiệt tốt, khối lượng riêng lớn và được ứng dụng rộng rãi trong thực tiễn
-
B.
Các kim loại chuyển tiếp dãy thứ nhất có xu hướng thể hiện nhiều trạng thái oxi hoá và tạo ra các hợp chất có màu sắc phong phú.
-
C.
Cấu hình electron của nguyên tử kim loại chuyển tiếp dãy thứ nhất đều có phân lớp 4s đã bão hoà.
-
D.
Phức chất [Co(NH3)6]3+ có nguyên tử trung tâm là Co3+ và phối tử là NH3
Đáp án : C
Dựa vào tính chất vật lí của kim loại chuyển tiếp dãy thứ nhất.
C sai, cấu hình electrong nguyên tử kim loại chuyển tiếp có nguyên tố có phân lớp 4s1 chưa bão hoà.
Đáp án C
A, B, C là 3 muối chloride của kim loại kiềm. Để xác định A, B, C người ta tiến hành thí nghiệm như sau.
Bước 1: Nhúng dây platinum vào ống nghiệm chứa dung dịch bão hòa A.
Bước 2: Hơ nóng đầu dây trên ngọn lửa đèn khí Bunsen (khí gas).
Tiến hành thí nghiệm tương tự với dung dịch bão hoà B, C.
Màu ngọn lửa được ghi lại ở bảng sau:
|
Mẫu thử |
A |
B |
C |
|
Màu ngọn lửa |
đỏ tía |
tím nhạt |
vàng |
Cho các phát biểu sau:
(1) Ở bước 1 phải làm sạch dây kim loại giữa những lần thí nghiệm.
(2) Dung dịch ở bước 1 lẫn bất kỳ tạp chất chứa ion kim loại khác lẫn vào sẽ không ảnh hưởng đến kết quả của thí nghiệm.
(3) Có thể phân biệt các kim loại kiềm do khi đốt hợp chất của kim loại kiềm trên ngọn lửa không màu làm ngọn lửa có màu đặc trưng.
(4) A là KCl, B là NaCl, C là LiCl.
Số nhận định đúng là
-
A.
1
-
B.
2
-
C.
4
-
D.
3
Đáp án : B
Dựa vào đặc điểm hợp chất IA.
(1) đúng, tránh sai màu sắc của các hợp chất.
(2) sai, có ảnh hưởng đến kết quả của thí nghiệm.
(3) đúng
(4) sai, A là LiCl, B là NaCl, C là KCl.
Đáp án B
Để xác định hàm lượng FeCO3 trong quặng Siderirte, người ta làm như sau: cân 0,6g mẫu quặng, chế hóa nó theo một quy trình hợp lí, thu được FeSO4 trong môi trường H2SO4 loãng. Chuẩn độ dung dịch thu được bằng dung dịch chuẩn KMnO4 0,025M thì dùng vừa hết 25,2ml. % theo khối lượng của FeCO3 là:
-
A.
12,18%
-
B.
24,26%
-
C.
60,9%
-
D.
30,45%
Đáp án : C
Tính số mol của KMnO4, viết phương trình chuẩn độ của Fe2+.
n KMnO4 = 0,025.25,2 = 0,63 mmol.
10FeSO4 + 2KMnO4 + 18H2SO4 → 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 18H2O
3,15 ← 0,63
m FeCO3 = 3,15.10-3.116 = 0,3654g
%FeCO3 = \(\frac{{0,3654}}{{0,6}}.100 = 60,9\% \)
Đáp án C
Cho các phát biểu sau:
(a) Nước chứa nhiều cation Ca2+ và Mg2+ là nước cứng.
(b) Nước cứng chia làm 3 loại: nước có tính cứng tạm thời, nước có tính cứng vĩnh cửu và nước có tính cứng toàn phần.
(c) Nước cứng gây nhiều tác hại cho sản xuất và đời sống.
(d) Hai phương pháp làm mềm nước cứng phổ biến là phương pháp kết tủa và phương pháp trao đổi ion.
(e) Phương pháp trao đổi ion làm giảm được cả tính cứng tạm thời và tính cứng vĩnh cửu.
Số phát biểu đúng là
-
A.
3
-
B.
2
-
C.
5
-
D.
4
Đáp án : C
Dựa vào khái niệm và phân loại nước cứng.
(a) đúng
(b) đúng
(c) đúng
(d) đúng
(e) đúng.
Đáp án C
Tiến hành thí nghiệm điều chế kim loại bằng cách dùng kim loại mạnh khử ion của kim loại yếu trong dung dịch theo các bước sau đây:
Bước 1: Đánh sạch gỉ một chiếc đinh sắt (iron) rồi thả vào dung dịch CuSO4.
Bước 2: Sau khoảng 10 phút, quan sát màu của chiếc đinh sắt (iron) và màu của dung dịch.
Phát biểu nào sau đây sai?
-
A.
Đinh sắt bị phủ một lớp màu đỏ.
-
B.
Màu xanh của dung dịch không đổi vì đó là màu của ion sulfate
-
C.
Màu xanh của dung dịch bị nhạt dần vì nồng độ ion Cu2+ giảm dần trong quá trình phản ứng.
-
D.
Màu đỏ trên đinh sắt (iron) là do copper sinh ra bám vào.
Đáp án : B
Dựa vào tính chất hoá học và màu sắc của kim loại chuyển tiếp thứ nhất.
B sai, màu xanh của dung dịch giảm dần.
Đáp án B
Theo TCVN 5502 : 2003, các mẫu nước có tổng nồng độ Ca2+ và Mg2+ lớn hơn 5.10-4 M là nước cứng. Cho dung dịch có nồng độ các ion như sau: Na+ (0,005 M), Ca2+ (0,001 M); Mg2+ (0,0005 M); Cl- (0,002 M, HCO3- (0,0035 M); SO42- (0,00125 M). Mẫu nước trên thuộc loại
-
A.
nước mềm.
-
B.
nước cứng tạm thời.
-
C.
nước cứng toàn phần.
-
D.
nước cứng vĩnh cửu.
Đáp án : C
Dựa vào nồng độ của các ion.
Mẫu nước trên thuộc nước cứng toàn phần do có chứa ion HCO3- (0,0035 M); SO42- (0,00125 M)
Đáp án C
Đơn chất, hợp chất kim loại nhóm IA không có tính chất nào sau đây:
-
A.
Là các kim loại mềm, nhẹ, có nhiệt độ nóng chảy và nhiệt độ sôi tăng từ lithium đến caesium.
-
B.
Có tính khử mạnh, tính khử tăng từ lithium đến caesium.
-
C.
Được bảo quản bằng cách ngâm trong dầu hoả khan hoặc bình khí hiếm.
-
D.
Có thể phân biệt nhờ màu ngọn lửa đặc trưng khi đốt chúng trên ngọn lửa đèn khí.
Đáp án : A
Dựa vào tính chất của hợp chất kim loại IA.
A sai, nhiệt độ nóng chảy, nhiệt độ sôi và nhiệt độ nóng chảy có xu hướng giảm dần từ Li đến Cs.
Đáp án A
Thực hiện thí nghiệm như sau:
- Cho 2 mL dung dịch FeCl3 1M vào ống nghiệm (1) và 2 mL dung dịch CuSO4 1M vào ống nghiệm (2)
- Thêm tiếp vào mỗi ống nghiệm 2 – 3 giọt dung dịch NaOH 1M, lắc nhẹ.
a) Ống nghiệm (1) có kết tủa màu xanh lam, ống nghiệm (2) có kết tủa màu vàng.
b) Phản ứng xảy ra trong ống nghiệm (1) có phương trình ion thu gọn là: Fe3+ + 3OH- → Fe(OH)3.
c) Nếu cho NaOH dư vào cả hai ống nghiệm thì ống nghiệm (1) không thu được kết tủa, ống nghiệm (2) vẫn thu được kết tủa.
d) Nếu thay dung dịch NaOH bằng dung dịch Ba(OH)2 thì số chất kết tủa thu được vẫn không thay đổi.
a) Ống nghiệm (1) có kết tủa màu xanh lam, ống nghiệm (2) có kết tủa màu vàng.
b) Phản ứng xảy ra trong ống nghiệm (1) có phương trình ion thu gọn là: Fe3+ + 3OH- → Fe(OH)3.
c) Nếu cho NaOH dư vào cả hai ống nghiệm thì ống nghiệm (1) không thu được kết tủa, ống nghiệm (2) vẫn thu được kết tủa.
d) Nếu thay dung dịch NaOH bằng dung dịch Ba(OH)2 thì số chất kết tủa thu được vẫn không thay đổi.
Dựa vào màu sắc của các hợp chất kim loại chuyển tiếp thứ nhất.
a) sai, ống nghiệm (1) có kết tủa nâu đỏ, ống nghiệm (2) kết tủa xanh
b) đúng
c) sai, ống nghiệm (1) vẫn thu được kết tủa.
d) sai, có thêm kết tủa BaSO4.
Tiến hành thí nghiệm xác định hàm lượng iron (II) sulfate bằng phương pháp chuẩn độ thuốc tím trong môi trường sulfuric acid dư.
- Dùng pipette lấy 5,0 mL dung dịch FeSO4 cho vào bình tam giác; thêm tiếp khoảng 5 mL dung dịch H2SO4 10% (lấy bằng ống đong).
- Cho dung dịch KMnO4 vào burette, điều chỉnh thể tích dung dịch trong burette về mức 0.
- Mở khoá burette, nhỏ từng giọt dung dịch KMnO4 xuống bình tam giác, lắc đều.
a. Ban đầu dung dịch trong bình tam giác xuất hiện màu hồng rồi mất màu nhanh.
b. Cần sử dụng chất chỉ thị để nhận biết điểm kết thúc chuẩn độ.
c. Iron (II) sulfate là chất khử, thuốc tím là chất oxi hoá.
d. Chuẩn độ đến khi màu hồng tồn tại bền trong khoảng 20 giây thì dừng chuẩn độ.
a. Ban đầu dung dịch trong bình tam giác xuất hiện màu hồng rồi mất màu nhanh.
b. Cần sử dụng chất chỉ thị để nhận biết điểm kết thúc chuẩn độ.
c. Iron (II) sulfate là chất khử, thuốc tím là chất oxi hoá.
d. Chuẩn độ đến khi màu hồng tồn tại bền trong khoảng 20 giây thì dừng chuẩn độ.
Dựa vào phương pháp chuẩn độ dung dịch Fe2+ bằng thuốc tím.
a. đúng
b. sai, vì nhận biết điểm kết thúc chuẩn độ bằng chính dung dịch KMnO4.
c. đúng
d. đúng
Cắt mẫu sodium bằng hạt đậu xanh, làm sạch lớp dầu bằng giấy thấm dầu. Dùng kẹp gắp mẩu sodium cho vào cốc nước có nhỏ vài giọt phenolphthalein.
a) Mẫu Na phản ứng chạy trên mặt nước.
b) Phản ứng giải phóng khí hydrogen.
c) Cốc nước hoá hồng.
d) Phản ứng với nước thu nhiệt.
a) Mẫu Na phản ứng chạy trên mặt nước.
b) Phản ứng giải phóng khí hydrogen.
c) Cốc nước hoá hồng.
d) Phản ứng với nước thu nhiệt.
Dựa vào tính chất hoá học của kim loại kiềm.
a) đúng
b) đúng
c) đúng
d) sai, phản ứng với nước toả nhiệt mạnh.
Y là hợp chất của calcium có nhiều ở dạng đá vôi, đá hoa,…Hợp chất Z có trong thành phần của không khí và thường dùng để chữa cháy, Biết rằng, Z được sinh ra khi cho Y phản ứng với dung dịch acid mạnh.
a) Chất Y và Z lần lượt là CaCO3 và N2.
b) Chất Y được sinh ra khi sục chất Z dư vào dung dịch Ca(OH)2.
c) Chất Y và Z đóng vai trò hình thành thạch nhũ trong hang động đá vôi.
d) Chất Y là nguyên liệu sản xuất NaHCO3 và Na2CO3 theo phương pháp Solvay.
a) Chất Y và Z lần lượt là CaCO3 và N2.
b) Chất Y được sinh ra khi sục chất Z dư vào dung dịch Ca(OH)2.
c) Chất Y và Z đóng vai trò hình thành thạch nhũ trong hang động đá vôi.
d) Chất Y là nguyên liệu sản xuất NaHCO3 và Na2CO3 theo phương pháp Solvay.
Dựa vào đặc tính của các hợp chất.
a) sai vì chất Y và Z lần lượt là CaCO3 và CO2.
b) sai, vì CO2 dư tạo muối Ca(HCO3)2.
c) đúng
d) đúng
Sodium carbonate (Na2CO3) là chất thường dùng để làm mềm nước cứng theo phương pháp kết tủa. Độ cứng của nước có thể tính theo số mg CaCO3 trong 1 lít nước, trong đó độ cứng không vượt quá 60mg.L-1 là nước mềm. Để xử lí một mẫu nước cứng vĩnh cửu có độ cứng a (mg CaCO3/L) người ta cho 1 lít dung dịch Na2CO3 0,020M vào 19 lít mẫu nước cứng, lắc đều, thu được kết tủa CaCO3 và nước mềm Y. Nồng độ Ca2+ và CO32- có trong mẫu nước mềm Y lần lượt là 5,00.10-4M và 8,93.10-6M. Giả thiết rằng, mẫu nước cứng chứa Ca2+ và các ion khác, các ion khác này không tham gia phản ứng, ion CO32- và ion Ca2+ không bị thuỷ phân trong nước. Tính giá trị của a (làm tròn đến hàng đơn vị).
Na2CO3 thêm vào để kết tủa và loại bỏ ion Ca2+ và Mg2+.
n Na2CO3 = 0,02 mol => n CO32- = 0,02 mol
CM CO32- ban đầu = 0,02 : 20 = 0,001M
=> CM CO32- phản ứng = 0,001 – 8,93.10-6 = 9,9107.10-4 (M)
[Ca2+] ban đầu = \(\frac{{a{{.10}^{ - 3}}}}{{100}}.19:20 = 9,{5.10^{ - 6}}.a(M)\)
=> [Ca2+] còn dư = 9,5.10-6.a - 9,9107.10-4 = 5.10-4 => a = 157
Đáp số 157.
Calcium oxide (CaO) còn được gọi là vôi sống, phần lớn được dùng làm vật liệu xây dựng. Ngoài ra, nó còn được dùng để làm chất hút ẩm trong công nghiệp, khử chua, tẩy uế….Có thể sản xuất vôi sống bằng cách nung đá vôi CaCO3 trong lò nung theo phương trình hoá học (1) như sau:
Phản ứng (1) là phản ứng thu nhiệt. Lượng nhiệt này được cung cấp từ quá trình đốt cháy hoàn toàn carbon trong lò nung theo phương trình hoá học (2):
C (graphite) + O2(g) → CO2(g) (2)
Xét các phản ứng ở điều kiện chuẩn, hiệu suất chuyển hoá calcium carbonate thành calcium oxide là 100%. Tính khối lượng calcium oxide sản xuất được (theo tấn, làm tròn đến hàng đơn vị) trong các quá trình trên khi đốt cháy hoàn toàn 28,8 tấn carbon (graphite). Biết có 90% nhiệt lượng toả ra từ phản ứng (2) được cung cấp cho phản ứng (1) và các giá trị nhiệt tạo thành (\({\Delta _f}H_{298}^o\)) ở các chất ở điều kiện chuẩn được cho trong bảng sau:
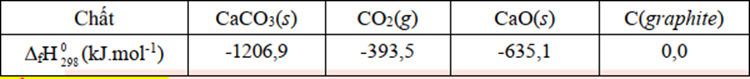
Tính biến thiên enthalpy của phản ứng (2), (1)
\(\begin{array}{l}{\Delta _r}H_{298}^o(1) = {\Delta _f}H_{298}^o(C{O_2}) + {\Delta _f}H_{298}^o(CaO) - {\Delta _f}H_{298}^o(CaC{O_3})\\ = ( - 393,5) + ( - 635,1) - ( - 1206,9) = 178,3kJ\end{array}\)
\({\Delta _r}H_{298}^o(2) = \Delta fH_{298}^o(C{O_2}) = - 393,5kJ\)
n C = 28,8 : 12 = 2,4 tấn mol => Nhiệt lượng toả ra khi đốt cháy hết 28,8 tấn là: 2,4.393,5.106 = 944,4.106 kJ.
Khối lượng CaO thu được là = \(\frac{{944,{{4.10}^6}.90\% }}{{178,3}}{.56.10^{ - 6}} = 267\)tấn
Tiến hành thí nghiệm xác định thành phần một chiếc đinh sắt (đã bị oxi hoá một phần thành gỉ sắt, Fe2O3.xH2O) theo các bước sau.
- Bước 1: Hoà tan toàn bộ đinh sắt trong dung dịch H2SO4 loãng (dùng gấp đôi lượng phản ứng, giả thiết Fe chỉ phản ứng với acid), thu được 250 mL dung dịch X.
- Bước 2: Nhỏ dung dịch BaCl2 dư vào cốc chứa 10,0 mL dung dịch X, thu được 0,8202 gam kết tủa trắng.
- Bước 3: Tiến hành chuẩn độ 10,0 mL dung dịch X bằng dung dịch KMnO4 0,02 M cần vừa đủ 12,80 mL.
Khối lượng của Fe2O3 ở đinh sắt ban đầu là bao nhiêu gam? (Làm tròn kết quả đến hàng phần mười)
Viết phương trình phản ứng của tường bước thí nghiệm. Tính số mol KMnO4 từ tỉ lệ tính được số mol của Fe.
Khối lượng của Fe2O3 là 0,6 gam
- Bước 1: Fe2O3 + 6H+ → 2Fe3+ + 3H2O (1)
a → 6a 2a
Fe + 2H+ → Fe2+ + H2↑ (2) [Lưu ý: bỏ qua phản ứng Fe + 2Fe3+ → 3Fe2+]
b → 2b b
- Bước 2: Ba2+ + SO42- → BaSO4↓ (3)
- Bước 3: 5Fe2+ + MnO4- + 8H+ → 5Fe3+ + Mn2+ + 4H2O (4)
+ Trong 250 ml dung dich X: chứa Fe3+ (2a), Fe2+ (b), H+ (6a + 2b), SO42- (6a + 2b)
+ Trong 10 ml dung dich X:
Bước 2: nSO42- = nBaSO4 = 3,52.10-3 (mol)
Bước 3: nFe2+ = 5nMnO4- = 1,28.10-3 (mol)
→ 6a + 2b = 25. 3,52.10-3
→ b = 25.1,28.10-3
→ b = 0,032 (mol) → a = 0,004 (mol) → mFe2O3 = 0,64 (gam)
Có bao nhiêu chất bị phân huỷ bởi nhiệt độ trong dãy các chất sau: Na2CO3, BaCO3, CaSO4, Ca(HCO3)2, Mg(NO3)2, NaHCO3.
Dựa vào tính chất hoá học của muối carbonate và nitrate của hợp chất kim loại IIA.
BaCO3, Ca(HCO3)2, Mg(NO3)2, NaHCO3 bị nhiệt phân bởi nhiệt.
Đáp án 4
Khi nói về hiện tượng gỉ (rỉ) sắt khi để gang, thép để trong không khí ẩm, một học sinh đã có phát biểu sau:
(1) Hiện tượng trên xảy ra chủ yếu do gang thép bị ăn mòn ăn mòn điện hóa.
(2) Khi bị ăn mòn điện hóa, nguyên tử Fe trong gang, thép đóng vai trò anode.
(3) Nguyên tử Fe đã bị khử thành cation Fe2+ theo quá trình Fe → Fe2+ + 2e.
(4) Nếu để gang thép trong không khí khô thì tốc độ rỉ sắt chậm hơn so với không khí ẩm
Liệt kê các phát biểu đúng theo thứ tự tăng dần.
Dựa vào sự ăm nòn của kim loại.
(1) đúng
(2) đúng
(3) sai, vì Fe bị oxi hoá thành Fe3+
(4) đúng
Đáp án 124
Muối Nigari (MgCl2.6H2O) làm đông tụ nhanh sữa đậu nành thành đậu hũ. Làm lạnh 805 gam dung dịch bão hoà MgCl2 ở 60 °C xuống 10 °C thì có m gam tinh thể MgCl2.6H2O tách ra khỏi dung dịch bão hoà. Biết độ tan của MgCl2 trong nước ở 10 °C và 60 °C lần lượt là 52,9 gam là 61,0 gam. Tính giá trị của m.
Tính khối lượng muối MgCl2 ở 2 nhiệt độ.
Ở 60oC: mMgCl2 = 805.61/(100 + 61) = 305 gam
Ở 10oC: mMgCl2 = (805-m).52,9/(100 + 52,9) + 95m/203 = 305 gam
=> m = 217
Hợp chất Kn[Fe(CN)6], trong đó Fe có số oxi hóa +3. Giá trị của n bằng
Cho phát biểu sau: “Phức chất đơn giản thường có một ...(1)...
Trong mạng tinh thể kim loại, liên kết kim loại được hình thành do
Nhiệt độ nóng chảy của các kim loại nhóm IA từ Li đến Cs biến đổi như thế nào?










Danh sách bình luận