Đề thi học kì 2 Hóa 12 Kết nối tri thức - Đề số 3
Cho phát biểu sau: “Phức chất đơn giản thường có một ...(1)...
Đề bài
Cho phát biểu sau: “Phức chất đơn giản thường có một ...(1)... liên kết với các phối tử bao quanh. Liên kết giữa nguyên từ trung tâm và phối tử trong phức chất là liên kết ...(2)....”. Cụm từ cần điền vào (1) và (2) lần lượt là:
-
A.
Cation kim loại, ion.
-
B.
Nguyên từ kim loại, cho - nhận.
-
C.
Nguyên từ trung tâm, cho - nhận.
-
D.
Phối tử, ion.
Phần tử có thể trở thành phối tử trong phức chất là:
-
A.
Anion hoặc phân tử trung hòa có cặp electron hóa trị riêng.
-
B.
Anion có kích thước lớn.
-
C.
Phân tử trung hòa có hoặc không có cặp electron hóa trị riêng.
-
D.
Cation kim loại chuyển tiếp có các orbital trống.
Cho các phát biểu sau:
(a) Tất cả các kim loại kiềm thổ đều tan trong nước.
(b) Các kim loại kiềm có thể đẩy được kim loại yếu hơn ra khỏi dung dịch muối của chúng.
(c) Các ion Na+, Mg2+, Al3+ có cùng cấu hình electron ở trạng thái cơ bản và đều có tính oxi
hóa yếu.
(d) Các kim loại kiềm K, Rb, Cs tự bốc cháy khi tiếp xúc với nước.
(e) Kim loại magnesium có cấu trúc mạng tinh thể lục phương.
Trong các phát biểu trên số phát biểu đúng là
-
A.
2
-
B.
3
-
C.
4
-
D.
5
Cho sơ đồ chuyển hoá sau:
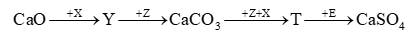
Biết: X, Y, Z, T, E là các hợp chất khác nhau; mỗi mũi tên ứng với một phương trình hoá học.
Các chất Z, E thoả mãn sơ đồ trên lần lượt là
-
A.
Na2CO3, H2SO4.
-
B.
CO2, KHSO4.
-
C.
NaHCO3, Na2SO4.
-
D.
CO2, BaSO4.
Phức chất nào sau đây có dạng bát diện?
-
A.
\({{\rm{[}}PtC{l_4}{\rm{]}}^{2 - }}\)
-
B.
\({{\rm{[}}Ni{(N{H_3})_4}]^{2 + }}\)
-
C.
\({{\rm{[}}Co{(N{H_3})_6}]^{3 + }}\)
-
D.
\({{\rm{[}}Ag{(N{H_3})_2}]^ + }\)
Có 3 ống nghiệm chứa riêng biệt: dung dịch bakinh soda, dung dịch lithium chloride, dung dịch potassium carbonate. Với mỗi dung dịch, nhúng đầu dây platinum vào rồi đem đốt trên ngọn lửa đèn khí.
Các phát biểu sau:
(a) Ngọn lửa có màu đỏ tía là của dung dịch baking soda.
(b) Ngọn lửa có màu vàng là của dung dịch baking soda.
(c) Ngọn lửa có màu tím là của dung dịch potassium carbonate.
(d) Ngọn lửa có màu đỏ tía là của dung dịch lithium chloride.
Số phát biểu đúng là
-
A.
2
-
B.
1
-
C.
3
-
D.
4
Trước khi thi đấu các môn thể thao như cử tạ, thể dục dụng cụ…, các vận động viên thường thoa vào tay một ít muối magnesium carbonate dưới dạng bột màu trắng nhằm tăng ma sát và hút ẩm. Công thức hóa học của magnesium carbonate là
-
A.
MgCO3.
-
B.
MnCO3.
-
C.
Mg(HCO3)2.
-
D.
CaSO4.
Cho bốn dung dịch sau: K2CO3, BaCl2, MgSO4, NaOH. Số dung dịch tác dụng với lượng dư dung dịch H2SO4 là
-
A.
3
-
B.
2
-
C.
1
-
D.
4
Một mẫu chất có thành phần chính là muối Mohr. Muối Mohr có công thức hoá học là (NH4)2SO4.FeSO4.6H2O. Hoà tan 0,2151 g mẫu chất trong dung dịch sulfuric acid loãng dư, thu được dung dịch có chứa cation Fe2+. Lượng Fe2+ trong dung dịch này phản ứng vừa đủ với 5,40 mL dung dịch thuốc tím nồng độ 0,020 M (Các chất và ion khác trong dung dịch không phản ứng với thuốc tím). Số mg sắt có trong mẫu chất là
-
A.
30,24.
-
B.
28,00
-
C.
30,80
-
D.
33,60
Khi hòa tan hợp chất CoCl2 vào nước thì hình thành phức chất aqua có dạng hình học là bát diện. Công thức của phức chất là
-
A.
[Co(OH2)6]3+.
-
B.
[Co(OH2)6]2+.
-
C.
[CoCl2(OH2)4].
-
D.
[CoCl2(OH2)4]2+.
Khi hòa tan hợp chất AgNO3 vào nước thì thu được dung dịch chứa phức chất tứ diện [Ag(OH2)m]n+ (aq).
Các phát biểu dưới đây về phức chất [Ag(OH2)m]n+:
(a) có điện tích +1.
(b) được hình thành từ quá trình cation Ag+ (aq) nhận các cặp electron hóa trị riêng từ các phân tử nước.
(c) có giá trị của m là 4.
(d) bền hơn cation Ag+ (aq).
Số phát biểu đúng là
-
A.
2
-
B.
1
-
C.
3
-
D.
4
Nhúng thanh sắt và thanh đồng vào cốc chứa dung dịch H2SO4 0,5M. Dùng dây dẫn điện nối thanh sắt và thanh đồng với đèn led như hình vẽ.
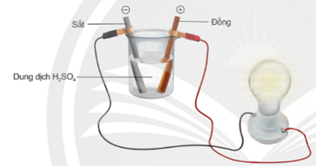
Các phát biểu sau về thí nghiệm như sau
(a) Bóng đèn phát sáng.
(b) Có bọt khí thoát ra ở thanh đồng.
(c) Thanh đồng nhanh chóng bị ăn mòn.
(d) Dung dịch chuyển sang màu xanh lam.
(e) Bọt khí thoát ra ở cả hai thanh
Số phát biểu đúng là
-
A.
2
-
B.
5
-
C.
6
-
D.
4
Cho bản số liệu độ tan (g/100 g nước) của muối sulfate của các kim loại nhóm IIA ở 20oC trong bảng sau:
|
Anion |
Cation |
|||
|
Mg2+ |
Ca2+ |
Sr2+ |
Ba2+ |
|
|
\(SO_4^{2 - }\) |
33,7 |
0,20 |
0,0132 |
0,0028 |
Hợp chất dễ tan là
-
A.
MgSO4.
-
B.
CaSO4.
-
C.
SrSO4.
-
D.
BaSO4
Nước cứng toàn phần gồm những thành phần của anion gốc acid với cation nào?
-
A.
\(C{a^{2 + }},{\rm{ }}M{g^{2 + }},HCO_3^ - ,SO_4^{2 - },C{l^ - }.\)
-
B.
\(C{a^{2 + }},{\rm{ }}M{g^{2 + }},HCO_3^ - .\)
-
C.
\(C{a^{2 + }},{\rm{ }}M{g^{2 + }},HCO_3^ - ,SO_4^{2 - },B{r^ - }.\)
-
D.
\(C{a^{2 + }},{\rm{ }}M{g^{2 + }},SO_4^{2 - }.\)
Hợp chất nào của calcium được dùng để đúc tượng, bó bột khi gãy xương?
-
A.
Thạch cao nung (CaSO4.H2O).
-
B.
Đá vôi (CaCO3).
-
C.
Vôi sống (CaO).
-
D.
Thạch cao sống (CaSO4.2H2O).
Trong xương động vật, nguyên tố calcium và phosphorus tồn tại chủ yếu dưới dạng Ca3(PO4)2. Theo em để ninh (hầm) được một nồi nước xương giàu calcium và phosphorus cung cấp dinh dưỡng cho cơ thể ta nên sử dụng cách nào trong các cách sau:
-
A.
Chỉ ninh xương với nước.
-
B.
Cho thêm một ít vôi tôi.
-
C.
Cho thêm một ít muối ăn.
-
D.
Cho thêm một ít quả chua: me, chanh,…
Trong quá trình Solvay, ở giai đoạn tạo thành NaHCO3 tồn tại cân bằng sau:
NaCI + NH3 + CO2 + H2O NaHCO3 + NH4CI
Khi làm lạnh dung dịch trên, muối bị tách ra khỏi dung dịch là
-
A.
NaHCO3.
-
B.
NH4Cl.
-
C.
NaCl.
-
D.
NH4HCO3.
Thành phần dịch vị dạ dày gồm 95% là nước, enzyme và hydrochloric aicid. Sự có mặt của hydrochloric aicid làm cho pH của dịch vị trong khoảng từ 2 – 3. Khi độ acid trong dịch vị dạ dày tăng thì dễ bị ợ chua, ợ hơi, ói mửa, buồn nôn, loét dạ dày, tá tràng. Để làm giảm bớt lượng acid dư trong dịch vị dạ dày người ta thường uống thuốc muối dạ dày“NABICA” từng lượng nhỏ và cách quãng.
Cho các phát biểu sau:
(a). Công thức hoá học của thuốc muối “Nabica” là NaHCO3.
(b). Công thức hoá học của thuốc muối “Nabica” là Na2CO3.
(c). Khi uống từng lượng nhỏ và cách quãng thuốc muối dạ dày “Nabica” thì pH của dịch vị dạ dày sẽ tăng từ từ.
(d). Khi uống từng lượng nhỏ và cách quãng thuốc muối dạ dày “Nabica” thì pH của dịch vị dạ dày sẽ giảm từ từ.
(e). Nếu có 10ml dịch vị dạ dày và coi pH của dạ dày hoàn toàn do hydrochloric acid gây ra, để nâng pH của dạ dày từ pH=1 lên pH=2 ta cần dùng hết 0,0756 gam thuốc muối Nabica(với giả thiết Nabica là nguyên chất).
(f). Khi uống thuốc muối dạ dày “Nabica” thì sẽ sinh ra khí carbon dioxide
(g). Khi uống thuốc muối dạ dày “Nabica” thì sẽ sinh khí carbon monoxide
(h). Các Bác sĩ khuyến cáo không lạm dụng uống nhiều Nabica vì uống nhiều Nabica sẽ làm mất cân bằng acid trong dạ dày làm cho bệnh càng trầm trọng hơn.
Số phát biểu đúng là
-
A.
5
-
B.
6
-
C.
4
-
D.
3
Nhiễm độc chì luôn luôn đáng lo ngại. Trong cơ thể con người, mức độ độc hại của chì có thể được giảm bớt bằng cách sử dụng phối tử EDTA4- để tạo phức [Pb(EDTA)]2- rất bền (hằng số bền β(Pb) = 1018,0) và được thận bài tiết. Phối tử EDTA4- được cung cấp bằng cách tiêm truyền dung dịch Na2[Ca(EDTA)]. Biết phức [Ca(EDTA)]2- tương đối kém bền (hằng số bền β(Ca) = 1010,7), sự trao đổi calcium với chì chủ yếu diễn ra trong mạch máu. Hàm lượng chì trong máu của một bệnh nhân là 0,828 μg/mL.
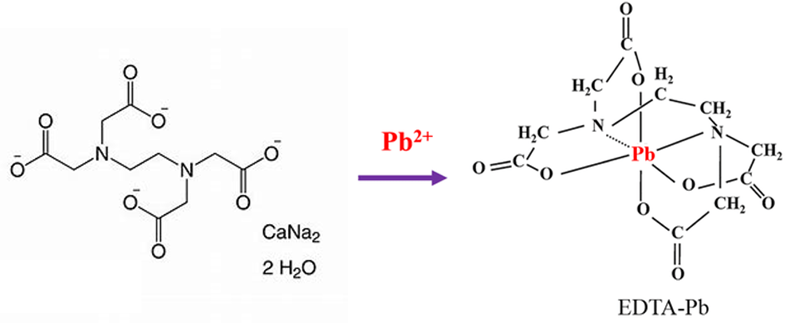
a. Nồng độ chì trong máu của bệnh nhân này là 4 (μmol/L).
b. [Pb(EDTA)]2- là phức đa càng, trong đó EDTA hoạt động như phối tử đa càng, liên kết với Pb2+ qua bốn nhóm chức.
c. Phức [Pb(EDTA)]2- bền hơn phức [Ca(EDTA)]2- nên xảy ra phản ứng thế Ca2+ bằng Pb2+ trong phức chất.
d. Phức [Pb(EDTA)]2- là một phức bền, có kích thước lớn và khó hòa tan trong nước, cho phép nó đi qua màng lọc của cầu thận và được bài tiết ra ngoài qua nước tiểu.
Cho bảng giá trị biến thiên enthalpy chuẩn của phản ứng phân hủy muối carbonate của một số nguyên tố nhóm IIA:
|
Muối MCO3 |
\({\Delta _r}H_{298}^o\)(kJ mol-1) |
|
MgCO3 |
100,7 |
|
CaCO3 |
179,2 |
|
SrCO3 |
234,6 |
|
BaCO3 |
271,5 |
a. Các muối này đều bị nhiệt phân thành oxide kim loại và carbon dioxide.
b. Độ bền nhiệt của các muối này có xu hướng giảm dần từ MgCO3 đến BaCO3.
c. Khi cùng phân hủy 1 mol các muối carbonate thì BaCO3 cần hấp thu nhiều năng lượng nhất.
d. Để phân huỷ hoàn toàn 100 g đá vôi (chứa 98% CaCO3) lượng khí CO2 thoát ra là 19,44 L (đkc), biết hiệu suất phản ứng là 80%.
Cho các phát biểu sau:
a. Nguyên tắc làm mềm nước cứng là làm giảm nồng độ của các ion magnesium và ion calcium.
b. Thành phần chính của bột thạch cao là hợp chất gồm calcium và gốc sulfate.
c. Nhiệt phân Mg(NO3)2(s) thu được khí duy nhất là NO2.
d. Bảo quản Na, K bằng cách ngâm trong dầu hỏa.
Cho vào ống nghiệm khoảng 0,5 mL CuSO4 0,5 M, sau đó thêm từ từ khoảng 2 mL dung dịch HCl đặc, lắc ống nghiệm, thì diễn ra quá trình sau:
[Cu(OH2)6)]2+(màu xanh) + 4Cl− ⇋ [CuCl4]2−(màu vàng) + 6H2O
a. Nếu tăng nồng độ Cl–(aq) thì màu xanh của dung dịch trở lên đậm hơn.
b. Phản ứng trên là phản ứng thay thế phối tử của phức chất trong dung dịch.
c. Phức [CuCl4]2– bền hơn phức [Cu(H2O)6]2+.
d. Phức chất [Cu(OH2)6)]2+ là phức bát diện.
Trong quá trình ăn mòn điện hóa của sắt (Fe), sự ăn mòn xảy ra khi sắt bị oxy hóa tại vùng anodic, trong khi phản ứng khử xảy ra tại vùng cathodic với sự hiện diện của oxygen và độ ẩm. Các phát biểu sau đây là đúng hay sai về các yếu tố liên quan đến quá trình ăn mòn sắt?
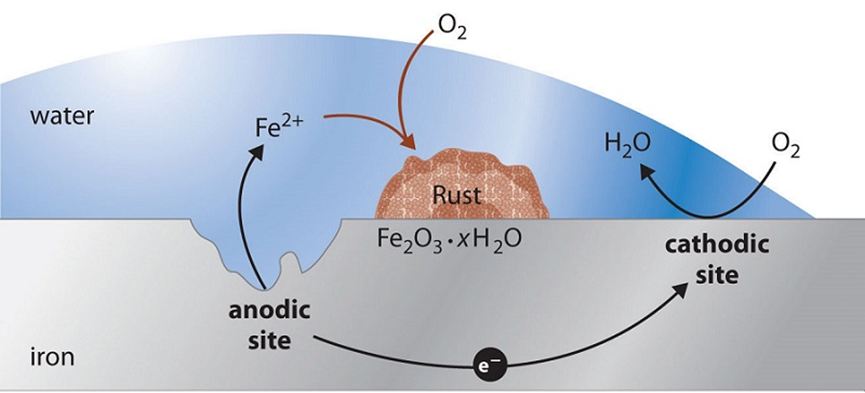
(1) Ở anode, sắt bị oxi hóa thành ion Fe²⁺, trong khi ở cathode, oxygen bị khử tạo thành ion hydroxide (OH⁻), dẫn đến sự hình thành gỉ sét.
(2) Độ ẩm giúp tạo một lớp điện ly mỏng, cho phép các ion di chuyển tự do, hỗ trợ quá trình ăn mòn.
(3) Các vùng kim loại bị trầy xước hoặc chịu tác động cơ học có xu hướng trở thành anode, dễ bị ăn mòn hơn.
(4) Khi hai kim loại khác nhau tiếp xúc trong môi trường ẩm, ăn mòn điện hóa được hình thành, với kim loại ít hoạt động hơn bị ăn mòn trước.
(5) Việc phủ lớp kẽm (mạ kẽm) có thể bảo vệ sắt nhờ vào lớp phủ hy sinh này, trong khi mạ thiếc có thể thúc đẩy ăn mòn nếu lớp phủ bị tổn thương.
Calcium trong máu hoặc nước tiểu có thể được xác định bằng kết tủa dưới dạng calcium oxalate (CaC2O4). Hòa tan kết tủa trong acid mạnh và chuẩn độ bằng dung dịch KMnO4. Phương trình phản ứng là:
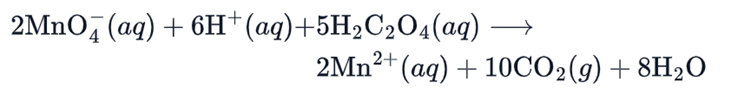
Mẫu nước tiểu 24 giờ được thu thập từ một bệnh nhân người lớn, một lượng nhỏ thể tích được trích ra và chuẩn độ vừa đủ với 26,2 mL KMnO4 0,0946 M. Ngưỡng cho phép về hàm lượng Ca2+ trong mẫu lượng cho một người lớn là 100 đến 300 mg mỗi 24 giờ. Hàm lượng Ca2+ (mg) trong máu của người lớn này là bao nhiêu? Làm tròn đến số nguyên gần nhất.
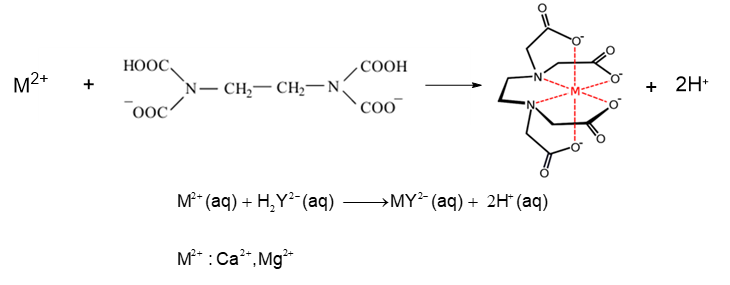
Một nhà máy muốn xác định độ cứng tổng và nồng độ ion Ca²⁺ của mẫu nước khoáng. Trong Phần A, kỹ sư chuẩn độ 50 cm³ nước khoáng với ethylenediaminetetraacetic acid (EDTA) 0,01 M, mất 18,5 mL EDTA để chuyển màu đỏ rượu sang xanh da trời. Trong Phần B, kỹ sư thêm NaOH để loại Mg²⁺, sau đó chuẩn độ 50 cm³ nước khoáng với EDTA 0,01 M, mất 12,4 mL để chuyển sang màu xanh da trời. Hãy tính Nồng độ Mg²⁺ (ppm) trong nước. Biết ppm số mg chất tan trong 1 L dung dịch và phương trình chuẩn độ như sau:
Trong số các chất sau: Ca(OH)2, Na2CO3, Na3PO4, KCl có bao nhiêu chất có thể làm mềm nước có tính cứng tạm thời là bao nhiêu chất?
Cho các phát biểu:
(1) Sodium chloride được dùng trong chế biến thức ăn.
(2) Sodium chloride có nhiều trong nước biển, mỏ muối.
(3) Potassium chloride dùng làm phân bón hóa học.
(4) Để bảo quản kim loại Na ta ngâm trong dầu hỏa.
(5) Khi uống thuốc chứa sodium hydrocarbonat thì trong dạ dày xảy ra phản ứng của acetic acid với sodium hydrocarbonat.
Sắp xếp các phát biểu đúng theo thứ tự tăng dần?
Soda khan (Na2CO3) là hóa chất dùng để xử lí các bể bơi, có thể loại bỏ hai cation Ca2+ và Mg2+ (có tác dụng làm mềm nước cứng). Theo kết quả phân tích, để xử lí 100 m3 nước cần 2,55 kg Na2CO3. Khối lượng soda (kg) cần thiết để xử lí 557,35 m3 nước ở hồ bơi là ?
Lời giải và đáp án
Cho phát biểu sau: “Phức chất đơn giản thường có một ...(1)... liên kết với các phối tử bao quanh. Liên kết giữa nguyên từ trung tâm và phối tử trong phức chất là liên kết ...(2)....”. Cụm từ cần điền vào (1) và (2) lần lượt là:
-
A.
Cation kim loại, ion.
-
B.
Nguyên từ kim loại, cho - nhận.
-
C.
Nguyên từ trung tâm, cho - nhận.
-
D.
Phối tử, ion.
Đáp án : C
Dựa vào khái niệm của phức chất.
(1) Nguyên tử trung tâm; (2) cho – nhận.
Đáp án C
Phần tử có thể trở thành phối tử trong phức chất là:
-
A.
Anion hoặc phân tử trung hòa có cặp electron hóa trị riêng.
-
B.
Anion có kích thước lớn.
-
C.
Phân tử trung hòa có hoặc không có cặp electron hóa trị riêng.
-
D.
Cation kim loại chuyển tiếp có các orbital trống.
Đáp án : A
Dựa vào khái niệm về nguyên tử trung tâm.
Anion hoặc phân tử trung hoà có cặp electron hoá trị riêng có thể trở thành phối tử do tạo được liên kết cho – nhận.
Đáp án A
Cho các phát biểu sau:
(a) Tất cả các kim loại kiềm thổ đều tan trong nước.
(b) Các kim loại kiềm có thể đẩy được kim loại yếu hơn ra khỏi dung dịch muối của chúng.
(c) Các ion Na+, Mg2+, Al3+ có cùng cấu hình electron ở trạng thái cơ bản và đều có tính oxi
hóa yếu.
(d) Các kim loại kiềm K, Rb, Cs tự bốc cháy khi tiếp xúc với nước.
(e) Kim loại magnesium có cấu trúc mạng tinh thể lục phương.
Trong các phát biểu trên số phát biểu đúng là
-
A.
2
-
B.
3
-
C.
4
-
D.
5
Đáp án : A
Dựa vào tính chất hoá học của kim loại kiềm.
(a) sai, Mg. Be là kim loại kiềm thổ không tan trong nước.
(b) sai, kim loại kiềm tác dụng với nước tạo hydroxide nên không đẩy được kim loại ra khỏi muối.
(c) đúng
(d) đúng
(e) sai, Mg có cấu trúc mạng tinh thể lập phương.
Đáp án A
Cho sơ đồ chuyển hoá sau:
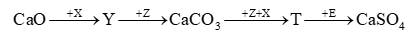
Biết: X, Y, Z, T, E là các hợp chất khác nhau; mỗi mũi tên ứng với một phương trình hoá học.
Các chất Z, E thoả mãn sơ đồ trên lần lượt là
-
A.
Na2CO3, H2SO4.
-
B.
CO2, KHSO4.
-
C.
NaHCO3, Na2SO4.
-
D.
CO2, BaSO4.
Đáp án : B
Dựa vào tính chất hoá học của nhóm IIA.
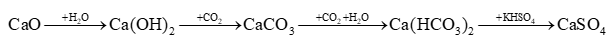
Vậy Z là CO2 và E là KHSO4 sẽ thoả mãn sơ đồ trên.
Đáp án B
Phức chất nào sau đây có dạng bát diện?
-
A.
\({{\rm{[}}PtC{l_4}{\rm{]}}^{2 - }}\)
-
B.
\({{\rm{[}}Ni{(N{H_3})_4}]^{2 + }}\)
-
C.
\({{\rm{[}}Co{(N{H_3})_6}]^{3 + }}\)
-
D.
\({{\rm{[}}Ag{(N{H_3})_2}]^ + }\)
Đáp án : C
Phức chất có hình bát diện khi có số phối tử 6.
\({{\rm{[}}Co{(N{H_3})_6}]^{3 + }}\)có dạng bát diện.
Đáp án C
Có 3 ống nghiệm chứa riêng biệt: dung dịch bakinh soda, dung dịch lithium chloride, dung dịch potassium carbonate. Với mỗi dung dịch, nhúng đầu dây platinum vào rồi đem đốt trên ngọn lửa đèn khí.
Các phát biểu sau:
(a) Ngọn lửa có màu đỏ tía là của dung dịch baking soda.
(b) Ngọn lửa có màu vàng là của dung dịch baking soda.
(c) Ngọn lửa có màu tím là của dung dịch potassium carbonate.
(d) Ngọn lửa có màu đỏ tía là của dung dịch lithium chloride.
Số phát biểu đúng là
-
A.
2
-
B.
1
-
C.
3
-
D.
4
Đáp án : C
Dựa vào ngọn lửa khi đốt muối của nhóm IA.
(a) sai, ngọn lửa màu vàng là của dung dịch baking soda.
(b) đúng
(c) đúng
(d) đúng
Đáp án C
Trước khi thi đấu các môn thể thao như cử tạ, thể dục dụng cụ…, các vận động viên thường thoa vào tay một ít muối magnesium carbonate dưới dạng bột màu trắng nhằm tăng ma sát và hút ẩm. Công thức hóa học của magnesium carbonate là
-
A.
MgCO3.
-
B.
MnCO3.
-
C.
Mg(HCO3)2.
-
D.
CaSO4.
Đáp án : A
Dựa vào tên gọi của muối.
Magnesium carbonate có công thức là MgCO3.
Đáp án A
Cho bốn dung dịch sau: K2CO3, BaCl2, MgSO4, NaOH. Số dung dịch tác dụng với lượng dư dung dịch H2SO4 là
-
A.
3
-
B.
2
-
C.
1
-
D.
4
Đáp án : A
Dựa vào tính chất hoá học của hợp chất nhóm IA, IIA.
K2CO3 + H2SO4 → K2SO4 + CO2 + H2O
BaCl2 + H2SO4 → BaSO4 + 2HCl
2NaOH + H2SO4 → Na2SO4 + H2O
Một mẫu chất có thành phần chính là muối Mohr. Muối Mohr có công thức hoá học là (NH4)2SO4.FeSO4.6H2O. Hoà tan 0,2151 g mẫu chất trong dung dịch sulfuric acid loãng dư, thu được dung dịch có chứa cation Fe2+. Lượng Fe2+ trong dung dịch này phản ứng vừa đủ với 5,40 mL dung dịch thuốc tím nồng độ 0,020 M (Các chất và ion khác trong dung dịch không phản ứng với thuốc tím). Số mg sắt có trong mẫu chất là
-
A.
30,24.
-
B.
28,00
-
C.
30,80
-
D.
33,60
Đáp án : A
Dựa vào phương trình chuẩn độ muối Mohr.
n KMnO4 = 5,4.0,02 = 0,108 mmol.
10FeSO4 + 18H2SO4 + 2KMnO4 → 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 18H2O
0,54 ← 0,108
m Fe = 0,54.56 = 30,24 mmg
Đáp án A
Khi hòa tan hợp chất CoCl2 vào nước thì hình thành phức chất aqua có dạng hình học là bát diện. Công thức của phức chất là
-
A.
[Co(OH2)6]3+.
-
B.
[Co(OH2)6]2+.
-
C.
[CoCl2(OH2)4].
-
D.
[CoCl2(OH2)4]2+.
Đáp án : B
Dựa vào phản ứng thay thế phối tử của phức chất.
Vì phản ứng tạo thành phức aqua có dạng hình bát diện nên có công thức là [Co(OH2)6]2+ vì điện tích của Co là 2+, số phối tử = 6.
Đáp án B
Khi hòa tan hợp chất AgNO3 vào nước thì thu được dung dịch chứa phức chất tứ diện [Ag(OH2)m]n+ (aq).
Các phát biểu dưới đây về phức chất [Ag(OH2)m]n+:
(a) có điện tích +1.
(b) được hình thành từ quá trình cation Ag+ (aq) nhận các cặp electron hóa trị riêng từ các phân tử nước.
(c) có giá trị của m là 4.
(d) bền hơn cation Ag+ (aq).
Số phát biểu đúng là
-
A.
2
-
B.
1
-
C.
3
-
D.
4
Đáp án : D
Dựa vào cấu tạo của phức chất.
(a) đúng, do phối tử aqua là phân tử nên điện tích của phức bằng điện tích của Ag.
(b) đúng
(c) đúng, do phức chất có hình tứ diện.
(d) đúng do khi hoà tan AgNO3 vào nước sẽ tạo ra phức chất bền hơn chính nó.
Nhúng thanh sắt và thanh đồng vào cốc chứa dung dịch H2SO4 0,5M. Dùng dây dẫn điện nối thanh sắt và thanh đồng với đèn led như hình vẽ.

Các phát biểu sau về thí nghiệm như sau
(a) Bóng đèn phát sáng.
(b) Có bọt khí thoát ra ở thanh đồng.
(c) Thanh đồng nhanh chóng bị ăn mòn.
(d) Dung dịch chuyển sang màu xanh lam.
(e) Bọt khí thoát ra ở cả hai thanh
Số phát biểu đúng là
-
A.
2
-
B.
5
-
C.
6
-
D.
4
Đáp án : D
Dựa vào nguyên tắc hoạt động của pin điện.
(a) đúng, vì có dòng điện hình thành.
(b) đúng, do 2H+ → H2 + 2e
(c) sai, thanh kẽm bị ăn mòn trước.
(d) đúng
(e) đúng
Cho bản số liệu độ tan (g/100 g nước) của muối sulfate của các kim loại nhóm IIA ở 20oC trong bảng sau:
|
Anion |
Cation |
|||
|
Mg2+ |
Ca2+ |
Sr2+ |
Ba2+ |
|
|
\(SO_4^{2 - }\) |
33,7 |
0,20 |
0,0132 |
0,0028 |
Hợp chất dễ tan là
-
A.
MgSO4.
-
B.
CaSO4.
-
C.
SrSO4.
-
D.
BaSO4
Đáp án : A
Dựa vào bảng độ tan của các muối.
Hợp chất MgSO4 có độ tan lớn nhất nên là hợp chất dễ tan.
Đáp án A
Nước cứng toàn phần gồm những thành phần của anion gốc acid với cation nào?
-
A.
\(C{a^{2 + }},{\rm{ }}M{g^{2 + }},HCO_3^ - ,SO_4^{2 - },C{l^ - }.\)
-
B.
\(C{a^{2 + }},{\rm{ }}M{g^{2 + }},HCO_3^ - .\)
-
C.
\(C{a^{2 + }},{\rm{ }}M{g^{2 + }},HCO_3^ - ,SO_4^{2 - },B{r^ - }.\)
-
D.
\(C{a^{2 + }},{\rm{ }}M{g^{2 + }},SO_4^{2 - }.\)
Đáp án : A
Dựa vào thành phần và phân loại nước cứng.
Nước cứng toàn phần gồm \(C{a^{2 + }},{\rm{ }}M{g^{2 + }},HCO_3^ - ,SO_4^{2 - },C{l^ - }.\)
Đáp án A
Hợp chất nào của calcium được dùng để đúc tượng, bó bột khi gãy xương?
-
A.
Thạch cao nung (CaSO4.H2O).
-
B.
Đá vôi (CaCO3).
-
C.
Vôi sống (CaO).
-
D.
Thạch cao sống (CaSO4.2H2O).
Đáp án : A
Dựa vào ứng dụng của hợp chất nhóm IIA.
Thạch cao nung được dùng để đúc tượng, bó bột khi gãy xương.
Đáp án A
Trong xương động vật, nguyên tố calcium và phosphorus tồn tại chủ yếu dưới dạng Ca3(PO4)2. Theo em để ninh (hầm) được một nồi nước xương giàu calcium và phosphorus cung cấp dinh dưỡng cho cơ thể ta nên sử dụng cách nào trong các cách sau:
-
A.
Chỉ ninh xương với nước.
-
B.
Cho thêm một ít vôi tôi.
-
C.
Cho thêm một ít muối ăn.
-
D.
Cho thêm một ít quả chua: me, chanh,…
Đáp án : D
Dựa vào tính chất của hợp chất nhóm IIA.
Cho thêm một ít quả chua sẽ làm phân huỷ hợp chất muối của calcium từ đó tạo ra nhiều ion Ca2+.
Đáp án D
Trong quá trình Solvay, ở giai đoạn tạo thành NaHCO3 tồn tại cân bằng sau:
NaCI + NH3 + CO2 + H2O NaHCO3 + NH4CI
Khi làm lạnh dung dịch trên, muối bị tách ra khỏi dung dịch là
-
A.
NaHCO3.
-
B.
NH4Cl.
-
C.
NaCl.
-
D.
NH4HCO3.
Đáp án : A
Dựa vào độ kết tinh của các loại muối.
NaHCO3 có nhiệt độ kết tinh thấp nên khi làm lạnh muối này sẽ bị tách ra khỏi dung dịch trước.
Đáp án A
Thành phần dịch vị dạ dày gồm 95% là nước, enzyme và hydrochloric aicid. Sự có mặt của hydrochloric aicid làm cho pH của dịch vị trong khoảng từ 2 – 3. Khi độ acid trong dịch vị dạ dày tăng thì dễ bị ợ chua, ợ hơi, ói mửa, buồn nôn, loét dạ dày, tá tràng. Để làm giảm bớt lượng acid dư trong dịch vị dạ dày người ta thường uống thuốc muối dạ dày“NABICA” từng lượng nhỏ và cách quãng.
Cho các phát biểu sau:
(a). Công thức hoá học của thuốc muối “Nabica” là NaHCO3.
(b). Công thức hoá học của thuốc muối “Nabica” là Na2CO3.
(c). Khi uống từng lượng nhỏ và cách quãng thuốc muối dạ dày “Nabica” thì pH của dịch vị dạ dày sẽ tăng từ từ.
(d). Khi uống từng lượng nhỏ và cách quãng thuốc muối dạ dày “Nabica” thì pH của dịch vị dạ dày sẽ giảm từ từ.
(e). Nếu có 10ml dịch vị dạ dày và coi pH của dạ dày hoàn toàn do hydrochloric acid gây ra, để nâng pH của dạ dày từ pH=1 lên pH=2 ta cần dùng hết 0,0756 gam thuốc muối Nabica(với giả thiết Nabica là nguyên chất).
(f). Khi uống thuốc muối dạ dày “Nabica” thì sẽ sinh ra khí carbon dioxide
(g). Khi uống thuốc muối dạ dày “Nabica” thì sẽ sinh khí carbon monoxide
(h). Các Bác sĩ khuyến cáo không lạm dụng uống nhiều Nabica vì uống nhiều Nabica sẽ làm mất cân bằng acid trong dạ dày làm cho bệnh càng trầm trọng hơn.
Số phát biểu đúng là
-
A.
5
-
B.
6
-
C.
4
-
D.
3
Đáp án : A
Dựa vào tính chất hoá học của hợp chất nhóm IA.
(a). Đúng, Công thức hoá học của thuốc muối “Nabica” là NaHCO3.
(b). Sai, Công thức hoá học của thuốc muối “Nabica” là Na2CO3.
(c). Đúng, Khi uống từng lượng nhỏ và cách quãng thuốc muối dạ dày “Nabica” thì pH của dịch vị dạ dày sẽ tăng từ từ.
(d). Sai vì Khi uống từng lượng nhỏ và cách quãng thuốc muối dạ dày “Nabica” thì pH của dịch vị dạ dày sẽ giảm từ từ.
(e). Đúng, Nếu có 10ml dịch vị dạ dày và coi pH của dạ dày hoàn toàn do axit clohiđric gây ra, để nâng pH của dạ dày từ pH=1 lên pH=2 ta cần dùng hết 0,0756 gam thuốc muối Nabica(với giả thiết Nabica là nguyên chất)
(f). Đúng, Khi uống thuốc muối dạ dày “Nabica” thì sẽ sinh ra khí carbon dioxide.
(g). Sai, Khi uống thuốc muối dạ dày “Nabica” thì sẽ sinh khí carbon monoxide.
(h). Đúng, Các Bác sĩ khuyến cáo không lạm dụng uống nhiều Nabica vì uống nhiều Nabica sẽ làm mất cân bằng axit trong dạ dày làm cho bệnh càng trầm trọng hơn.
Đáp án A
Nhiễm độc chì luôn luôn đáng lo ngại. Trong cơ thể con người, mức độ độc hại của chì có thể được giảm bớt bằng cách sử dụng phối tử EDTA4- để tạo phức [Pb(EDTA)]2- rất bền (hằng số bền β(Pb) = 1018,0) và được thận bài tiết. Phối tử EDTA4- được cung cấp bằng cách tiêm truyền dung dịch Na2[Ca(EDTA)]. Biết phức [Ca(EDTA)]2- tương đối kém bền (hằng số bền β(Ca) = 1010,7), sự trao đổi calcium với chì chủ yếu diễn ra trong mạch máu. Hàm lượng chì trong máu của một bệnh nhân là 0,828 μg/mL.

a. Nồng độ chì trong máu của bệnh nhân này là 4 (μmol/L).
b. [Pb(EDTA)]2- là phức đa càng, trong đó EDTA hoạt động như phối tử đa càng, liên kết với Pb2+ qua bốn nhóm chức.
c. Phức [Pb(EDTA)]2- bền hơn phức [Ca(EDTA)]2- nên xảy ra phản ứng thế Ca2+ bằng Pb2+ trong phức chất.
d. Phức [Pb(EDTA)]2- là một phức bền, có kích thước lớn và khó hòa tan trong nước, cho phép nó đi qua màng lọc của cầu thận và được bài tiết ra ngoài qua nước tiểu.
a. Nồng độ chì trong máu của bệnh nhân này là 4 (μmol/L).
b. [Pb(EDTA)]2- là phức đa càng, trong đó EDTA hoạt động như phối tử đa càng, liên kết với Pb2+ qua bốn nhóm chức.
c. Phức [Pb(EDTA)]2- bền hơn phức [Ca(EDTA)]2- nên xảy ra phản ứng thế Ca2+ bằng Pb2+ trong phức chất.
d. Phức [Pb(EDTA)]2- là một phức bền, có kích thước lớn và khó hòa tan trong nước, cho phép nó đi qua màng lọc của cầu thận và được bài tiết ra ngoài qua nước tiểu.
Dựa vào tính chất hoá học của phức chất.
a. đúng, vì hàm lượng chì trong máu là 0,828 μg/mL => nồng độ chì trong máu của bệnh nhân là: \(\frac{{0,828}}{{207}}{.10^3} = 4\mu mol/L\)
b. sai, EDTA liên kết với Pb2+ qua 6 nhóm chức.
c. đúng
d. sai, Phức [Pb(EDTA)]2- dễ tan trong nước
Cho bảng giá trị biến thiên enthalpy chuẩn của phản ứng phân hủy muối carbonate của một số nguyên tố nhóm IIA:
|
Muối MCO3 |
\({\Delta _r}H_{298}^o\)(kJ mol-1) |
|
MgCO3 |
100,7 |
|
CaCO3 |
179,2 |
|
SrCO3 |
234,6 |
|
BaCO3 |
271,5 |
a. Các muối này đều bị nhiệt phân thành oxide kim loại và carbon dioxide.
b. Độ bền nhiệt của các muối này có xu hướng giảm dần từ MgCO3 đến BaCO3.
c. Khi cùng phân hủy 1 mol các muối carbonate thì BaCO3 cần hấp thu nhiều năng lượng nhất.
d. Để phân huỷ hoàn toàn 100 g đá vôi (chứa 98% CaCO3) lượng khí CO2 thoát ra là 19,44 L (đkc), biết hiệu suất phản ứng là 80%.
a. Các muối này đều bị nhiệt phân thành oxide kim loại và carbon dioxide.
b. Độ bền nhiệt của các muối này có xu hướng giảm dần từ MgCO3 đến BaCO3.
c. Khi cùng phân hủy 1 mol các muối carbonate thì BaCO3 cần hấp thu nhiều năng lượng nhất.
d. Để phân huỷ hoàn toàn 100 g đá vôi (chứa 98% CaCO3) lượng khí CO2 thoát ra là 19,44 L (đkc), biết hiệu suất phản ứng là 80%.
Dựa vào giá trị biến thiên enthalpy chuẩn của phản ứng nhiệt phân muối.
a. đúng
b. sai, độ bền nhiệt tăng dần từ MgCO3 đến BaCO3.
c. đúng
d. đúng
m CaCO3 = 100.98% = 98g => n CaCO3 = 98 : 100 = 0,98 mol => n CO2 = 0,98.24,79.80% = 19,44L
Cho các phát biểu sau:
a. Nguyên tắc làm mềm nước cứng là làm giảm nồng độ của các ion magnesium và ion calcium.
b. Thành phần chính của bột thạch cao là hợp chất gồm calcium và gốc sulfate.
c. Nhiệt phân Mg(NO3)2(s) thu được khí duy nhất là NO2.
d. Bảo quản Na, K bằng cách ngâm trong dầu hỏa.
a. Nguyên tắc làm mềm nước cứng là làm giảm nồng độ của các ion magnesium và ion calcium.
b. Thành phần chính của bột thạch cao là hợp chất gồm calcium và gốc sulfate.
c. Nhiệt phân Mg(NO3)2(s) thu được khí duy nhất là NO2.
d. Bảo quản Na, K bằng cách ngâm trong dầu hỏa.
Dựa vào tính chất hoá học của nhóm IIA.
a. đúng
b. đúng
c. sai, thu được khí O2.
d. đúng
Cho vào ống nghiệm khoảng 0,5 mL CuSO4 0,5 M, sau đó thêm từ từ khoảng 2 mL dung dịch HCl đặc, lắc ống nghiệm, thì diễn ra quá trình sau:
[Cu(OH2)6)]2+(màu xanh) + 4Cl− ⇋ [CuCl4]2−(màu vàng) + 6H2O
a. Nếu tăng nồng độ Cl–(aq) thì màu xanh của dung dịch trở lên đậm hơn.
b. Phản ứng trên là phản ứng thay thế phối tử của phức chất trong dung dịch.
c. Phức [CuCl4]2– bền hơn phức [Cu(H2O)6]2+.
d. Phức chất [Cu(OH2)6)]2+ là phức bát diện.
a. Nếu tăng nồng độ Cl–(aq) thì màu xanh của dung dịch trở lên đậm hơn.
b. Phản ứng trên là phản ứng thay thế phối tử của phức chất trong dung dịch.
c. Phức [CuCl4]2– bền hơn phức [Cu(H2O)6]2+.
d. Phức chất [Cu(OH2)6)]2+ là phức bát diện.
Dựa vào tính chất hoá học của phức chất.
a. sai, khi tăng nồng độ Cl- thì màu xanh của dung dịch nhạt dần.
b. đúng
c. đúng
d. đúng
Trong quá trình ăn mòn điện hóa của sắt (Fe), sự ăn mòn xảy ra khi sắt bị oxy hóa tại vùng anodic, trong khi phản ứng khử xảy ra tại vùng cathodic với sự hiện diện của oxygen và độ ẩm. Các phát biểu sau đây là đúng hay sai về các yếu tố liên quan đến quá trình ăn mòn sắt?

(1) Ở anode, sắt bị oxi hóa thành ion Fe²⁺, trong khi ở cathode, oxygen bị khử tạo thành ion hydroxide (OH⁻), dẫn đến sự hình thành gỉ sét.
(2) Độ ẩm giúp tạo một lớp điện ly mỏng, cho phép các ion di chuyển tự do, hỗ trợ quá trình ăn mòn.
(3) Các vùng kim loại bị trầy xước hoặc chịu tác động cơ học có xu hướng trở thành anode, dễ bị ăn mòn hơn.
(4) Khi hai kim loại khác nhau tiếp xúc trong môi trường ẩm, ăn mòn điện hóa được hình thành, với kim loại ít hoạt động hơn bị ăn mòn trước.
(5) Việc phủ lớp kẽm (mạ kẽm) có thể bảo vệ sắt nhờ vào lớp phủ hy sinh này, trong khi mạ thiếc có thể thúc đẩy ăn mòn nếu lớp phủ bị tổn thương.
Dựa vào sự ăn mòn kim loại.
(1) sai, sắt bị oxi hoá thành ion Fe3+.
(2) đúng
(3) đúng
(4) đúng
(5) đúng
Số phát biểu đúng là 4
Calcium trong máu hoặc nước tiểu có thể được xác định bằng kết tủa dưới dạng calcium oxalate (CaC2O4). Hòa tan kết tủa trong acid mạnh và chuẩn độ bằng dung dịch KMnO4. Phương trình phản ứng là:
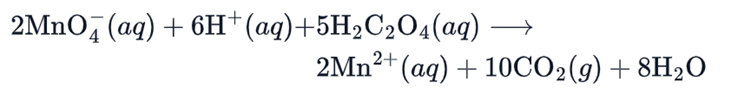
Mẫu nước tiểu 24 giờ được thu thập từ một bệnh nhân người lớn, một lượng nhỏ thể tích được trích ra và chuẩn độ vừa đủ với 26,2 mL KMnO4 0,0946 M. Ngưỡng cho phép về hàm lượng Ca2+ trong mẫu lượng cho một người lớn là 100 đến 300 mg mỗi 24 giờ. Hàm lượng Ca2+ (mg) trong máu của người lớn này là bao nhiêu? Làm tròn đến số nguyên gần nhất.
Tính số mol KMnO4, dựa vào phương trình hoá học tính được lượng Ca2+
n KMnO4 = 26,2.0,0946 = 2,47852mmol.
n Ca2+ = 6,1963 mmol
m Ca2+ = 248mg.
Đáp án 248.
Một nhà máy muốn xác định độ cứng tổng và nồng độ ion Ca²⁺ của mẫu nước khoáng. Trong Phần A, kỹ sư chuẩn độ 50 cm³ nước khoáng với ethylenediaminetetraacetic acid (EDTA) 0,01 M, mất 18,5 mL EDTA để chuyển màu đỏ rượu sang xanh da trời. Trong Phần B, kỹ sư thêm NaOH để loại Mg²⁺, sau đó chuẩn độ 50 cm³ nước khoáng với EDTA 0,01 M, mất 12,4 mL để chuyển sang màu xanh da trời. Hãy tính Nồng độ Mg²⁺ (ppm) trong nước. Biết ppm số mg chất tan trong 1 L dung dịch và phương trình chuẩn độ như sau:

Tính nồng độ EDTA sau đó tính nồng độ Mg2+.
n EDTA trong phần 1 = 18,5.0,01 = 0,185 mmol.
n EDTA trong phần 2 = 12,4.0,01 = 0,124 mmol => n Ca2+ = 0,124 mmol => n Mg2+ = 0,185 – 0,124 = 0,061 mmol.
Đổi 50 cm3 = 0,05L.
Nồng độ Mg2+ là: 0,061.24 : 0,05 = 29,28 ppm ≈ 29ppm.
Đáp án 29
Trong số các chất sau: Ca(OH)2, Na2CO3, Na3PO4, KCl có bao nhiêu chất có thể làm mềm nước có tính cứng tạm thời là bao nhiêu chất?
Nguyên tắc làm mềm nước cứng là giảm nồng độ ion Ca2+ và Mg2+.
Nước cứng tạm thời có thể làm mềm bằng Ca(OH)2, Na2CO3, Na3PO4.
Đáp án 3
Cho các phát biểu:
(1) Sodium chloride được dùng trong chế biến thức ăn.
(2) Sodium chloride có nhiều trong nước biển, mỏ muối.
(3) Potassium chloride dùng làm phân bón hóa học.
(4) Để bảo quản kim loại Na ta ngâm trong dầu hỏa.
(5) Khi uống thuốc chứa sodium hydrocarbonat thì trong dạ dày xảy ra phản ứng của acetic acid với sodium hydrocarbonat.
Sắp xếp các phát biểu đúng theo thứ tự tăng dần?
Dựa vào tính chất hoá học của hợp chất nhóm IA.
(1) đúng
(2) đúng
(3) đúng
(4) đúng
(5) sai, phản ứng giữa acid HCl.
Đáp án 1234.
Soda khan (Na2CO3) là hóa chất dùng để xử lí các bể bơi, có thể loại bỏ hai cation Ca2+ và Mg2+ (có tác dụng làm mềm nước cứng). Theo kết quả phân tích, để xử lí 100 m3 nước cần 2,55 kg Na2CO3. Khối lượng soda (kg) cần thiết để xử lí 557,35 m3 nước ở hồ bơi là ?
Dựa vào tính chất hoá học của nhóm IA.
Cho sodan khan vào nước thì phân li thành hai ion : Na+,CO32-
Na2CO3 ⇌ 2Na+ + CO32-
Ion CO32- giúp loại bỏ được hai ion Ca2+ và Mg2+ :
Ca2+ + CO32- → CaCO3
Mg 2+ + CO32- → MgCO3
mSoda cần dùng = \(\frac{{2,55.557,35}}{{100}} = 14,2kg\)
Đáp án 14,2
Các rạn san hô và đá vôi có thành phần chính là:
Hợp chất Kn[Fe(CN)6], trong đó Fe có số oxi hóa +3. Giá trị của n bằng
Trong mạng tinh thể kim loại, liên kết kim loại được hình thành do
Nhiệt độ nóng chảy của các kim loại nhóm IA từ Li đến Cs biến đổi như thế nào?










Danh sách bình luận