Đề thi học kì 2 Hóa 12 Kết nối tri thức - Đề số 5
Hợp chất Kn[Fe(CN)6], trong đó Fe có số oxi hóa +3. Giá trị của n bằng
Đề bài
Hợp chất Kn[Fe(CN)6], trong đó Fe có số oxi hóa +3. Giá trị của n bằng
-
A.
4
-
B.
2
-
C.
3
-
D.
6
Kim loại chuyển tiếp nào cho dưới đây không phản ứng với dung dịch HCl?
-
A.
Mn.
-
B.
Fe.
-
C.
Cu.
-
D.
Ni.
Ion Na+ là một trong những chất điện giải quan trọng trong cơ thể con người, và lượng tiêu thụ của nó có ảnh hưởng lớn đến sức khỏe. Các chuyên gia khuyến nghị rằng lượng sodium hàng ngày của một người trưởng thành không nên vượt quá 2400 mg.
Bột ngọt (mì chính) là muối sodium của glutamic acid với công thức C₅H₈NO₄Na.
Hỏi khi tiêu thụ 2,0 g bột ngọt, lượng sodium trong đó tương đương với bao nhiêu gam muối ăn (NaCl)? Cho khối lượng mol: H = 1, C = 12; N = 14; O = 16; Na = 23;; Cl = 35,5.
-
A.
0,692 gam.
-
B.
0,136 gam.
-
C.
0,346 gam.
-
D.
0,272 gam.
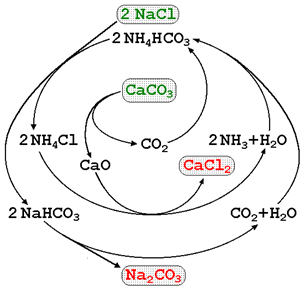
Phương pháp Solvay là phương pháp phổ biến nhất hiện nay để sản xuất Na2CO3. Hình dưới. Phương trình hóa học nào sau đây không có trong phương pháp Solvay?
-
A.
NaCl + NH₃ + H₂O + CO₂ → NH₄Cl + NaHCO₃
-
B.
NH3 + 2HCl → NH4Cl
-
C.
CaCO₃ → CaO + CO₂
-
D.
2NaHCO3 → Na2CO3 + CO2 + H2O
Tiến hành các thí nghiệm sau:
(a) Điện phân MgCl2 nóng chảy.
(b) Nhiệt phân hoàn toàn BaCO3.
(c) Cho kim loại K vào dung dịch CuSO4 dư.
(d) Dẫn khí CO dư đi qua bột Fe2O3 nung nóng.
(e) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3 dư.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được kim loại là
-
A.
4
-
B.
2
-
C.
5
-
D.
3
Nguyên tố X thuộc chu kì 3, nhóm IIA. Cấu hình electron nguyên tử của X là
-
A.
1s22s22p1.
-
B.
1s22s22p63s2.
-
C.
1s22s22p63s23p2.
-
D.
1s22s22p63s1.
Cho cấu hình electron 26Fe là [Ar]3d64s2. Cấu hình electron nào sau đây là của ion Fe3+
-
A.
[Ar]3d6.
-
B.
[Ar]3d44s2.
-
C.
[Ar]3d54s1.
-
D.
[Ar]3d5.
Cho dung dịch HCl vào dung dịch chất X, thu được khí không màu, nặng hơn không khí, mùi sốc. Chất X là
-
A.
NaOH.
-
B.
NaHCO3.
-
C.
NaHSO3.
-
D.
NaCl.
Ở một số quốc gia, khoáng vật trona là nguyên liệu chính để sản xuất soda. Thành phần hóa học chính của khoáng vật trona là
-
A.
Na2CO3.NaHCO3.2H2O.
-
B.
3NaF.AlF3.
-
C.
NaNO3.
-
D.
NaCl.KCl.
Cho các phát biểu sau
1. Nước cứng là nước chứa nhiều cation Ca2+ và Mg2+.
2. Nguyên tố calcium có nhiều trong sữa, ngũ cốc, các loại hạt, rau cải, hải sản,…
3. Nguyên tố nhóm IA tồn tại trong tự nhiên dưới dạng đơn chất.
4. Hợp kim Mg – Al được dùng để chế tạo các bộ phận của máy bay, ô tô,…
Số phát biểu đúng là
-
A.
1
-
B.
2
-
C.
3
-
D.
4
Cho các phát biểu sau:
a. Phức chất [CoCl2(NH3)4]+ có dạng hình học bát diện.
b. Phức chất [CoCl2(NH3)4]+ có điện tích +3, nguyên tử trung tâm là Co phối tử là Cl và NH3.
c. Trong công thức của phức chất [CoCl2(NH3)4]Cl, [CoCl2(NH3)4]+ là cầu nội, Cl- là cầu ngoại.
d. Vitamin B12 là phức chất của [CoCl2(NH3)4]+ có vai trò thiết yếu trong việc hình thành tế bào hồng cầu, chuyển hoá tế bào, chức năng thần kinh và sản xuất DNA.
Số phát biểu đúng là
-
A.
3
-
B.
2
-
C.
1
-
D.
4
Thực hiện các thí nghiệm sau:
(a) Cho Na vào H2O.
(b) Cho bột Mg dư vào dung dịch FeCl3.
(c) Cho Al vào dung dịch AgNO3.
(d) Cho Al vào dung dịch HCl.
(e) Cho Ag vào dung dịch H2SO4 loãng.
(g) Cho bột Fe dư vào dung dịch HNO3 đặc, nguội.
Số thí nghiệm xảy ra phản ứng là
-
A.
2
-
B.
3
-
C.
4
-
D.
5
Đốt cháy cation K+ngọn lửa có màu gì?
-
A.
Xanh da trời.
-
B.
Đỏ.
-
C.
Vàng.
-
D.
Tím hoa cà.
Cho dãy các chất: MgCO3, CaCO3, SrCO3, BaCO3. Độ bền nhiệt của muối carbonate lớn nhất là
-
A.
MgCO3.
-
B.
CaCO3.
-
C.
SrCO3.
-
D.
BaCO3.
Cho các phức chất có công thức sau: [Fe(OH2)6]2+, [PtCl2(NH3)2], [Cu(NH3)4] 2+, [Co(NH3)6]3+. Số phức chất mang điện tích và số phức chất không mang điện tích lần lượt là
-
A.
2 và 2
-
B.
3 và 1
-
C.
1 và 3
-
D.
4 và 0
Phức chất [Co(NH3)6]Cl3 có số phối trí là 6. Phức này có dạng hình học nào sau đây?
-
A.
Đường thẳng.
-
B.
Bát diện.
-
C.
Tứ diện.
-
D.
Lưỡng chóp tam giác
Phức chất aqua có dạng bát diện khi cho copper (II) sulfate vào nước. Công thức của phức là
-
A.
Cu(H2O)6
-
B.
Cu(H2O)4
-
C.
[Cu(H2O)6] SO4
-
D.
[Cu(OH2)4] SO4
Phản ứng nào dưới đây không là phản ứng thay thế phối tử trong phức chất
-
A.
[Cr(OH2)6]3+ + 6OH- → [Cr(OH)6]3- + 6H2O
-
B.
[Ni(OH2)6]3+ + 6NH3 → [Cr(NH3)6]2+ + 6H2O
-
C.
Cu2+ + 6H2O → [Cu(H2O)6]2+
-
D.
[NiCl4]2- + 2NH3 → [NiCl2(NH3)2] + 2Cl-
Quặng vàng (Gold) tồn tại trong tự nhiên thường có hàm lượng vàng thấp. Phương pháp tách vàng phù hợp hiện nay là phương pháp Cyanide. Theo phương pháp này, để thu hồi vàng từ quặng, người ta thường nghiền nhỏ quặng rồi hoà tan trong dung dịch KCN (potassium cyanide, rất độc) cùng với dòng không khí liên tục được thổi vào. Khi đó, vàng bị hoà tan tạo thành phức chất (các chất khác trong quặng không phản ứng với KCN):
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l) → 4K[Au(CN)2](aq) + 4KOH(aq) (1)
Tiếp theo cho bột kẽm đến dư vào dung dịch phức, thu được bột vàng (có lẫn một ít bột kẽm):
Zn(s) + 2K[Au(CN)2] (aq) → K2[Zn(CN)4] (aq)+ 2Au(s) (2)
a) Phương pháp tách vàng ở trên thân thiện với môi trường.
b) Phương pháp tách vàng ở trên là phương pháp thuỷ luyện.
c) Để loại bỏ Zn lẫn trong bột vàng, có thể dùng dung dịch HCl.
d) Để thu được 37,5 gam vàng cần 23,5 gam KCN (hiệu suất cả quá trình tách đạt 95%). Biết nguyên tử khối của C = 12; N = 14; K = 39; Au = 197.
Thép thường hay là thép carbon là hợp kim của Fe và C (≤ 2%), nguyên tố khác rất ít hoặc không có. Để xác định hàm lượng Fe trong một mẫu thép chứa Fe, C và Si người ta thực hiện các thí nghiệm sau:
- Cân 10,00 gam mẫu thép rồi cho vào 200mL dung dịch H2SO4 1M, đến khi phản ứng xảy ra hoàn toàn được 200,0mL dung dịch X.
-Lấy 10,0mL dung dịch X vào trong cốc thủy tinh, thêm tiếp dung dịch H2SO4 1M (dư) rồi chuẩn độ bằng dung dịch KMnO4 0,1M. Kết thúc chuẩn độ, thể tích (mL) dung dịch KMnO4 0,1M sử dụng qua 3 lần chuẩn độ như sau:

a) Vai trò của C trong thép là bảo vệ Fe không bị ăn mòn điện hóa.
b) Hàm lượng Fe trong thép là 98,0%.
c) Trong phản ứng chuẩn độ, chất khử là KMnO4.
d) Điểm tương đương (kết thúc chuẩn độ) là khi dung dịch trong cốc bắt đầu chuyển màu tím.
Những phát biểu nào sau đây về phức chất bát diện [Cu(OH2)6]2+ là đúng?
a. Nguyên tử trung tâm được hình thành từ quá trình cation Cu2+ sử dụng 6 orbital trống để nhận các cặp electron hoá trị riêng của các phân tử H2O
b. Số oxi hoá của nguyên tử trung tâm là +2.
c. Số liên kết cho - nhận giữa phối tử và nguyên tử trung tâm cũng là hoá trị phổ biến của đồng.
d. Mỗi phân tử nước chỉ sử dụng 1 trong 2 cặp electron hoá trị riêng của nó để tạo liên kết cho - nhận với cation Cu2+.
Hòa tan hoàn toàn x gam kim loại R trong m gam dung dịch H2SO4 đặc, nóng, vừa đủ. Sau khi phản ứng xảy ra hoàn toàn, thu được 2,479 lít SO2 (sản phẩm khử duy nhất, ở đkc) và m gam dung dịch chỉ chứa muối.
a. Trong phản ứng trên, H2SO4 là chất bị oxi hóa.
b. R là kim loại chuyển tiếp dãy thứ nhất.
c. Trong muối thu được, R có số oxi hóa +2.
d. Giá trị của x lớn hơn 5,6.
Một nhà hóa học trẻ quyết định nghiên cứu về sự nhiệt phân muối cobalt(II) sulfate pentahydrate (CoSO4.5H2O) để phục vụ cho dự án khoa học của mình. Để tiến hành, anh ta đặt một mẫu muối màu hồng tươi vào thiết bị phân tích nhiệt trọng (TGA) và bắt đầu quá trình đun nóng đến 950°C. Kết quả là anh ta nhận được đồ thị về sự phụ thuộc của khối lượng mẫu vào nhiệt độ như trong hình sau:
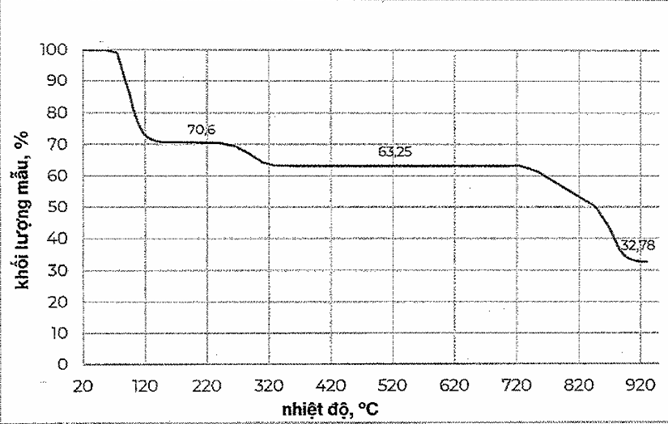
Số nguyên tử trong một phân tử mẫu ở 220oC là bao nhiêu?
Cho một mẫu hợp kim Na–Ba tác dụng với nước (dư), thu được dung dịch X và 3,7185 lít khí H2 (ở đkc). Để trung hòa dung dịch X cần dùng V mL dung dịch acid H2SO4 2M. Xác định giá trị của V?
Một vết nứt đường ray tàu hỏa có thể thể tích 8,96 cm3. Người ta dùng hỗn hợp Tecmit (Al và Fe2O3 theo tỉ lệ mol tương ứng 2:1) để hàn vết nứt trên. Biết lượng Fe cần hàn cho vết nứt bằng 79% lượng Fe sinh ra trong phản ứng nhiệt nhôm và giả thiết chỉ xảy ra phản ứng khử Fe2O3 thành Fe với hiệu suất 96%. Khối lượng riêng của sắt 7,9 g/cm3. Khối lượng của hỗn hợp Tecmit tối thiểu cần dùng trong quá trình trên trên là bao nhiêu gam? (Làm tròn kết quả đến hàng đơn vị).
Cho từ từ K (potassium) dư vào các dung dịch các chất sau : CuSO4, NH4Cl, NaHCO3, Ba(HCO3)2, Al(NO3)3, FeCl2, ZnSO4. Có bao nhiêu trường hợp vừa có khí thoát ra vừa có kết tủa sau khi phản ứng kết thúc?
Nhiệt phân hoàn toàn 40g một loại quặng dolomite có lẫn tạp chất trơ sinh ra 9,916 lít khí CO2 (điều kiện chuẩn). Thành phần phần trăm về khối lượng của CaCO3.MgCO3 trong loại quặng nêu trên là bao nhiêu?
Cho các ứng dụng: (1) nguyên liệu sản xuất thủy tinh; (2) sản xuất sodium; (3) tẩy vết dầu mỡ trước khi mạ điện, sơn, hàn; (4) tách ion Fe3+ để xử lí nước phèn; (5) làm mềm nước cứng. Có bao nhiêu ứng dụng là của sodium carbonate?
Lời giải và đáp án
Hợp chất Kn[Fe(CN)6], trong đó Fe có số oxi hóa +3. Giá trị của n bằng
-
A.
4
-
B.
2
-
C.
3
-
D.
6
Đáp án : C
Dựa vào số oxi hoá của Fe.
Hợp chất trên trung hoà về điện mà Fe có số oxi hoá +3 nên n = 3.
Đáp án C
Kim loại chuyển tiếp nào cho dưới đây không phản ứng với dung dịch HCl?
-
A.
Mn.
-
B.
Fe.
-
C.
Cu.
-
D.
Ni.
Đáp án : C
Dựa vào ý nghĩa của thế điện cực của kim loại.
Cu có thế điện cực lớn hơn H+ nên không phản ứng với dung dịch HCl.
Đáp án C
Ion Na+ là một trong những chất điện giải quan trọng trong cơ thể con người, và lượng tiêu thụ của nó có ảnh hưởng lớn đến sức khỏe. Các chuyên gia khuyến nghị rằng lượng sodium hàng ngày của một người trưởng thành không nên vượt quá 2400 mg.
Bột ngọt (mì chính) là muối sodium của glutamic acid với công thức C₅H₈NO₄Na.
Hỏi khi tiêu thụ 2,0 g bột ngọt, lượng sodium trong đó tương đương với bao nhiêu gam muối ăn (NaCl)? Cho khối lượng mol: H = 1, C = 12; N = 14; O = 16; Na = 23;; Cl = 35,5.
-
A.
0,692 gam.
-
B.
0,136 gam.
-
C.
0,346 gam.
-
D.
0,272 gam.
Đáp án : A
Tính số mol bột ngọt từ đo tính lượng muối tương đương.
n bột ngọt = 2 : 169 = \(\frac{2}{{169}}mol\)→ n Na+ = \(\frac{2}{{169}}mol\) → m NaCl = \(\frac{2}{{169}}.58,5 = 0,692\)gam
Đáp án A
Phương pháp Solvay là phương pháp phổ biến nhất hiện nay để sản xuất Na2CO3. Hình dưới. Phương trình hóa học nào sau đây không có trong phương pháp Solvay?

-
A.
NaCl + NH₃ + H₂O + CO₂ → NH₄Cl + NaHCO₃
-
B.
NH3 + 2HCl → NH4Cl
-
C.
CaCO₃ → CaO + CO₂
-
D.
2NaHCO3 → Na2CO3 + CO2 + H2O
Đáp án : B
Dựa vào phương pháp Solvay.
B sai, do NH4Cl được tạo ra khi NH4HCO3 tác dụng với NaCl.
Đáp án B
Tiến hành các thí nghiệm sau:
(a) Điện phân MgCl2 nóng chảy.
(b) Nhiệt phân hoàn toàn BaCO3.
(c) Cho kim loại K vào dung dịch CuSO4 dư.
(d) Dẫn khí CO dư đi qua bột Fe2O3 nung nóng.
(e) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3 dư.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được kim loại là
-
A.
4
-
B.
2
-
C.
5
-
D.
3
Đáp án : D
Dựa vào tính chất hoá học của kim loại.
(a) MgCl2 → Mg + Cl2
(b) BaCO3 → BaO + CO2
(c) K + H2O → KOH + ½ H2
2KOH + CuSO4 → Cu(OH)2 + K2SO4
(d) 3CO + Fe2O3 → 2Fe + 3CO2
(e) Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag
Đáp án D
Nguyên tố X thuộc chu kì 3, nhóm IIA. Cấu hình electron nguyên tử của X là
-
A.
1s22s22p1.
-
B.
1s22s22p63s2.
-
C.
1s22s22p63s23p2.
-
D.
1s22s22p63s1.
Đáp án : B
Dựa vào vị trí của X trong bảng tuần hoàn.
Cấu hình electron nguyên tử của X là 1s22s22p63s2.
Đáp án B
Cho cấu hình electron 26Fe là [Ar]3d64s2. Cấu hình electron nào sau đây là của ion Fe3+
-
A.
[Ar]3d6.
-
B.
[Ar]3d44s2.
-
C.
[Ar]3d54s1.
-
D.
[Ar]3d5.
Đáp án : D
Dựa vào cấu hình của Fe.
Cấu hình electron nào sau đây là của ion Fe3+ là [Ar]3d5.
Đáp án D
Cho dung dịch HCl vào dung dịch chất X, thu được khí không màu, nặng hơn không khí, mùi sốc. Chất X là
-
A.
NaOH.
-
B.
NaHCO3.
-
C.
NaHSO3.
-
D.
NaCl.
Đáp án : C
Dựa vào mùi của khí để xác định hợp chất X.
Vì khi chất X tác dụng với HCl thu được khí không màu, nặng hơn không khí, mùi sốc nên X là NaHSO3.
Đáp án C
Ở một số quốc gia, khoáng vật trona là nguyên liệu chính để sản xuất soda. Thành phần hóa học chính của khoáng vật trona là
-
A.
Na2CO3.NaHCO3.2H2O.
-
B.
3NaF.AlF3.
-
C.
NaNO3.
-
D.
NaCl.KCl.
Đáp án : A
Dựa vào kim loại trong tự nhiên.
Khoáng vật trona có thành phần chính là Na2CO3.NaHCO3.2H2O
Đáp án A
Cho các phát biểu sau
1. Nước cứng là nước chứa nhiều cation Ca2+ và Mg2+.
2. Nguyên tố calcium có nhiều trong sữa, ngũ cốc, các loại hạt, rau cải, hải sản,…
3. Nguyên tố nhóm IA tồn tại trong tự nhiên dưới dạng đơn chất.
4. Hợp kim Mg – Al được dùng để chế tạo các bộ phận của máy bay, ô tô,…
Số phát biểu đúng là
-
A.
1
-
B.
2
-
C.
3
-
D.
4
Đáp án : C
Dựa vào ứng dụng của hợp chất nhóm IIA.
1. đúng
2. đúng
3. sai, nguyên tố nhóm IA tồn tại dưới dạng hợp chất.
4. đúng
Đáp án C
Cho các phát biểu sau:
a. Phức chất [CoCl2(NH3)4]+ có dạng hình học bát diện.
b. Phức chất [CoCl2(NH3)4]+ có điện tích +3, nguyên tử trung tâm là Co phối tử là Cl và NH3.
c. Trong công thức của phức chất [CoCl2(NH3)4]Cl, [CoCl2(NH3)4]+ là cầu nội, Cl- là cầu ngoại.
d. Vitamin B12 là phức chất của [CoCl2(NH3)4]+ có vai trò thiết yếu trong việc hình thành tế bào hồng cầu, chuyển hoá tế bào, chức năng thần kinh và sản xuất DNA.
Số phát biểu đúng là
-
A.
3
-
B.
2
-
C.
1
-
D.
4
Đáp án : B
Dựa vào ứng dụng của phức chất.
a. đúng
b. sai, phức chất có điện tích +1.
c. đúng
d. sai, vitamin B12 không có vai trò hình thành tế bào hồng cầu.
đáp án B
Thực hiện các thí nghiệm sau:
(a) Cho Na vào H2O.
(b) Cho bột Mg dư vào dung dịch FeCl3.
(c) Cho Al vào dung dịch AgNO3.
(d) Cho Al vào dung dịch HCl.
(e) Cho Ag vào dung dịch H2SO4 loãng.
(g) Cho bột Fe dư vào dung dịch HNO3 đặc, nguội.
Số thí nghiệm xảy ra phản ứng là
-
A.
2
-
B.
3
-
C.
4
-
D.
5
Đáp án : C
Dựa vào tính chất hoá học của kim loại.
a. Na + H2O → NaOH + ½ H2
b. Mg + 2FeCl3 → MgCl2 + 2FeCl2
c. Al + 3AgNO3 → Al(NO3)3 + 3Ag
d. 2Al + 6HCl → 2AlCl3 + 3H2
e. không phản ứng
g. không phản ứng
đáp án C
Đốt cháy cation K+ngọn lửa có màu gì?
-
A.
Xanh da trời.
-
B.
Đỏ.
-
C.
Vàng.
-
D.
Tím hoa cà.
Đáp án : D
Dựa vào ngọn lửa đốt cháy hợp chất nhóm IA.
Đốt cháy cation K+ngọn lửa có màu tím
Đáp án D
Cho dãy các chất: MgCO3, CaCO3, SrCO3, BaCO3. Độ bền nhiệt của muối carbonate lớn nhất là
-
A.
MgCO3.
-
B.
CaCO3.
-
C.
SrCO3.
-
D.
BaCO3.
Đáp án : D
Dựa vào sự biến đổi của muối carbonate nhóm IIA.
BaCO3 có độ bền nhiệt lớn nhất do nhiệt độ phân huỷ lớn.
Đáp án D
Cho các phức chất có công thức sau: [Fe(OH2)6]2+, [PtCl2(NH3)2], [Cu(NH3)4] 2+, [Co(NH3)6]3+. Số phức chất mang điện tích và số phức chất không mang điện tích lần lượt là
-
A.
2 và 2
-
B.
3 và 1
-
C.
1 và 3
-
D.
4 và 0
Đáp án : B
Dựa vào điện tích của phức chất.
[Fe(OH2)6]2+, [Cu(NH3)4] 2+, [Co(NH3)6]3+ mang điện tích
[PtCl2(NH3)2] không mang điện tích
Đáp án B
Phức chất [Co(NH3)6]Cl3 có số phối trí là 6. Phức này có dạng hình học nào sau đây?
-
A.
Đường thẳng.
-
B.
Bát diện.
-
C.
Tứ diện.
-
D.
Lưỡng chóp tam giác
Đáp án : B
Dựa vào hình dạng của phức chất.
Phức chất trên có số phối trí là 6 nên có hình bát diện.
Đáp án B
Phức chất aqua có dạng bát diện khi cho copper (II) sulfate vào nước. Công thức của phức là
-
A.
Cu(H2O)6
-
B.
Cu(H2O)4
-
C.
[Cu(H2O)6] SO4
-
D.
[Cu(OH2)4] SO4
Đáp án : C
Dựa vào hình dạng của phức chất.
Phức chất aqua có dạng bát diện khi cho copper(II) sulfate vào nước nên công thức của phức là [Cu(H2O)6] SO4
Đáp án C
Phản ứng nào dưới đây không là phản ứng thay thế phối tử trong phức chất
-
A.
[Cr(OH2)6]3+ + 6OH- → [Cr(OH)6]3- + 6H2O
-
B.
[Ni(OH2)6]3+ + 6NH3 → [Cr(NH3)6]2+ + 6H2O
-
C.
Cu2+ + 6H2O → [Cu(H2O)6]2+
-
D.
[NiCl4]2- + 2NH3 → [NiCl2(NH3)2] + 2Cl-
Đáp án : C
Dựa vào phản ứng thay thế phổi tử trong phức chất.
C sai vì phản ứng C là phản ứng tạo phức
Quặng vàng (Gold) tồn tại trong tự nhiên thường có hàm lượng vàng thấp. Phương pháp tách vàng phù hợp hiện nay là phương pháp Cyanide. Theo phương pháp này, để thu hồi vàng từ quặng, người ta thường nghiền nhỏ quặng rồi hoà tan trong dung dịch KCN (potassium cyanide, rất độc) cùng với dòng không khí liên tục được thổi vào. Khi đó, vàng bị hoà tan tạo thành phức chất (các chất khác trong quặng không phản ứng với KCN):
4Au(s) + 8KCN(aq) + O2(g) + 2H2O(l) → 4K[Au(CN)2](aq) + 4KOH(aq) (1)
Tiếp theo cho bột kẽm đến dư vào dung dịch phức, thu được bột vàng (có lẫn một ít bột kẽm):
Zn(s) + 2K[Au(CN)2] (aq) → K2[Zn(CN)4] (aq)+ 2Au(s) (2)
a) Phương pháp tách vàng ở trên thân thiện với môi trường.
b) Phương pháp tách vàng ở trên là phương pháp thuỷ luyện.
c) Để loại bỏ Zn lẫn trong bột vàng, có thể dùng dung dịch HCl.
d) Để thu được 37,5 gam vàng cần 23,5 gam KCN (hiệu suất cả quá trình tách đạt 95%). Biết nguyên tử khối của C = 12; N = 14; K = 39; Au = 197.
a) Phương pháp tách vàng ở trên thân thiện với môi trường.
b) Phương pháp tách vàng ở trên là phương pháp thuỷ luyện.
c) Để loại bỏ Zn lẫn trong bột vàng, có thể dùng dung dịch HCl.
d) Để thu được 37,5 gam vàng cần 23,5 gam KCN (hiệu suất cả quá trình tách đạt 95%). Biết nguyên tử khối của C = 12; N = 14; K = 39; Au = 197.
a) sai, phương pháp trên không thân thiện với môi trường vì KCN rất độc
b) đúng
c) đúng
d) sai, cần 26 gam KCN.
Thép thường hay là thép carbon là hợp kim của Fe và C (≤ 2%), nguyên tố khác rất ít hoặc không có. Để xác định hàm lượng Fe trong một mẫu thép chứa Fe, C và Si người ta thực hiện các thí nghiệm sau:
- Cân 10,00 gam mẫu thép rồi cho vào 200mL dung dịch H2SO4 1M, đến khi phản ứng xảy ra hoàn toàn được 200,0mL dung dịch X.
-Lấy 10,0mL dung dịch X vào trong cốc thủy tinh, thêm tiếp dung dịch H2SO4 1M (dư) rồi chuẩn độ bằng dung dịch KMnO4 0,1M. Kết thúc chuẩn độ, thể tích (mL) dung dịch KMnO4 0,1M sử dụng qua 3 lần chuẩn độ như sau:

a) Vai trò của C trong thép là bảo vệ Fe không bị ăn mòn điện hóa.
b) Hàm lượng Fe trong thép là 98,0%.
c) Trong phản ứng chuẩn độ, chất khử là KMnO4.
d) Điểm tương đương (kết thúc chuẩn độ) là khi dung dịch trong cốc bắt đầu chuyển màu tím.
a) Vai trò của C trong thép là bảo vệ Fe không bị ăn mòn điện hóa.
b) Hàm lượng Fe trong thép là 98,0%.
c) Trong phản ứng chuẩn độ, chất khử là KMnO4.
d) Điểm tương đương (kết thúc chuẩn độ) là khi dung dịch trong cốc bắt đầu chuyển màu tím.
Dựa vào phương pháp chuẩn độ iron(II).
a) Sai, vai trò của C là tạo hợp kim với Fe
b) đúng
c) sai, chất oxi hoá là KMnO4.
d) đúng.
Những phát biểu nào sau đây về phức chất bát diện [Cu(OH2)6]2+ là đúng?
a. Nguyên tử trung tâm được hình thành từ quá trình cation Cu2+ sử dụng 6 orbital trống để nhận các cặp electron hoá trị riêng của các phân tử H2O
b. Số oxi hoá của nguyên tử trung tâm là +2.
c. Số liên kết cho - nhận giữa phối tử và nguyên tử trung tâm cũng là hoá trị phổ biến của đồng.
d. Mỗi phân tử nước chỉ sử dụng 1 trong 2 cặp electron hoá trị riêng của nó để tạo liên kết cho - nhận với cation Cu2+.
a. Nguyên tử trung tâm được hình thành từ quá trình cation Cu2+ sử dụng 6 orbital trống để nhận các cặp electron hoá trị riêng của các phân tử H2O
b. Số oxi hoá của nguyên tử trung tâm là +2.
c. Số liên kết cho - nhận giữa phối tử và nguyên tử trung tâm cũng là hoá trị phổ biến của đồng.
d. Mỗi phân tử nước chỉ sử dụng 1 trong 2 cặp electron hoá trị riêng của nó để tạo liên kết cho - nhận với cation Cu2+.
Dựa vào công thức của phức chất.
a. sai, nguyên tử Cu sử dụng 3 orbital trống để nhận các cặp electron hoá trị riêng của các phân tử H2O.
b. đúng
c. sai, hoá trị phổ biến của đồng là 2.
d. đúng
Hòa tan hoàn toàn x gam kim loại R trong m gam dung dịch H2SO4 đặc, nóng, vừa đủ. Sau khi phản ứng xảy ra hoàn toàn, thu được 2,479 lít SO2 (sản phẩm khử duy nhất, ở đkc) và m gam dung dịch chỉ chứa muối.
a. Trong phản ứng trên, H2SO4 là chất bị oxi hóa.
b. R là kim loại chuyển tiếp dãy thứ nhất.
c. Trong muối thu được, R có số oxi hóa +2.
d. Giá trị của x lớn hơn 5,6.
a. Trong phản ứng trên, H2SO4 là chất bị oxi hóa.
b. R là kim loại chuyển tiếp dãy thứ nhất.
c. Trong muối thu được, R có số oxi hóa +2.
d. Giá trị của x lớn hơn 5,6.
Tính số mol SO2 từ đố xác định kim loại R.
n SO2 = 2,479 : 24,79 = 0,1 mol
n R = n SO2.
a. sai, H2SO4 là chất bị khử.
b. đúng
c. đúng
d. đúng vì bảo toàn khối lượng: m R + m H2SO4 = m muối + m SO2 + m H2O
Một nhà hóa học trẻ quyết định nghiên cứu về sự nhiệt phân muối cobalt(II) sulfate pentahydrate (CoSO4.5H2O) để phục vụ cho dự án khoa học của mình. Để tiến hành, anh ta đặt một mẫu muối màu hồng tươi vào thiết bị phân tích nhiệt trọng (TGA) và bắt đầu quá trình đun nóng đến 950°C. Kết quả là anh ta nhận được đồ thị về sự phụ thuộc của khối lượng mẫu vào nhiệt độ như trong hình sau:

Số nguyên tử trong một phân tử mẫu ở 220oC là bao nhiêu?
Dựa vào đồ thị ta thấy được khối lượng mẫu ban đầu giảm là do phân tử H2O bị tách ra.
Tại 220oC, có 70,6% mẫu => %m H2O bị tách ra = 100 – 70,6 = 29,4%
Gọi công thức của mẫu còn lại là CoSO4.xH2O = \(\frac{{x.18}}{{59 + 96 + x.18}}.100 = 29,4\% \to x \approx 4\)
Vậy số nguyên tử trong một phân tử mẫu ở 220oC là: 1 + 1 + 4 + 4.2 + 4 = 18.
Cho một mẫu hợp kim Na–Ba tác dụng với nước (dư), thu được dung dịch X và 3,7185 lít khí H2 (ở đkc). Để trung hòa dung dịch X cần dùng V mL dung dịch acid H2SO4 2M. Xác định giá trị của V?
Dựa vào tính chất hoá học của kimm loại tác dụng với nước.
n H2 = 3,7185 : 24,79 = 0,15 mol
Na + H2O → NaOH + ½ H2
Ba + H2O → Ba(OH)2 + H2
Nhận xét: n OH- = 2.nH2 = 0,15.2 = 0,3 mol
n H+ = V.2.2 = 4V
OH- + H+ → H2O
0,3 4V
Ta có: 0,3 = 4V → V = 0,075L = 75 mL
Đáp án 75
Một vết nứt đường ray tàu hỏa có thể thể tích 8,96 cm3. Người ta dùng hỗn hợp Tecmit (Al và Fe2O3 theo tỉ lệ mol tương ứng 2:1) để hàn vết nứt trên. Biết lượng Fe cần hàn cho vết nứt bằng 79% lượng Fe sinh ra trong phản ứng nhiệt nhôm và giả thiết chỉ xảy ra phản ứng khử Fe2O3 thành Fe với hiệu suất 96%. Khối lượng riêng của sắt 7,9 g/cm3. Khối lượng của hỗn hợp Tecmit tối thiểu cần dùng trong quá trình trên trên là bao nhiêu gam? (Làm tròn kết quả đến hàng đơn vị).
Viết phản ứng nhiệt nhôm, tính số mol của Fe.
Phản ứng: 2Al + Fe2O3 → Al2O3 + 2Fe
- Khối lượng Fe đủ để hàn vết nứt là: mFe = 8,96.7,9= 70,784 gam → nFe = 1,264 (mol)
→ mhh = (27.1,264 + 160.1,264/2)/(96%.79%) = 178,3 (gam)
Đáp án 178
Cho từ từ K (potassium) dư vào các dung dịch các chất sau : CuSO4, NH4Cl, NaHCO3, Ba(HCO3)2, Al(NO3)3, FeCl2, ZnSO4. Có bao nhiêu trường hợp vừa có khí thoát ra vừa có kết tủa sau khi phản ứng kết thúc?
Dựa vào tính chất hoá học của nguyên tố nhóm IA.
K là kim loại mạnh sẽ tác dụng với nước ở điều kiện thường tạo dung dịch KOH.
K + H2O → KOH + ½ H2
KOH + CuSO4 → K2SO4 + Cu(OH)2
2KOH + Ba(HCO3)2 → BaCO3 + K2CO3 + 2H2O
2KOH + FeCl2 → Fe(OH)2 + 2KCl
Có 3 phản ứng vừa có kết tủa vừa có chất khí.
Đáp án 3
Nhiệt phân hoàn toàn 40g một loại quặng dolomite có lẫn tạp chất trơ sinh ra 9,916 lít khí CO2 (điều kiện chuẩn). Thành phần phần trăm về khối lượng của CaCO3.MgCO3 trong loại quặng nêu trên là bao nhiêu?
Tính số mol CO2 từ đó tính số mol CaCO3.MgCO3.
n CO2 = 9,916 : 24,79 = 0,4 mol
2.n CaCO3.MgCO3 = n CO2 => n CaCO3.MgCO3 = 0,2 mol
m CaCO3.MgCO3 = 0,2.184 = 36,8g
%CaCO3.MgCO3 = \(\frac{{36,8}}{{40}}.100\% = 92\% \)
Cho các ứng dụng: (1) nguyên liệu sản xuất thủy tinh; (2) sản xuất sodium; (3) tẩy vết dầu mỡ trước khi mạ điện, sơn, hàn; (4) tách ion Fe3+ để xử lí nước phèn; (5) làm mềm nước cứng. Có bao nhiêu ứng dụng là của sodium carbonate?
Dựa vào ứng dụng của hợp chất nhóm IA.
(1), (3), (5) là các ứng dụng của sodium carbonate (soda).
Các rạn san hô và đá vôi có thành phần chính là:
Cho phát biểu sau: “Phức chất đơn giản thường có một ...(1)...
Trong mạng tinh thể kim loại, liên kết kim loại được hình thành do
Nhiệt độ nóng chảy của các kim loại nhóm IA từ Li đến Cs biến đổi như thế nào?










Danh sách bình luận