Đề tham khảo thi THPT môn Hóa - Đề số 4 (hay, chi tiết)
Hợp chất nào sau đây là ester ?
Đề bài
Hợp chất nào sau đây là ester ?
-
A.
CH3CH2Cl.
-
B.
HCOOC6H5.
-
C.
CH3CH2NH2.
-
D.
HCOOH.
Hợp chất carbohydrate luôn có nhóm chức nào?
-
A.
-CO-.
-
B.
-OH.
-
C.
-CHO.
-
D.
-COOH.
Trong các chất dưới đây, chất nào là amine bậc hai?
-
A.
H2N[CH2]6NH2.
-
B.
(CH3)2CHNH2.
-
C.
CH3NHCH3.
-
D.
C6H5NH2.
Polymer nào sau đây thuộc loại polymer tổng hợp?
-
A.
Tinh bột.
-
B.
Tơ tằm.
-
C.
Polyethylene.
-
D.
Cao su thiên nhiên.
Giá trị thế điện cực chuẩn của cặp oxi hoá - khử nào được quy ước bằng 0 V?
-
A.
Na+/Na.
-
B.
2H+/H2.
-
C.
A13+/A1.
-
D.
Cl2/2Cl-
Trong công nghiệp, Mg được điều chế bằng cách nào dưới đây?
-
A.
Điện phân nóng chảy MgCl2.
-
B.
Cho kim loại Fe vào dung dịch MgCl2.
-
C.
Điện phân dung dịch MgSO4.
-
D.
Cho kim loại K vào dung dịch Mg(NO3)2
Để tạo màu cho pháo hoa, người ta dùng một số muối hay oxide kim loại, trong đó có hợp chất kim loại nhóm IA, để tạo màu vàng thường người ta sẽ dùng muối nào?
-
A.
lithium cacbonate.
-
B.
sodium nitrate.
-
C.
sodium hydroxide.
-
D.
potassium hydroxide.
Phức chất [Fe(CN)6]3- có số phối trí là bao nhiêu?
-
A.
4
-
B.
6
-
C.
2
-
D.
8
Cho cân bằng sau trong bình kín:  Biết khi hạ nhiệt độ của bình thì màu nâu đỏ nhạt dần. Phản ứng thuận có:
Biết khi hạ nhiệt độ của bình thì màu nâu đỏ nhạt dần. Phản ứng thuận có:
-
A.
ΔH < 0, phản ứng toả nhiệt
-
B.
ΔH > 0, phản ứng toả nhiệt
-
C.
ΔH < 0, phản ứng thu nhiệt
-
D.
ΔH > 0, phản ứng thu nhiệt
Chất nào sau đây có đồng phân hình học ?
-
A.
\(C{H_3} - C \equiv C - C{H_3}.\)
-
B.
\(C{H_3} - CH = CH - C{H_3}.\)
-
C.
\(C{H_2}Cl - C{H_2}Cl.\)
-
D.
\(C{H_2} = CCl - C{H_3}.\)
Phát biểu nào sau đây sai?
-
A.
Ethyl acetate có công thức phân tử là C4H8O2.
-
B.
Phân tử methyl methacrylate có một liên kết π trong phân tử.
-
C.
Methyl acrylate có khả năng tham gia phản ứng cộng Br2 trong dung dịch.
-
D.
Ethyl formate có khả năng tham gia phản ứng tráng bạc.
Ở pH >10, đặt dung dịch alanine trong một điện trường. Khi đó: alanine sẽ
-
A.
di chuyển về phía cực âm của điện trường.
-
B.
di chuyển về phía cực dương của điện trường.
-
C.
không di chuyển dưới tác dụng của điện trường.
-
D.
chuyển hoàn toàn về dạng phân tử trung hoà.
Tiến hành các thí nghiệm sau
(1) Ngâm lá đồng trong dung dịch silver nitrate;
(2) Ngâm lá kẽm trong dung dịch HCl loãng;
(3) Ngâm lá nhôm trong dung dịch NaOH;
(4) Ngâm lá sắt được cuốn dây copper trong dung dịch HCl;
Số thí nghiệm xảy ra ăn mòn điện hóa là
-
A.
2
-
B.
1
-
C.
3
-
D.
4
Phát biểu nào sau đây về phức chất Na3[Co(NO2)6] là không đúng?
-
A.
Có liên kết cho — nhận và liên kết ion trong phân tử.
-
B.
Có anion [Co(NO2)6]3- cũng là một phức chất.
-
C.
Có nguyên tử trung tâm là sodium và cobalt.
-
D.
Nguyên từ trung tâm có số oxi hoá là +3.
Cho phản ứng sau: CHºCH(g) + 2H2(g) → CH3-CH3.
Biết năng lượng liên kết trong bảng sau:
|
Liên kết |
H – H |
C – C |
C – H |
C º C |
|
Eb |
436 |
347 |
414 |
839 |
Biến thiên enthalpy của phản ứng là
-
A.
+292 kJ.
-
B.
+192 kJ.
-
C.
-292 kJ.
-
D.
-192 kJ.
Phản ứng chuyển hóa hydrogen sulfide trong khí thiên nhiên thành sulfur được thực hiện Theo sơ đồ phản ứng: H2S + SO2 → S + H2O
Khối lượng sulfur tối đa tạo ra khi chuyển hóa 1000m3 khí thiên nhiên (đkc) (chứa 5mgH2S/m3) là
-
A.
10,0g.
-
B.
5,0g.
-
C.
7,06g.
-
D.
100,0g.
. Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá – khử sau:
|
Cặp oxi hoá – khử |
Cu2+/Cu |
Zn2+/Zn |
Fe2+/Fe |
Ni2+/Ni |
2H+/H2 |
|
Thế điện cực chuẩn (V) |
0,340 |
–0,763 |
–0,440 |
–0,257 |
0 |
Số kim loại trong dãy các kim loại Zn, Ni, Fe, Cu phản ứng được với dung dịch HCl ở điều kiện chuẩn là
-
A.
3
-
B.
4
-
C.
1
-
D.
2
Cho sơ đồ:
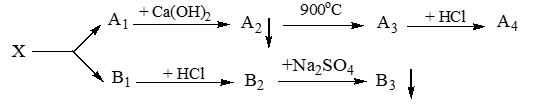
Các chất X, A2, A3, A4, B1, B2, B3 là các hợp chất của kim loại kiềm thổ. Chất B3 được dùng làm chất cản quang trong y tế.
Cho các phát biểu sau:
(a) Chất X là barium carbonate.
(b) Chất A2 là thành phần chính của núi đá vôi, các rặn san hô.
(c) Chất A1 và khí methane là các nguyên nhân chủ yếu gây hiệu ứng nhà kính.
(d) Các chất A3 và B1 tác dụng mạnh với nước tạo dung dịch có tính kiềm.
(e) Từ A4 có thể điều chế trực tiếp A2 bằng một phản ứng hóa học.
(g) A1 tác dụng với A3 ở điều kiện thích hợp tạo A2.
Số phát biểu đúng là
-
A.
3
-
B.
4
-
C.
5
-
D.
6
Trong phòng thí nghiệm, ethyl acetate được điều chế từ acetic acid và ethanol, xúc tác H2SO4 đặc, theo mô hình thí nghiệm sau:
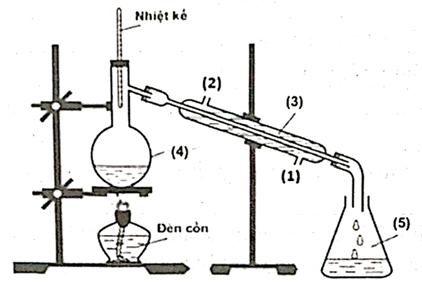
Biết nhiệt độ trong bình cầu (4) giữ ở mức 65-70oC, nhiệt độ trong ống sinh hàn (3) duy trì ở 25oC.
Sau thí nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của acetic acid, ethanol và ethyl acetate. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau:
|
Liên kết |
O-H (alcohol) |
O-H (carboxylic acid) |
C=O (ester, carboxylic acid) |
|
Số sóng (cm-1) |
3650-3200 |
3300-2500 |
1780-1650 |
a) Chất lỏng trong bình hứng (5) có ethyl acetate.
b) Vai trò của ống sinh hàn (3) để ngưng tụ hơi; nước vào từ (1), nước ra ở (2).
c) Nhiệt độ phản ứng ở bình cầu (4) càng cao thì phản ứng điều chế ethyl acetate xảy ra càng nhanh.
d) Dựa vào phổ hồng ngoại, phân biệt được acetic acid, ethanol và ethyl acetate.
Cho hai chất hữu cơ mạch hở X, Y có cùng công thức đơn giản nhất là . Các chất tham gia phản ứng theo đúng tỉ lệ mol trong các phương trình dưới đây:

Biết: là các chất hữu cơ trong đó đa chức và . Có các nhận định sau:
a) Y là hợp chất hữu cơ tạp chức.
b) Y3 khi tác dụng với dung dịch silver nitrate trong ammonia thu được tủa silver.
c) Đốt cháy thu được số mol carbon dioxide lớn hơn số mol nước.
d) Cho 4,4 g X2 tác dụng hoàn toàn với thuốc thử Tollens thu được 18g silver thì hiệu suất phản ứng đạt 85%.
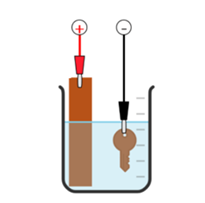
a) Trong quá trình điện phân, thanh kim loại đóng vai trò là cathode, chiếc chìa khóa đóng vai trò là anode và dung dịch điện phân là dung dịch CuSO4.
b) Nếu sử dụng dòng điện xoay chiều vẫn mạ được đồng lên chìa khóa .
c) Độ dày của lớp mạ tỉ lệ thuận với cường độ dòng điện chạy qua dung dịch điện phân và thời gian mạ.
d) Điện phân 200 ml dung dịch CuSO4 với điện cực trơ bằng dòng điện một chiều I = 9,65 A. Khi thể tích khí thoát ra ở cả hai điện cực đều là 1,24 lít (đkc) thì dừng điện phân. Khối lượng kim loại sinh ra bám vào cathode và thời gian điện phân là 3,2g và 2000s.
Năm 1965, trong quá trình tổng hợp thuốc chống loét dạ dày, nhà hóa học James M. Schlatter (Mỹ) đã vô tình phát hiện hợp chất X (một chất ngọt nhân tạo với tên thường gọi là “Aspartame”) có cấu tạo như hình dưới:
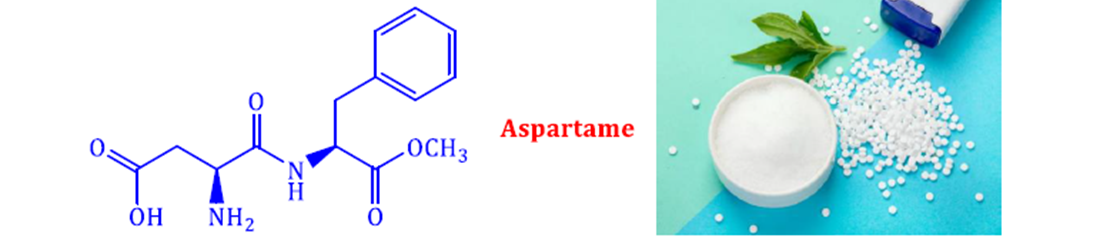
Aspartame ngọt hơn khoảng 200 lần so với đường ăn thông thường. Aspartame thường được sử dụng trong đồ uống và thực phẩm dành cho người ăn kiêng vì có ít calo hơn đường thông thường. Tổ chức Y tế thế giới (WHO) thông báo xếp chất làm ngọt nhân tạo aspartame vào danh sách các chất "có thể gây ung thư cho con người"
nhưng lưu ý chất này vẫn an toàn nếu được tiêu thụ trong giới hạn khuyến nghị hằng ngày. Hướng dẫn của WHO đã không thay đổi kể từ năm 1981: tối đa 40 miligam aspartame/mỗi kg trọng lượng cơ thể/ngày. Các khuyến nghị của Mỹ "hào phóng" hơn một chút: Vào năm 1983, FDA (Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ) đưa ra mức 50 miligam/mỗi kg trọng lượng cơ thể/ngày. Hiệp hội Đồ uống Mỹ cho biết soda dành cho người ăn kiêng thường chứa trung bình 100 miligam aspartame mỗi lon.
a) Phần trăm khối lượng của nguyên tố oxygen trong aspartame khoảng 27,21%.
b) X là hợp chất hữu cơ tạp chức.
c) 1 mol X tác dụng tối đa với 4 mol NaOH.
d) Số lon soda mà một người nặng trung bình ở Mỹ là 83kg nên uống theo khuyến nghị về lượng aspartame giới hạn hằng ngày của WHO và FDA hơn kém nhau khoảng 10 lon.
Cho các hiện tượng nổ sau : (a) Nổ cốc thí nghiệm khi cho lượng sodium quá lớn vào cốc thủy tính chứa nước, (b) nổ nồi hơi, (c) nổ thuốc súng (potassium, carbon và sulfur), (d) nổ bình khí nén, (e) nổ đường ống dẫn khí, (f) nổ thuốc nổ TNT (trinitrotoluene), (g) nổ khoang tàu chứa dầu đã hút cạn dầu. Số hiện tượng nổ hóa học là ?
Đáp án:
Cho các phản ứng sau
(a) Poly(vinyl acetate) bị thủy phân trong môi trường kiềm thu được poly(vinyl alcohol).
(b) Polyisoprene tham gia phản ứng cộng với hydrogen chloride.
(c) Nhiệt phân polystyrene thu được styrene.
(d) Thủy phân cellulose trong môi trường acid thu được glucose.
(e) Quá trình lưu hóa cao su xảy ra khi đun nóng cao su với sulfur.
(f) Thủy phân tơ capron khi đun nóng có mặt chất xúc tác thu được 6-aminohexanoic acid.
Số phản ứng giữ nguyên mạch polymer là bao nhiêu?
Đáp án:
Dung dịch glucose (C6H12O6) 5%, có khối lượng riêng là 1,02 g/mL, phản ứng oxi hoá 1 mol glucose tạo thành CO2 (g) và H2O(l) tỏa ra nhiệt lượng là 2 803,0 kJ. Một người bệnh được truyền một chai chứa 500 mL dung dịch glucose 5%. Tính năng lượng tối đa từ phản ứng oxi hoá hoàn toàn glucose mà bệnh nhân đó có thể nhận được? (Làm tròn đến phần nguyên)
Đáp án:
Cho các chất: methylamine, glycine, alanine, acetic acid, glutamic acid. Có bao nhiêu chất phản ứng với dung dịch HCl tạo muối?
Đáp án:
Quặng sắt là các khoáng vật chứa các hợp chất của sắt mà chủ yếu ở dạng các oxide. Hematite là một loại quặng chứa hàm lượng sắt cao và được dùng để trực tiếp sản xuất gang bằng cách nạp thẳng vào lò cao. Giả thiết 90% sắt trong quặng được chuyển vào gang. Từ 1 000 tấn quặng hematite (có hàm lượng 69,9% Fe) có thể sản xuất được bao nhiêu tấn gang loại 96% Fe? (Làm tròn kết quả đến phần nguyên)
Đáp án:
Hoà tan 1,61 g FeCl3 vào 10 mL nước thu được dung dịch (I). Hoà tan 5,52g K2C2O4 vào 30 mL nước thu được dung dịch (II). Cho từ từ dung dịch (II) vào dung dịch (I) và khuấy liên tục. Sau một thời gian thêm ethanol vào dung dịch phản ứng thì xuất hiện tinh thể. Lọc, thu tinh thể sạch của phức chất có công thức là K3[FeC2O4]3H2O với khối lượng là 3,51g. Phương trình hoá học của phản ứng diễn ra là:
FeCl3+3K2C2O4 + 3H2O→ K3[Fe(C2O4)3]3H2O + 3KCI Hiệu suất của phản ứng hình thành phức chất trên là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
Đáp án:
Lời giải và đáp án
Hợp chất nào sau đây là ester ?
-
A.
CH3CH2Cl.
-
B.
HCOOC6H5.
-
C.
CH3CH2NH2.
-
D.
HCOOH.
Đáp án : B
Dựa vào cấu tạo của ester là RCOOR’.
HCOOC6H5 thuộc hợp chất ester.
Đáp án B.
Hợp chất carbohydrate luôn có nhóm chức nào?
-
A.
-CO-.
-
B.
-OH.
-
C.
-CHO.
-
D.
-COOH.
Đáp án : B
Dựa vào cấu tạo của carbohydrate.
Trong hợp chất carbohydrate luôn có nhóm chức – OH.
Đáp án B
Trong các chất dưới đây, chất nào là amine bậc hai?
-
A.
H2N[CH2]6NH2.
-
B.
(CH3)2CHNH2.
-
C.
CH3NHCH3.
-
D.
C6H5NH2.
Đáp án : C
Amine bậc hai có công thức tổng quát: RNHR’.
CH3NHCH3 là amine bậc hai.
Đáp án C
Polymer nào sau đây thuộc loại polymer tổng hợp?
-
A.
Tinh bột.
-
B.
Tơ tằm.
-
C.
Polyethylene.
-
D.
Cao su thiên nhiên.
Đáp án : C
Dựa vào phân loại polymer gồm polymer thiên nhiên và polymer tổng hợp.
Polyethylene thuộc loại polymer tổng hợp.
Đáp án C.
Giá trị thế điện cực chuẩn của cặp oxi hoá - khử nào được quy ước bằng 0 V?
-
A.
Na+/Na.
-
B.
2H+/H2.
-
C.
A13+/A1.
-
D.
Cl2/2Cl-
Đáp án : B
Dựa vào bảng giá trị thế điện cực của cặp oxi hóa – khử.
2H+/H2 có giá trị thế điện cực chuẩn bằng 0V.
Đáp án B
Trong công nghiệp, Mg được điều chế bằng cách nào dưới đây?
-
A.
Điện phân nóng chảy MgCl2.
-
B.
Cho kim loại Fe vào dung dịch MgCl2.
-
C.
Điện phân dung dịch MgSO4.
-
D.
Cho kim loại K vào dung dịch Mg(NO3)2
Đáp án : A
Dựa vào các phương pháp tách kim loại.
Mg là kim loại có tính khử mạnh nên được điều chế bằng phương pháp điện phân nóng chảy MgCl2.
Đáp án A.
Để tạo màu cho pháo hoa, người ta dùng một số muối hay oxide kim loại, trong đó có hợp chất kim loại nhóm IA, để tạo màu vàng thường người ta sẽ dùng muối nào?
-
A.
lithium cacbonate.
-
B.
sodium nitrate.
-
C.
sodium hydroxide.
-
D.
potassium hydroxide.
Đáp án : B
Dựa vào tính chất hóa học của kim loại nhóm IA.
Để tạo màu vàng, người ta sử dụng muối soidum nitrate vì ion Na+ khi cháy tạo ngọn lửa màu vàng.
Đáp án B
Phức chất [Fe(CN)6]3- có số phối trí là bao nhiêu?
-
A.
4
-
B.
6
-
C.
2
-
D.
8
Đáp án : B
Số phối trí là tổng liên kết xích ma giữa phối tử và nguyên tử trung tâm.
Phức chất [Fe(CN)6]3- có số phối trí là 6.
Đáp án B
Cho cân bằng sau trong bình kín:  Biết khi hạ nhiệt độ của bình thì màu nâu đỏ nhạt dần. Phản ứng thuận có:
Biết khi hạ nhiệt độ của bình thì màu nâu đỏ nhạt dần. Phản ứng thuận có:
-
A.
ΔH < 0, phản ứng toả nhiệt
-
B.
ΔH > 0, phản ứng toả nhiệt
-
C.
ΔH < 0, phản ứng thu nhiệt
-
D.
ΔH > 0, phản ứng thu nhiệt
Đáp án : A
Dựa vào thông tin khi hạ nhiệt độ của bình thì màu nâu đỏ nhạt dần.
Khi hạ nhiệt độ, màu nâu đỏ nhạt dần tức là NO2 chuyển dần sang N2O4, phản ứng xảy ra ở nhiệt độ bình thường, không cần cung cấp nhiệt nên ΔH < 0, phản ứng toả nhiệt.
Đáp án A
Chất nào sau đây có đồng phân hình học ?
-
A.
\(C{H_3} - C \equiv C - C{H_3}.\)
-
B.
\(C{H_3} - CH = CH - C{H_3}.\)
-
C.
\(C{H_2}Cl - C{H_2}Cl.\)
-
D.
\(C{H_2} = CCl - C{H_3}.\)
Đáp án : B
Điều kiện để có đồng phân hình học là:
- trong cấu tạo phân tử phải có 1 liên kết đôi.
- 2 nhóm thế liên kết với cùng 1 cacbon của nối đôi phải khác nhau.
\(C{H_3} - CH = CH - C{H_3}.\) có đồng phân hình học.
Phát biểu nào sau đây sai?
-
A.
Ethyl acetate có công thức phân tử là C4H8O2.
-
B.
Phân tử methyl methacrylate có một liên kết π trong phân tử.
-
C.
Methyl acrylate có khả năng tham gia phản ứng cộng Br2 trong dung dịch.
-
D.
Ethyl formate có khả năng tham gia phản ứng tráng bạc.
Đáp án : B
Dựa vào tính chất hóa học của ester.
B sai vì CTCT của methyl methacrylate CH2=CH – COOCH3 trong CTCT có 2π lần lượt trong liên kết C = O và C = C.
Ở pH >10, đặt dung dịch alanine trong một điện trường. Khi đó: alanine sẽ
-
A.
di chuyển về phía cực âm của điện trường.
-
B.
di chuyển về phía cực dương của điện trường.
-
C.
không di chuyển dưới tác dụng của điện trường.
-
D.
chuyển hoàn toàn về dạng phân tử trung hoà.
Đáp án : B
Dựa vào tính điện di của amino acid.
Ở pH >10 (môi trường base) alanine tồn tại ở dạng anion H2N – CH (CH3) – COO- nên khi đặt trong điện trường sẽ di chuyển về phía cực dương.
Đáp án B.
Tiến hành các thí nghiệm sau
(1) Ngâm lá đồng trong dung dịch silver nitrate;
(2) Ngâm lá kẽm trong dung dịch HCl loãng;
(3) Ngâm lá nhôm trong dung dịch NaOH;
(4) Ngâm lá sắt được cuốn dây copper trong dung dịch HCl;
Số thí nghiệm xảy ra ăn mòn điện hóa là
-
A.
2
-
B.
1
-
C.
3
-
D.
4
Đáp án : A
Điều kiện ăn mòn điện hóa:
+ 2 điện cực khác nhau về bản chất (KL-KL, KL-PK, hợp kim,...)
+ 2 điện cực nối trực tiếp hoăc gián tiếp với nhau bằng dây dẫn
+ 2 điện cực cùng nhúng vào dung dịch chất điện li.
(1) Ngâm lá đồng trong dung dịch silver nitrate; (ăn mòn điện hóa)
(2) Ngâm lá kẽm trong dung dịch HCl loãng; (ăn mòn hóa học)
(3) Ngâm lá nhôm trong dung dịch NaOH; (ăn mòn hóa học)
(4) Ngâm lá sắt được cuốn dây copper trong dung dịch HCl; (ăn mòn điện hóa)
Đáp án A
Phát biểu nào sau đây về phức chất Na3[Co(NO2)6] là không đúng?
-
A.
Có liên kết cho — nhận và liên kết ion trong phân tử.
-
B.
Có anion [Co(NO2)6]3- cũng là một phức chất.
-
C.
Có nguyên tử trung tâm là sodium và cobalt.
-
D.
Nguyên từ trung tâm có số oxi hoá là +3.
Đáp án : C
Dựa vào các khái niệm về phức chất.
C sai, vì nguyên tử trung tâm là Co3+
Đáp án C
Cho phản ứng sau: CHºCH(g) + 2H2(g) → CH3-CH3.
Biết năng lượng liên kết trong bảng sau:
|
Liên kết |
H – H |
C – C |
C – H |
C º C |
|
Eb |
436 |
347 |
414 |
839 |
Biến thiên enthalpy của phản ứng là
-
A.
+292 kJ.
-
B.
+192 kJ.
-
C.
-292 kJ.
-
D.
-192 kJ.
Đáp án : C
Dựa vào công thức tính biến thiên enthalpy phản ứng theo năng lượng liên kết.
∆H = 2E(C-H) + E(C≡C) + 2E(H-H) – 6E(C-H) – E(C-C)
∆H = (2.414) + 839 + (2.436) – (6.414) – 347 = -292 (kJ/mol) < 0
⇒ Phản ứng tỏa nhiệt.
Đáp án C
Phản ứng chuyển hóa hydrogen sulfide trong khí thiên nhiên thành sulfur được thực hiện Theo sơ đồ phản ứng: H2S + SO2 → S + H2O
Khối lượng sulfur tối đa tạo ra khi chuyển hóa 1000m3 khí thiên nhiên (đkc) (chứa 5mgH2S/m3) là
-
A.
10,0g.
-
B.
5,0g.
-
C.
7,06g.
-
D.
100,0g.
Đáp án : C
Dựa vào phản ứng hydrogen sulfide.
Cứ 1m3 khí thiên nhiên chứa 5mg H2S
=> 1000m3 khí thiên nhiên chứa 5000mg H2S = 5g H2S
nH2S =5:(1.2+32) = 5/34 (mol)
2H2S + SO2 → 3S + 2H2O
5/34 15/68 (mol)
mS = 15/68 .32 \( \approx \) 7,06 (g)
. Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá – khử sau:
|
Cặp oxi hoá – khử |
Cu2+/Cu |
Zn2+/Zn |
Fe2+/Fe |
Ni2+/Ni |
2H+/H2 |
|
Thế điện cực chuẩn (V) |
0,340 |
–0,763 |
–0,440 |
–0,257 |
0 |
Số kim loại trong dãy các kim loại Zn, Ni, Fe, Cu phản ứng được với dung dịch HCl ở điều kiện chuẩn là
-
A.
3
-
B.
4
-
C.
1
-
D.
2
Đáp án : A
Dựa vào ý nghĩa thế điện cực của kim loại.
Zn, Fe, Ni phản ứng được với dung dịch HCl
Đáp án A
Cho sơ đồ:
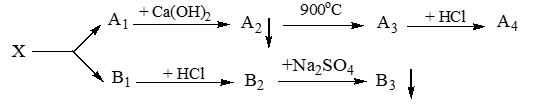
Các chất X, A2, A3, A4, B1, B2, B3 là các hợp chất của kim loại kiềm thổ. Chất B3 được dùng làm chất cản quang trong y tế.
Cho các phát biểu sau:
(a) Chất X là barium carbonate.
(b) Chất A2 là thành phần chính của núi đá vôi, các rặn san hô.
(c) Chất A1 và khí methane là các nguyên nhân chủ yếu gây hiệu ứng nhà kính.
(d) Các chất A3 và B1 tác dụng mạnh với nước tạo dung dịch có tính kiềm.
(e) Từ A4 có thể điều chế trực tiếp A2 bằng một phản ứng hóa học.
(g) A1 tác dụng với A3 ở điều kiện thích hợp tạo A2.
Số phát biểu đúng là
-
A.
3
-
B.
4
-
C.
5
-
D.
6
Đáp án : C
Chất B3 được dùng làm chất cản quang trong y tế nên B3 là BaSO4.
Từ đó dự đoán các chất còn lại
A: BaCO3 A1: CO2 A2: CaCO3 A3: CaO A4: CaCl2 B1: BaO B2: BaCl2
(a) Chất X là barium carbonate. (đúng)
(b) Chất A2 là thành phần chính của núi đá vôi, các rặn san hô.(đúng)
(c) Chất A1 và khí methane là các nguyên nhân chủ yếu gây hiệu ứng nhà kính.(đúng)
(d) Các chất A3 và B1 tác dụng mạnh với nước tạo dung dịch có tính kiềm.(đúng)
CaO + H2O → Ca(OH)2 BaO + H2O → Ba(OH)2
(e) Từ A4 có thể điều chế trực tiếp A2 bằng một phản ứng hóa học.(đúng)
CaCl2 + Na2CO3 → CaCO3 + 2NaCl
(g) A1 tác dụng với A3 ở điều kiện thích hợp tạo A2. (đúng)
CO2 + CaO → CaCO3
Đáp án C
Trong phòng thí nghiệm, ethyl acetate được điều chế từ acetic acid và ethanol, xúc tác H2SO4 đặc, theo mô hình thí nghiệm sau:

Biết nhiệt độ trong bình cầu (4) giữ ở mức 65-70oC, nhiệt độ trong ống sinh hàn (3) duy trì ở 25oC.
Sau thí nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của acetic acid, ethanol và ethyl acetate. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau:
|
Liên kết |
O-H (alcohol) |
O-H (carboxylic acid) |
C=O (ester, carboxylic acid) |
|
Số sóng (cm-1) |
3650-3200 |
3300-2500 |
1780-1650 |
a) Chất lỏng trong bình hứng (5) có ethyl acetate.
b) Vai trò của ống sinh hàn (3) để ngưng tụ hơi; nước vào từ (1), nước ra ở (2).
c) Nhiệt độ phản ứng ở bình cầu (4) càng cao thì phản ứng điều chế ethyl acetate xảy ra càng nhanh.
d) Dựa vào phổ hồng ngoại, phân biệt được acetic acid, ethanol và ethyl acetate.
a) Chất lỏng trong bình hứng (5) có ethyl acetate.
b) Vai trò của ống sinh hàn (3) để ngưng tụ hơi; nước vào từ (1), nước ra ở (2).
c) Nhiệt độ phản ứng ở bình cầu (4) càng cao thì phản ứng điều chế ethyl acetate xảy ra càng nhanh.
d) Dựa vào phổ hồng ngoại, phân biệt được acetic acid, ethanol và ethyl acetate.
Dựa vào sơ đồ điều chế ester.
a) Đúng
b) Đúng
c) Sai, vì khi nhiệt độ càng cao sẽ làm cho alcohol và acid bay hơi không tạo ra ester.
d) đúng
Cho hai chất hữu cơ mạch hở X, Y có cùng công thức đơn giản nhất là . Các chất tham gia phản ứng theo đúng tỉ lệ mol trong các phương trình dưới đây:

Biết: là các chất hữu cơ trong đó đa chức và . Có các nhận định sau:
a) Y là hợp chất hữu cơ tạp chức.
b) Y3 khi tác dụng với dung dịch silver nitrate trong ammonia thu được tủa silver.
c) Đốt cháy thu được số mol carbon dioxide lớn hơn số mol nước.
d) Cho 4,4 g X2 tác dụng hoàn toàn với thuốc thử Tollens thu được 18g silver thì hiệu suất phản ứng đạt 85%.
a) Y là hợp chất hữu cơ tạp chức.
b) Y3 khi tác dụng với dung dịch silver nitrate trong ammonia thu được tủa silver.
c) Đốt cháy thu được số mol carbon dioxide lớn hơn số mol nước.
d) Cho 4,4 g X2 tác dụng hoàn toàn với thuốc thử Tollens thu được 18g silver thì hiệu suất phản ứng đạt 85%.
Dựa vào tính chất hóa học của ester.
a) đúng vì hai chất hữu cơ mạch hở X, Y có cùng công thức đơn giản nhất là \({{\rm{C}}_3}{{\rm{H}}_4}{{\rm{O}}_2}\)và \({{\rm{M}}_{\rm{X}}} < {{\rm{M}}_{\rm{Y}}} < 146\)nên X là \({{\rm{C}}_3}{{\rm{H}}_4}{{\rm{O}}_2}\)và Y là \({{\rm{C}}_6}{{\rm{H}}_8}{{\rm{O}}_4}\).
Theo phản ứng (2) và các chất hữu cơ trong đó \({{\rm{Y}}_2}\) đa chức nên Y là \(CH \equiv C{\rm{ }}--{\rm{ }}COOC{H_2}CH\left( {OH} \right)C{H_2}\left( {OH} \right)\).
b) Sai vì Y1 là \(CH \equiv C{\rm{ }}--{\rm{ }}COONa\)
Y2 là \((OH)C{H_2}CH\left( {OH} \right)C{H_2}\left( {OH} \right)\)
Y3 là \(CH \equiv C{\rm{ }}--{\rm{ }}COOH\)
Y3 khi tác dụng với dung dịch silver nitrate trong ammonia thu được tủa vàng \(AgC \equiv C{\rm{ }}--{\rm{ }}COOH\).
c) sai Vì Y2 có CTPT là C3H8O2
C3H8O2 + 4O2 --> 3CO2 + 4H2O
d) sai, X là HCOOCH=CH2
X1 là HCOONa
X2 là CH3CHO
X3 là HCOOH
Vậy X2 tác dụng với Tollens cho 2 Ag
Hiệu suất phản ứng = 18 : ( 4,4 : 44.2.108) .100% = 83,33%
a) Trong quá trình điện phân, thanh kim loại đóng vai trò là cathode, chiếc chìa khóa đóng vai trò là anode và dung dịch điện phân là dung dịch CuSO4.
b) Nếu sử dụng dòng điện xoay chiều vẫn mạ được đồng lên chìa khóa .
c) Độ dày của lớp mạ tỉ lệ thuận với cường độ dòng điện chạy qua dung dịch điện phân và thời gian mạ.
d) Điện phân 200 ml dung dịch CuSO4 với điện cực trơ bằng dòng điện một chiều I = 9,65 A. Khi thể tích khí thoát ra ở cả hai điện cực đều là 1,24 lít (đkc) thì dừng điện phân. Khối lượng kim loại sinh ra bám vào cathode và thời gian điện phân là 3,2g và 2000s.
a) Trong quá trình điện phân, thanh kim loại đóng vai trò là cathode, chiếc chìa khóa đóng vai trò là anode và dung dịch điện phân là dung dịch CuSO4.
b) Nếu sử dụng dòng điện xoay chiều vẫn mạ được đồng lên chìa khóa .
c) Độ dày của lớp mạ tỉ lệ thuận với cường độ dòng điện chạy qua dung dịch điện phân và thời gian mạ.
d) Điện phân 200 ml dung dịch CuSO4 với điện cực trơ bằng dòng điện một chiều I = 9,65 A. Khi thể tích khí thoát ra ở cả hai điện cực đều là 1,24 lít (đkc) thì dừng điện phân. Khối lượng kim loại sinh ra bám vào cathode và thời gian điện phân là 3,2g và 2000s.
Dựa vào ứng dụng của điện phân.
a) sai vì thanh kim loại đóng vai trò là anode, chiếc thìa khóa đóng vai trò là cathode.
b) sai vì chỉ sử dụng được dòng điện 1 chiều trong điện phân.
c) đúng
d) đúng vì nH2 = nO2 = 0,05 mol nCu = x mol
Bảo toàn electron => 2nCu + 2nH2 = 4nO2 x = 0,05 mol
→ mCu = 3,2 gam ne = 4nO2 = 0,2 = It/F , t= 2000s
Năm 1965, trong quá trình tổng hợp thuốc chống loét dạ dày, nhà hóa học James M. Schlatter (Mỹ) đã vô tình phát hiện hợp chất X (một chất ngọt nhân tạo với tên thường gọi là “Aspartame”) có cấu tạo như hình dưới:

Aspartame ngọt hơn khoảng 200 lần so với đường ăn thông thường. Aspartame thường được sử dụng trong đồ uống và thực phẩm dành cho người ăn kiêng vì có ít calo hơn đường thông thường. Tổ chức Y tế thế giới (WHO) thông báo xếp chất làm ngọt nhân tạo aspartame vào danh sách các chất "có thể gây ung thư cho con người"
nhưng lưu ý chất này vẫn an toàn nếu được tiêu thụ trong giới hạn khuyến nghị hằng ngày. Hướng dẫn của WHO đã không thay đổi kể từ năm 1981: tối đa 40 miligam aspartame/mỗi kg trọng lượng cơ thể/ngày. Các khuyến nghị của Mỹ "hào phóng" hơn một chút: Vào năm 1983, FDA (Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ) đưa ra mức 50 miligam/mỗi kg trọng lượng cơ thể/ngày. Hiệp hội Đồ uống Mỹ cho biết soda dành cho người ăn kiêng thường chứa trung bình 100 miligam aspartame mỗi lon.
a) Phần trăm khối lượng của nguyên tố oxygen trong aspartame khoảng 27,21%.
b) X là hợp chất hữu cơ tạp chức.
c) 1 mol X tác dụng tối đa với 4 mol NaOH.
d) Số lon soda mà một người nặng trung bình ở Mỹ là 83kg nên uống theo khuyến nghị về lượng aspartame giới hạn hằng ngày của WHO và FDA hơn kém nhau khoảng 10 lon.
a) Phần trăm khối lượng của nguyên tố oxygen trong aspartame khoảng 27,21%.
b) X là hợp chất hữu cơ tạp chức.
c) 1 mol X tác dụng tối đa với 4 mol NaOH.
d) Số lon soda mà một người nặng trung bình ở Mỹ là 83kg nên uống theo khuyến nghị về lượng aspartame giới hạn hằng ngày của WHO và FDA hơn kém nhau khoảng 10 lon.
Dựa vào tính chất hóa học của amino acid.
a. đúng vì CTPT của aspartame C14H18N2O5 thì %O = (5.16) : (14.12+18.1+14.2+5.16) .100% = 27,21%
b. đúng vì CTCT của aspartame chứa các nhóm chức -COOH (carboxylic acid) , -NH2 (amino), - CO-NH- (peptide), -COO- (ester).
c. sai vì 1 mol X tác dụng tối đa với 3 mol NaOH.
d. sai Vì số lon theo khuyến cáo của WHO của người đó trong 1 ngày: 40.83:100=33 (lon)
Số lon theo khuyến cáo của FDA của người đó trong 1 ngày: 50.83:100= 41 (lon)
Số lon chênh lệch: 41 – 33 = 8 (lon)
Cho các hiện tượng nổ sau : (a) Nổ cốc thí nghiệm khi cho lượng sodium quá lớn vào cốc thủy tính chứa nước, (b) nổ nồi hơi, (c) nổ thuốc súng (potassium, carbon và sulfur), (d) nổ bình khí nén, (e) nổ đường ống dẫn khí, (f) nổ thuốc nổ TNT (trinitrotoluene), (g) nổ khoang tàu chứa dầu đã hút cạn dầu. Số hiện tượng nổ hóa học là ?
Đáp án:
Đáp án:
Dựa vào khái niệm về nổ hóa học: là hiện tượng cháy xảy ra với tốc độ nhanh làm hỗn hợp khí xung quanh giãn nở đột biến sinh công gây nổ. Khi có đủ 3 yếu tố nói trên thì sự cháy vẫn chưa xuất hiện được mà cần phải có 3 điều kiện nữa thì sự cháy mới có thể xuất hiện.
Hiện tượng nổ hóa học là : (a)Nổ cốc thí nghiệm khi cho lượng sodium quá lớn vào cốc thủy tính chứa nước, (c)nổ thuốc súng (potassium, carbon và sulfur), (f) nổ thuốc nổ TNT (trinitrotoluene),(g) nổ khoang tàu chứa dầu đã hút cạn dầu.
Đáp án 4.
Cho các phản ứng sau
(a) Poly(vinyl acetate) bị thủy phân trong môi trường kiềm thu được poly(vinyl alcohol).
(b) Polyisoprene tham gia phản ứng cộng với hydrogen chloride.
(c) Nhiệt phân polystyrene thu được styrene.
(d) Thủy phân cellulose trong môi trường acid thu được glucose.
(e) Quá trình lưu hóa cao su xảy ra khi đun nóng cao su với sulfur.
(f) Thủy phân tơ capron khi đun nóng có mặt chất xúc tác thu được 6-aminohexanoic acid.
Số phản ứng giữ nguyên mạch polymer là bao nhiêu?
Đáp án:
Đáp án:
phản ứng giữ nguyên mạch là phản ứng mà không làm thay đổi số mắt xích n của polime. Đây thông thường là các phản ứng thế nguyên tử H ở trong mạch polyme hay phản ứng cộng vao liên kết pi hoặc phản ứng ở nhóm chức không nằm trên trục chính của mạch polyme kiểu như phản ứng thủy phân poly vinyl acetate để tạo ra polyvinyl alcohol.
(a) và (b) là phẩn ứng giữ nguyên mạch polymer.
Đáp án 2
Dung dịch glucose (C6H12O6) 5%, có khối lượng riêng là 1,02 g/mL, phản ứng oxi hoá 1 mol glucose tạo thành CO2 (g) và H2O(l) tỏa ra nhiệt lượng là 2 803,0 kJ. Một người bệnh được truyền một chai chứa 500 mL dung dịch glucose 5%. Tính năng lượng tối đa từ phản ứng oxi hoá hoàn toàn glucose mà bệnh nhân đó có thể nhận được? (Làm tròn đến phần nguyên)
Đáp án:
Đáp án:
Dựa vào tính chất hóa học của glucose.
Chú ý phản ứng tỏa nhiệt nên \({\Delta _{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\) = - 2803,0 kJ/mol. mdd = V(mL).D(g/mL)
C% = \(\frac{{{{\rm{m}}_{{\rm{ct}}}}}}{{{{\rm{m}}_{{\rm{dd}}}}}}{\rm{.100\% }}\) => 5% = \(\frac{{180.{{\rm{n}}_{{\rm{glucose}}}}}}{{500.1,02}}{\rm{.100\% }}\) => nglucose = 0,14167 mol
Q = 2803,0. 0,14167 = 397,1(kJ)
Đáp án 397
Cho các chất: methylamine, glycine, alanine, acetic acid, glutamic acid. Có bao nhiêu chất phản ứng với dung dịch HCl tạo muối?
Đáp án:
Đáp án:
Dựa vào tính chất hóa học của amino acid và amine.
Methylamine, glycine, alanine, glutamic acid có phản ứng với HCl tạo muối.
Đáp án 4.
Quặng sắt là các khoáng vật chứa các hợp chất của sắt mà chủ yếu ở dạng các oxide. Hematite là một loại quặng chứa hàm lượng sắt cao và được dùng để trực tiếp sản xuất gang bằng cách nạp thẳng vào lò cao. Giả thiết 90% sắt trong quặng được chuyển vào gang. Từ 1 000 tấn quặng hematite (có hàm lượng 69,9% Fe) có thể sản xuất được bao nhiêu tấn gang loại 96% Fe? (Làm tròn kết quả đến phần nguyên)
Đáp án:
Đáp án:
Dựa vào quá trình sản xuất gang
Khối lượng Fe trong quặng: 1000.69,9% = 699 tấn
Khối lượng Fe chuyển vào trong gang là: 699.90% = 629,1 tấn
Số tấn gang loại 96% Fe là: 629,1 : 96% = 655 tấn
Hoà tan 1,61 g FeCl3 vào 10 mL nước thu được dung dịch (I). Hoà tan 5,52g K2C2O4 vào 30 mL nước thu được dung dịch (II). Cho từ từ dung dịch (II) vào dung dịch (I) và khuấy liên tục. Sau một thời gian thêm ethanol vào dung dịch phản ứng thì xuất hiện tinh thể. Lọc, thu tinh thể sạch của phức chất có công thức là K3[FeC2O4]3H2O với khối lượng là 3,51g. Phương trình hoá học của phản ứng diễn ra là:
FeCl3+3K2C2O4 + 3H2O→ K3[Fe(C2O4)3]3H2O + 3KCI Hiệu suất của phản ứng hình thành phức chất trên là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
Đáp án:
Đáp án:
Từ kết quả so sánh số mol FeCl3 và số mol của K2Cr2O7 chọn tính toán lí thuyết theo số
mol FeCl3. Số mol phức chất thu được theo lí thuyết bằng số mol FeCl3 và là:
1,61 : 162,5 = 9,9 . 10-3 (mol).
Khối lượng phức chất thu được theo lí thuyết là:
491 . 9,9. 10-3 = 4,86 (g).
Hiệu suất phản ứng là:
(3,51 : 4,86) . 100% = 72,2%.
Trong ăn mòn hóa học, phản ứng hóa học xảy ra là loại phản ứng nào sau đây?
Kim loại cứng nhất, thường được pha vào thép để tăng độ cứng và khả năng chống gỉ cho thép là
Phần I. Trắc nghiệm nhiều đáp án lựa chọn
Ở trạng thái cơ bản, cấu hình electron của nguyên tử Be (Z = 4) là
Quá trình tạo thành ion Ca2+ nào sau đây là đúng?
Kim loại X được sử dụng trong nhiệt kế, áp kế và một số thiết bị khác. Ở điều kiện thường, X là chất lỏng. Kim loại X là
Khi thay thế nhóm …(1) ở nhóm …(2) của carboxylic acid bằng nhóm
Phức chất đơn giản thường có một
Cho phản ứng oxi hóa – khử:
Các bài khác cùng chuyên mục









Danh sách bình luận