Lý thuyết Tính chất hóa học của muối
I.Tính chất hóa học của muối
I. Tính chất hóa học của muối
1. Tác dụng với kim loại → muối mới + kim loại mới
- Điều kiện: Kim loại mạnh hơn đẩy kim loại yếu hơn ra khỏi muối
Thí dụ:
Fe + CuSO4 → FeSO4 + Cu↓
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓
2. Tác dụng với axit → muối mới + axit mới
* Điều kiện xảy ra phản ứng: sản phẩm tạo thành phải có chất khí hoặc chất kết tủa hoặc nước
Thí dụ:
BaCl2 + H2SO4 → 2HCl + BaSO4↓
CaCO3 + 2HCl → CaCl2 + \(CO_2\)↑ + H2O
3. Tác dụng với dung dịch muối → 2 muối mới
* Điều kiện xảy ra phản ứng: sản phẩm tạo thành phải có chất khí hoặc chất kết tủa hoặc nước
Thí dụ:
AgNO3 + NaCl → NaNO3 + AgCl↓
4. Tác dụng với dung dịch bazơ → muối mới + bazơ mới
* Điều kiện xảy ra phản ứng: sản phẩm tạo thành phải có chất khí hoặc chất kết tủa hoặc nước
Thí dụ:
Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3↓
5. Phản ứng phân hủy muối
- Nhiều muối bị phân hủy ở nhiệt độ cao như: KClO3, KMnO4, CaCO3,…
Thí dụ:
2KClO3 \(\overset{t^{0}}{\rightarrow}\) 2KCl + 3O2
\(CaCO_3\) \(\overset{t^{0}}{\rightarrow}\) CaO + CO2
II. Phản ứng trao đổi trong dung dịch
1. Định nghĩa: Phản ứng trao đổi là phản ứng hóa học, trong đó hai hợp chất tham gia phản ứng trao đổi với nhau những thành phần cấu tạo của chúng để tạo ra những hợp chất mới.
2. Điều kiện xảy ra phản ứng trao đổi
Phản ứng trao đổi trong dung dịch của các chất chỉ xảy ra nếu sản phẩm tạo thành có chất không tan hoặc chất khí.
Thí dụ:
CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2↓
K2SO4 + NaOH: Phản ứng không xảy ra.
- Chú thích: phản ứng trung hòa cũng thuộc loại phản ứng trao đổi và luôn xảy ra.
Thí dụ:
H2SO4 + 2NaOH → Na2SO4 + 2H2O
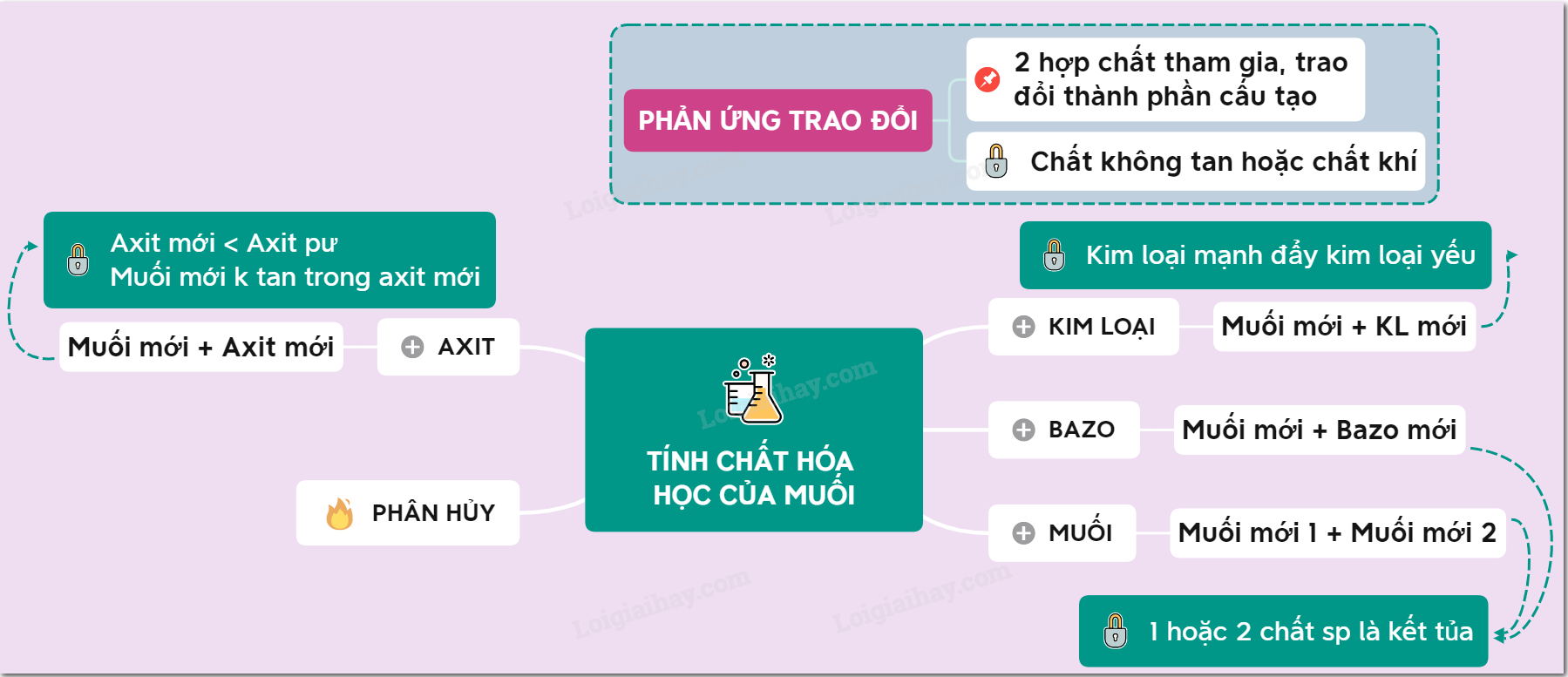
Sơ đồ tư duy: Tính chất hóa học của muối
Các bài khác cùng chuyên mục
- Đề số 9 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 8 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 7 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 6 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Phương pháp giải bài tập về độ rượu
- Đề số 9 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 8 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 7 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 6 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Phương pháp giải bài tập về độ rượu













Danh sách bình luận