1. Nguyên tử là gì?
Nguyên tử vô cùng nhỏ nhưng được tạo thành từ các hạt nhỏ hơn, trung hoà về điện.
2. Một số mô hình nguyên tử phổ biến thường gặp
|
Mô hình nguyên tử theo Ruther - Bo |
Thông tin cơ bản |
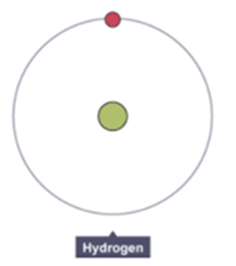 |
Hydrogen có 1 electron và 1 proton. Nguyên tử H không chứa neutron. Điện tích hạt nhân: +1 Số khối A = Z + N = 1 + 0 = 1 Khối lượng nguyên tử = m p = 1 amu |
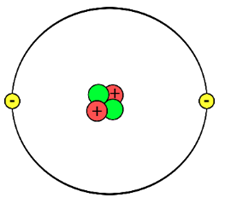 |
Helium có 2 electron; 2 proton và 2 neutron. Điện tích hạt nhân Z = +2 Số khối A = Z + N = 2 + 2 = 4 Khối lượng nguyên tử = 2.mp + 2.mn = 2.1 + 2.1 = 4 amu |
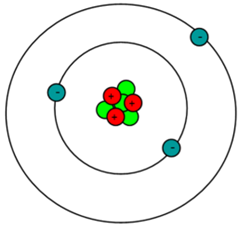 |
Lithium có 3 electron; 2 proton và 4 neutron. Điện tích hạt nhân Z = +3 Số khối A = Z + N = 3 + 4 = 7 Khối lượng nguyên tử = 3.mp + 4.mn = 3.1 + 4.1 = 7 amu |
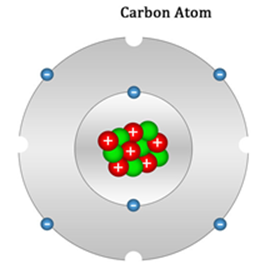 |
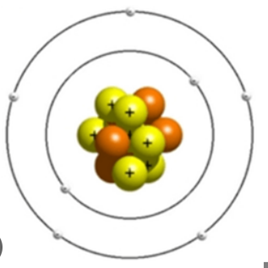
Carbon có 6 electron; 6 proton và 6 neutron Điện tích hạt nhân Z = +6 Số khối A = Z +N = 6 + 6 = 12 Khối lượng nguyên tử = 6.mp + 6.mn = 6.1 + 6.1 = 12 amu |
 |
Nitrogen có 7 electron; 7 proton và 7 neutron Điện tích hạt nhân Z = +7 Số khối A = Z +N = 7 + 7 = 14 Khối lượng nguyên tử = 7.mp + 7.mn = 7.1 + 7.1 = 14 amu |
 |
Oxygen có 8 electron; 8 proton và 8 neutron Điện tích hạt nhân Z = +8 Số khối A = Z + N = 8 + 8 = 16 Khối lượng nguyên tử = 8.mp + 8.mn = 8.1 + 8.1 = 16amu |
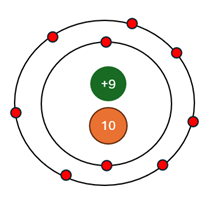 |
Fluorine có 9 electron; 9 proton và 10 neutron Điện tích hạt nhân Z = +9 Số khối A = Z + N = 9 + 10 = 19 Khối lượng nguyên tử = 9.mp + 10.mn = 9.1 + 10.1 = 19amu |
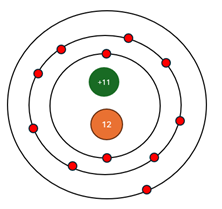 |
Sodium có 11 electron; 11 proton và 12 neutron Điện tích hạt nhân Z = +11 Số khối A = Z + N = 11 + 12 = 23 Khối lượng nguyên tử = 11.mp + 12.mn = 11.1 + 12.1 = 23 amu |
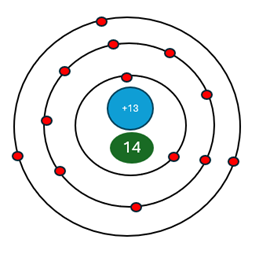 |
Aluminium có 13 electron; 13 proton và 14 neutron Điện tích hạt nhân Z = +13 Số khối A = Z + N = 13 + 14 = 27 Khối lượng nguyên tử = 13.mp + 14.mn = 13.1 + 14.1 = 27 amu |

 Cấu tạo nguyên tử - Từ điển Hoá 10
Cấu tạo nguyên tử - Từ điển Hoá 10 






Danh sách bình luận