 Giải bài tập hóa học 8, Hóa 8 - Để học tốt hóa học 8
Giải bài tập hóa học 8, Hóa 8 - Để học tốt hóa học 8
 ĐỀ KIỂM TRA HỌC KÌ 2 (ĐỀ THI HỌC KÌ 2) - HÓA HỌC 8
ĐỀ KIỂM TRA HỌC KÌ 2 (ĐỀ THI HỌC KÌ 2) - HÓA HỌC 8
Đề số 5 - Đề kiểm tra học kì II - Hóa học 8
Đề kiểm tra hết học kì II môn hóa lớp 8 có lời giải chi tiết
Đề bài
I. TRẮC NGHIỆM: (2,0 điểm)
Hãy chọn một trong các chữ cái A, B, C hoặc D trước phương án mà em cho là đúng nhất:
Câu 1 : Dãy chỉ gồm các oxit axit:
A. CO2, SO2, CuO, P2O5
B. CO2, SO3, Na2O, NO2
C. SO2, P2O5, CO2, SO3
D. H2O, CO, NO, Al2O3.
Câu 2 : Thành phần thể tích của không khí là:
A. 21% khí oxi, 78% khí nitơ, 1% các khí khác (CO2, CO, khí hiếm...)
B. 78% khí oxi, 21% khí nitơ, 1% các khí khác (CO2, CO, khí hiếm...)
C. 21% khí oxi, 78% các khí khác, 1% khí nitơ.
D. 1% khí oxi, 78% khí nitơ, 21% các khí khác.
Câu 3 : Nguyên liệu điều chế khí oxi trong phòng thí nghiệm:
A. CaCO3 B. Không khí
C. KMnO4 D. Nước
Câu 4 : Sự oxi hóa chậm là:
A. Sự oxi hóa có tỏa nhiệt mà không phát sáng.
B. Sự oxi hóa có tỏa nhiệt và phát sáng.
C. Sự oxi hóa có phát sáng.
D. Sự oxi hóa nhưng không tỏa nhiệt.
Câu 5 : Chất nào sau đây dùng làm nhiên liệu, không gây ô nhiễm môi trường:
A. Than B. Khí Hidro
C. Dầu hỏa D. Vỏ trấu
Câu 6 : Cặp chất nào sau đây phản ứng với nhau sinh ra khí hidro:
A. Zn và HCl B. Zn và O2
C. Zn và Cl2 D. Fe2O3 và H2
Câu 7 : Kim loại nào sau đây tan trong nước tạo ra dung dịch bazơ và khí hidro:
A. Fe B. Na
C. Pb D. Cu
Câu 8 : Độ tan của một chất trong nước ở nhiệt độ xác định là:
A. Số gam chất đó có thể tan trong 100g dung dịch.
B. Số gam chất đó có thể tan trong 100g nước.
C. Số gam chất đó có thể tan trong 100g dung môi để tạo thành dung dịch bão hòa.
D. Số gam chất đó có thể tan trong 100g nước để tạo thành dung dịch bão hòa.
II. TỰ LUẬN: (8,0 điểm)
Câu 9 : Cho các chất có công thức hóa học sau: K, MgO, Na2O, SO3.
a. Chất nào tác dụng được với nước?
b. Viết các phương trình hóa học xảy ra?
Câu 10 : Phân loại và gọi tên các hợp chất có công thức hóa học sau: Mg(OH)2, NaCl, H2SO4, Ca(HCO3)2.
Câu 11 : Oxi trong không khí là đơn chất hay hợp chất? Vì sao cá sống được trong nước? Những lĩnh vực hoạt động nào của con người cần thiết phải dùng bình nén oxi để hô hấp ?
Câu 12 : Cho 4,8 gam kim loại magie phản ứng hoàn toàn với dung dịch axit clohidric (HCl), sau phản ứng thu được muối magie clorua và khí Hidro
a. Viết phương trình hóa học xảy ra?
b. Tính thể tích khí Hidro sinh ra (ở đktc)?
c. Nếu đốt cháy toàn bộ lượng khí Hidro sinh ra ở trên trong không khí. Tính thể tích không khí cần dùng? (Biết Vkk = 5.VO2)
( Cho Mg =24 , O = 16 , H = 1 , Cl = 35,5)
Lời giải chi tiết
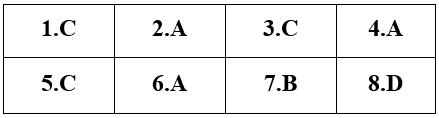
ĐÁP ÁN
HƯỚNG DẪN GIẢI CHI TIẾT
Câu 1:
Phương pháp: oxit axit là thường là oxit của phi kim và tương ứng với một axit
Mẹo nhận biết: oxit axit: thành phần chứa nguyên tố phi kim và oxi.
Oxit bazơ: thành phần chứa nguyên tố kim loại và oxi.
Hướng dẫn giải:
A. Loại CuO là oxit bazơ
B. Loại Na2O là oxit bazơ
C. Thỏa mãn tất cả cùng là oxit axit
D. Loại Al2O3 là oxit bazơ
Đáp án C
Câu 2:
Phương pháp: Dựa vào kết luận thành phần về không khí trong sgk hóa 8 – trang 96
Hướng dẫn giải:
Thành phần của không khí gồm: 21% khí oxi, 78% khí nitơ, 1% các khí khác (CO2, CO, khí hiếm...)
Đáp án A
Câu 3:
Phương pháp: Dựa vào kiến thức điều chế oxi trong PTN được học trong sgk hóa 8 – trang 92
Hướng dẫn giải:
Nguyên liệu để điều chế oxi trong PTN là các hợp chất giàu oxi và dễ phân hủy ở nhiệt độ cao như: KMnO4
Đáp án C
Câu 4:
Phương pháp: Dựa vào kiến thức học về sự oxi hóa chậm trong sgk hóa 8 trang 97
Hướng dẫn giải:
Sự oxi hóa chậm sự oxi hóa có tỏa nhiệt mà không phát sáng.
Đáp án A
Câu 5:
Hướng dẫn giải:
Than và vỏ trấu là nguyên liệu đốt cháy có thể gây ô nhiễm môi trường vì sinh ra khí độc hại như CO2 CO.
Dầu hỏa là nhiên liệu đốt cũng sinh ra các khí có thể gây ô nhiễm môi trường như CO2…
Khí hidro là nhiên liệu không gây ô nhiễm môi trường vì sinh ra H2O không ô nhiễm.
Đáp án B
Câu 6:
Phương pháp: Dựa vào kiến thức điều chế hidro trong phòng thí nghiệm sgk hóa 8- trang 114
Hướng dẫn giải:
Cặp chất phản ứng với nhau sinh ra khí H2 là Zn và HCl
PTHH: Zn + 2HCl → ZnCl2 + H2↑
Đáp án A
Câu 7:
Phương pháp: Dựa vào tính chất hóa học của nước trong sgk hóa 8 – trang 123
Hướng dẫn giải:
Na tan trong nước tạo ra dd bazơ và khí H2 theo PTHH sau:
2Na + 2H2O → 2NaOH (dd bazơ) + H2↑
Đáp án B
Câu 8:
Phương pháp: Dựa vào khái niệm độ tan của một chất trong nước trong sgk hóa 8 – trang 140
Hướng dẫn giải:
Độ tan của một chất trong nước ở nhiệt độ xác định là số gam chất đó có thể tan trong 100g nước để tạo thành dung dịch bão hòa.
Đáp án D
II. TỰ LUẬN: (8,0 điểm)
Câu 9:
Phương pháp: Dựa vào tính chất hóa học của nước trong sgk hóa 8 trang 123
Hướng dẫn giải:
a. Các chất tác dụng với nước là: K, Na2O, SO3
b. PTHH: 2K + 2H2O → 2KOH + H2↑
Na2O + H2O → 2NaOH
SO3 + H2O → H2SO4
Câu 10:
Phương pháp:
Phân loại các chất trên thành các loại muối, axit hoặc bazơ học trong sgk hóa 8 – trang 127
Tên axit có oxi
+ Axit có nhiều oxi: Tên axit = axit + tên phi kim + ic
+ Axit có ít oxi: Tên axit = axit + tên phi kim + ơ
- Tên ba zơ = tên kim loại (kèm hóa trị nếu kim loại có nhiều hóa trị) + hiđroxit
- Tên muối = tên kim loại (kèm hóa trị nếu kim loại có nhiều hóa trị) + tên gốc axit
Hướng dẫn giải:
Bazơ: Mg(OH)2 – magiê hi đroxit
Muối: NaCl – Natri clorua
Ca(HCO3)2 – Canxi hiđrocacbonat
Axit: H2SO4 – axit sunfuric
Câu 11:
Phương pháp: Dựa vào khái niệm đơn chất, hợp chất sgk hóa 8 – trang 22
Dựa vào ứng dụng của oxi trong sgk hóa 8 – trang 85
Hướng dẫn giải:
- Oxi trong không khí là đơn chất, vì oxi có công thức hóa học là O2 chỉ được tạo nên từ một nguyên tố hóa học.
- Cá sống được trong nước vì một lượng oxi có trong không khí tan vào trong nước, cá lấy lượng oxi có trong nước để hô hấp nhờ đó cá sống được.
- Những lĩnh vực hoạt động của con người cần thiết phải dùng bình nén oxi để hô hấp là:
+ Lĩnh vực hàng không: những phi công (phải bay cao, nơi thiếu nhiều khí oxi và không khí quá loãng)
+ Thợ lặn (thợ lặn dưới nước thiếu oxi)
+ Những chiến sĩ chữa cháy (phải làm việc ở nơi nhiều khói, có khí độc, thiếu không khí…)
Câu 12:
Phương pháp:
a) KL + HCl → Muối Clorua + H2
b) Đổi số mol Mg, tính mol H2 theo mol Mg dựa vào PTHH
c) Viết PTHH, tính số mol O2 theo số mol H2.
Từ đó tính được VO2(đktc) = ? → Vkk = 5.VO2 = ?
Hướng dẫn giải:
a) PTHH: Mg + 2HCl → MgCl2 + H2↑
b) Số mol Mg là:
Theo PTHH: Cứ 1 mol Mg phản ứng sinh ra 1 mol H2
Theo Đề Bài: Vậy cứ 0,2 mol Mg phản ứng sinh ra x =? Mol H2
Thể tích khí H2 sinh ra là:
VH2(đktc) = nH2 × 22,4 = 0,2 × 22,4 = 4,48 (lít)
c) PTHH: 2H2 + O2 → 2H2O
(mol) 2 1
(mol) 0,2→ y=?
→ Số mol O2 pư = 0,1 (mol)
→ VO2(đktc) = nO2 × 22,4 = 0,1× 22,4 = 2,24 (lít)
Vì thể tích không khí bằng 5 lần thể tích oxi nên ta có:
Vkk = 5VO2 = 5×2,24 = 11,2 (lít)
Nguồn: Sưu tầm
Loigiaihay.com
Các bài khác cùng chuyên mục













Danh sách bình luận