Lý thuyết Khái niệm về cân bằng hóa học - Hóa học 11 - Chân trời sáng tạo
Khái niệm: Phản ứng một chiều là phản ứng mà sản phẩm sinh ra không phản ứng được với nhau để tạo thành chất đầu.
Tổng hợp đề thi học kì 2 lớp 11 tất cả các môn - Chân trời sáng tạo
Toán - Văn - Anh - Lí - Hóa - Sinh
I. Phản ứng một chiều và phản ứng thuận nghịch và cân bằng hóa học
1. Phản ứng một chiều
- Khái niệm: Phản ứng một chiều là phản ứng mà sản phẩm sinh ra không phản ứng được với nhau để tạo thành chất đầu.
- Ví dụ: CH4 + 2O2 → CO2 + 2H2O
2. Phản ứng thuận nghịch
- Phản ứng thuận nghịch là phản ứng xảy ra theo hai chiều ngược nhau trong cùng điều kiện.
- Biểu diễn: Bằng hai nửa mũi tên ngược chiều nhau.()
- Ví dụ: H2(g) + I2(g) 2HI(g)
II. Hằng số cân bằng của phản ứng thuận nghịch
1. Trạng thái cân bằng
- Trạng thái cân bằng của phản ứng thuận nghịch là trạng thái tại đó tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
2. Hệ số cân bằng
a, Biểu thức của hằng số cân bằng.
- Xét phản ứng thuận nghịch tổng quát: aA + bB cC + dD.
Ở trạng thái cân bằng, hằng số cân bằng (KC) được xác định theo biểu thức:
\({K_C} = \frac{{{{[C]}^C}.{{[D]}^D}}}{{{{[A]}^A}.{{[B]}^B}}}\)
Trong đó:
+ [A], [B], [C], [D] là nồng độ mol của các chất A, B, C, D ở trạng thái cân bằng.
+ a, b, c, d là hệ số tỉ lượng của các chất trong phương trình hóa học của phản ứng.
- Ví dụ: Xét phản ứng: C(s) + CO2(g) 2CO(g)
\({K_C} = \frac{{{{[CO]}^2}}}{{[C].[C{O_2}]}}\)
b, Ý nghĩa của hằng số cân bằng
- Hằng số cân bằng KC phụ thuộc vào bản chất của phản ứng và nhiệt độ.
- KC càng lớn thì phản ứng thuận càng chiếm ưu thế và ngược lại.
III. Các yêu tố ảnh hưởng đến sự dịch chuyển cân bằng hóa học
1. Ảnh hưởng của nhiệt độ
- Khi nhiệt độ tăng, cân bằng chuyển dịch theo chiều làm giảm nhiệt độ, tức là chiều phản ứng thu nhiệt, nghĩa là chiều làm giảm tác động của tăng nhiệt độ và ngược lại.
2. Ảnh hưởng của nồng độ
- Khi tăng nồng độ một chất trong phản ứng thì cân bằng hóa học bị phá vỡ và chuyển dịch theo chiều làm giảm nồng độ của chất đó và ngược lại.
3. Ảnh hưởng của áp suất
- Khi tăng áp suất chung của hệ, thì cân bằng chuyển dịch theo chiều làm giảm áp suất, tức là chiều làm giảm số mol khí và ngược lại.
4. Nguyên lí chuyển dịch cân bằng Le Chatelier
- Nguyên lí chuyển dịch cân bằng Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng, khi chịu một tác động bên ngoài như biến đổi nồng độ, nhiệt độ, áp suất thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó.
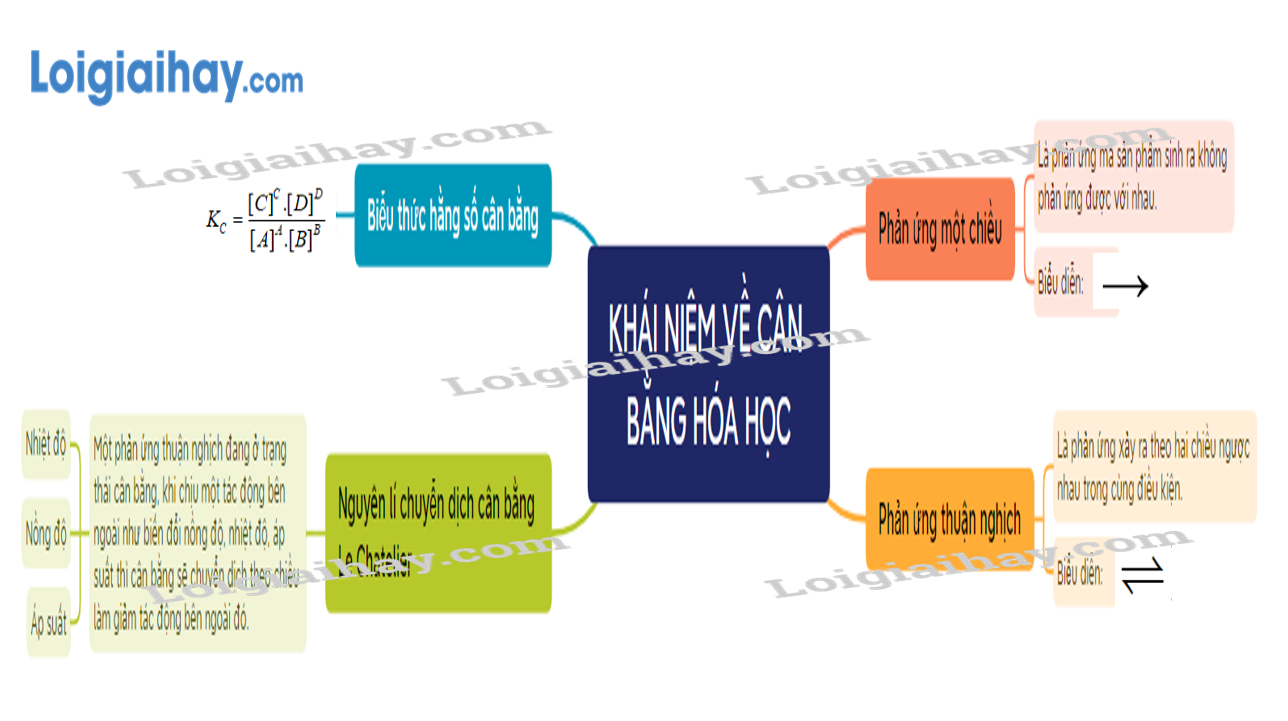
SƠ ĐỒ TƯ DUY
Luyện Bài Tập Trắc nghiệm Hóa 11 - Chân trời sáng tạo - Xem ngay
Các bài khác cùng chuyên mục
- Bài 19: Carboxylic acid trang 124, 125, 126, 127, 128, 129, 130, 131, 132 Hóa học 11 Chân trời sáng tạo
- Bài 18: Hợp chất carbonyl trang 115, 116, 117, 118, 119, 120, 121, 122, 123 Hóa học 11 Chân trời sáng tạo
- Bài 17: Phenol trang 108, 109, 110, 111, 112, 113, 114 Hóa học 11 Chân trời sáng tạo
- Bài 16: Alcohol trang 99, 100, 101, 102, 103, 104, 105, 106, 107 Hóa học 11 Chân trời sáng tạo
- Bài 15: Dẫn xuất halogen trang 92, 93, 94, 95, 96, 97, 98 Hóa học 11 Chân trời sáng tạo












Danh sách bình luận