Bài 14. Tính biến thiên enthalpy của phản ứng hóa học trang 56, 57, 58 SBT Hóa 10 Chân trời sáng tạo
Trình bày cách tính enthalpy của phản ứng hoá học dựa vào năng lượng liên kết và dựa vào enthalpy tạo thành của các chất Cho phản ứng tổng quát aA + bB -> mM + nN. Hãy chọn các phương án tính đúng. ({Delta _r}H_{298}^0) của phản ứng:
Tổng hợp đề thi học kì 1 lớp 10 tất cả các môn - Chân trời sáng tạo
Toán - Văn - Anh - Lí - Hóa - Sinh - Sử - Địa...
14.1
Trình bày cách tính enthalpy của phản ứng hoá học dựa vào năng lượng liên kết và dựa vào enthalpy tạo thành của các chất
Lời giải chi tiết:
- Cách tính enthalpy của phản ứng hóa học dựa vào năng lượng liên kết
\({\Delta _r}H_{298}^0 = \sum {{E_b}(cd)} - \sum {{E_b}(sp)} \)
Trong đó: \(\sum {{E_b}(cd)} \) và \(\sum {{E_b}(sp)} \) là tổng năng lượng liên kết trong phân tử các chất đầu và các chất sản phẩm
- Cách tính enthalpy của phản ứng hóa học dựa vào enthalpy tạo thành của các chất
\({\Delta _r}H_{298}^0 = \sum {{\Delta _r}H_{298}^0(sp)} - \sum {{\Delta _r}H_{298}^0(cd)} \)
Trong đó: \(\sum {{\Delta _r}H_{298}^0(sp)} \) và \(\sum {{\Delta _r}H_{298}^0(cd)} \) là tổng enthalpy tạo thành ở điều kiện chuẩn của sản phẩm và chất đầu của phản ứng
14.2
Cho phản ứng tổng quát aA + bB -> mM + nN. Hãy chọn các phương án tính đúng. \({\Delta _r}H_{298}^0\) của phản ứng:
(a) \({\Delta _r}H_{298K}^0 = m\;x\;{\Delta _f}H_{298}^0(M) + n\;x\;{\Delta _f}H_{298}^0(N) - a\;x\;{\Delta _f}H_{298}^0(A) - b\;x\;{\Delta _f}H_{298}^0(B)\)
(b) \({\Delta _r}H_{298K}^0 = a\;x\;{\Delta _f}H_{298}^0(A) + b\;x\;{\Delta _f}H_{298}^0(B) - m\;x\;{\Delta _f}H_{298}^0(M) - n\;x\;{\Delta _f}H_{298}^0(N)\)
(c) \({\Delta _r}H_{298K}^0 = a\;x\;{E_b}(A) + b\;x\;{E_b}(B) - m\;x\;{E_b}(M) - n\;x\;{E_b}(N)\)
(d) \({\Delta _r}H_{298K}^0 = m\;x\;{E_b}(M) + n\;x\;{E_b}(N) - a\;x\;{E_b}(A) - b\;x\;{E_b}(B)\)
Phương pháp giải:
- Theo năng lượng liên kết :\({\Delta _r}H_{298}^0 = \sum {{E_b}(cd)} - \sum {{E_b}(sp)} \)
- Theo enthalpy tạo thành của các chất: \({\Delta _r}H_{298}^0 = \sum {{\Delta _r}H_{298}^0(sp)} - \sum {{\Delta _r}H_{298}^0(cd)} \)
Lời giải chi tiết:
- Đáp án: (a) và (c)
14.3
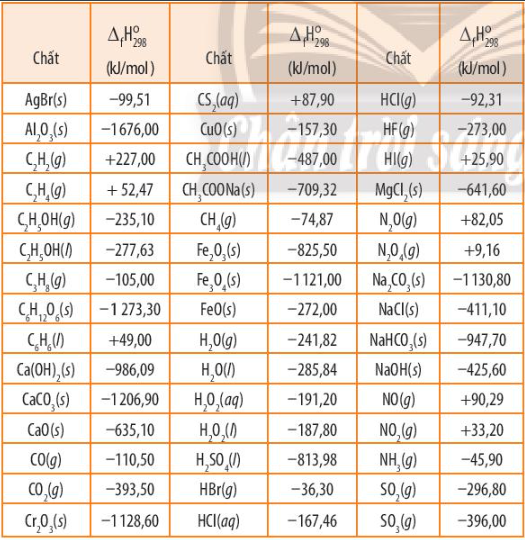
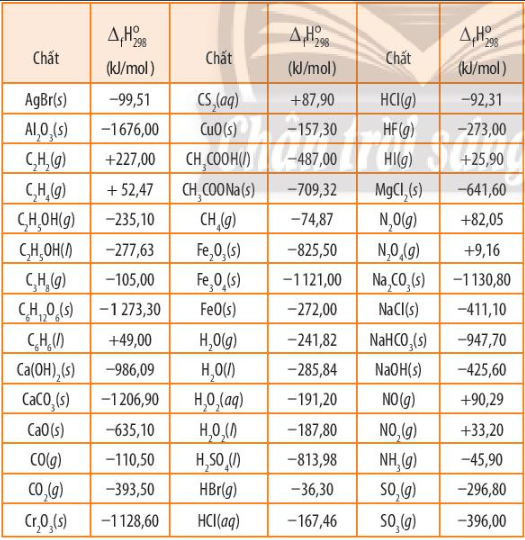
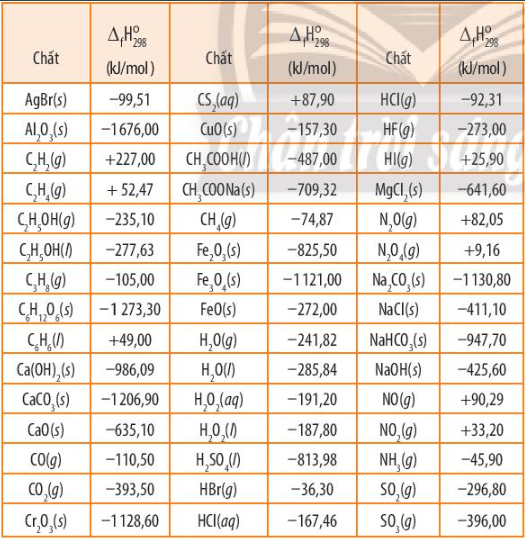
Thành phần chính của đa số các loại đá dùng trong xây dựng là CaCO3, chúng vừa có tác dụng chịu nhiệt, vừa chịu được lực. Dựa vào bảng 13.1 SGK trang 84, tính \({\Delta _r}H_{298}^0\) của phản ứng:
CaCO3(s) -> CaO(s) + CO2(g)
Phản ứng có xảy ra thuận lợi ở điều kiện thường không?
Phương pháp giải:
Dựa vào công thức tính: \({\Delta _r}H_{298}^0 = \sum {{\Delta _r}H_{298}^0(sp)} - \sum {{\Delta _r}H_{298}^0(cd)} \) và bảng số liệu
Lời giải chi tiết:
\({\Delta _r}H_{298}^0 = - 635,1 + ( - 393,5) - ( - 1206,9) = + 178,3kJ\)
=> Phản ứng không xảy ra ở điều kiện thường do có \({\Delta _r}H_{298}^0 > 0\)
14.4
Propene là nguyên liệu cho sản xuất nhựa polypropylene (PP). PP được sử dụng để sản xuất các sản phẩm ông, màng, dày cách điện, kéo sợi, đồ gia dụng và các sản phẩm tạo hình khác.

Phản ứng tạo thành propene từ propyne:
CH3-C≡CH(g) + H2(g) ->CH3-CH=CH2(g)
a) Hãy xác định số liên kết C-H; C-C; C=C trong hợp chất CH3-C≡CH (propyne).
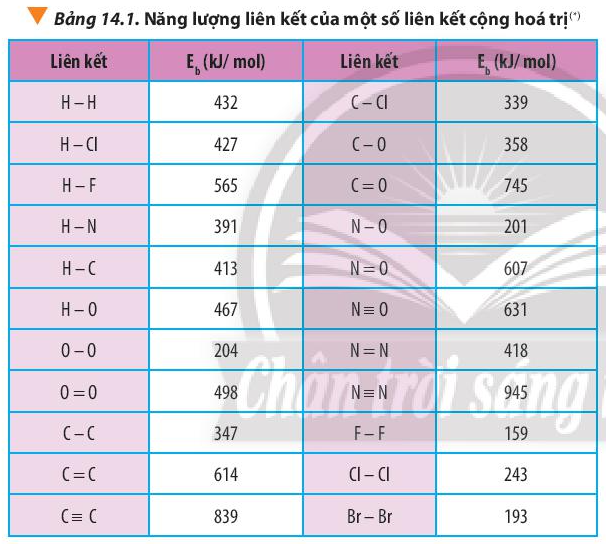
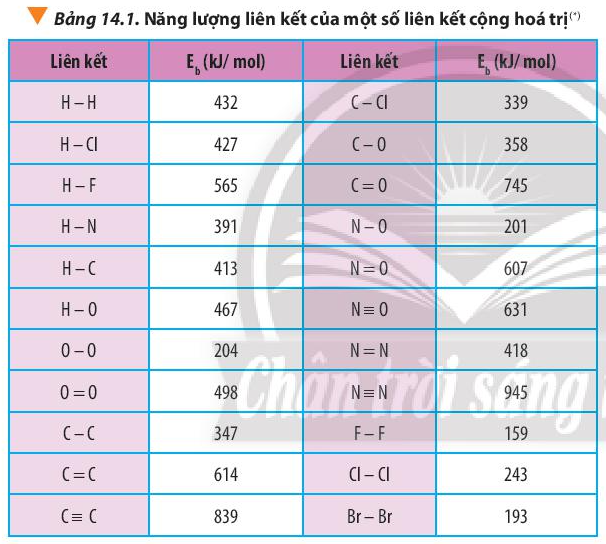
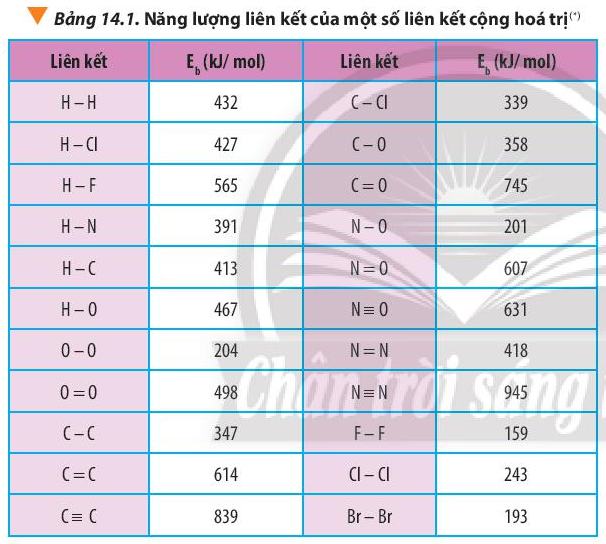
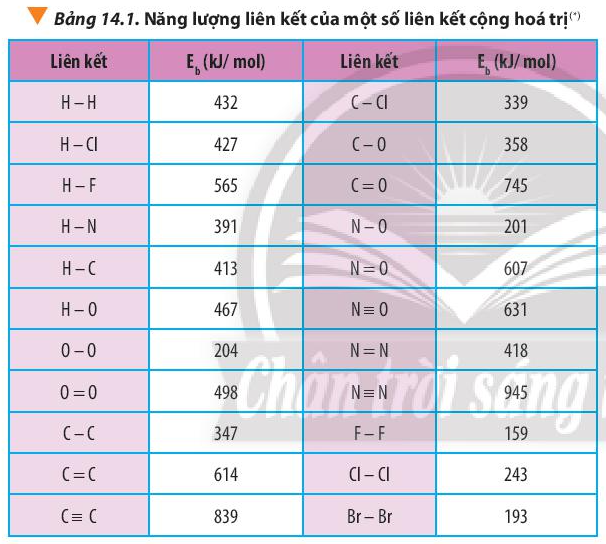
b) Từ năng lượng của các liên kết (Bảng 14.1, SGK trang 89), hãy tính biến thiên enthalpy của phản ứng tạo thành propene trên.
Phương pháp giải:
Dựa vào công thức \({\Delta _r}H_{298}^0 = \sum {{E_b}(cd)} - \sum {{E_b}(sp)} \) và bảng số liệu
Lời giải chi tiết:
a) Trong hợp chất CH3-C≡CH có 4 liên kết C-H, 1 liên kết C-C và 1 liên kết C≡C
b) Biến thiên enthalpy của phản ứng là:
\({\Delta _r}H_{298}^0 = \sum {{E_b}(cd)} - \sum {{E_b}(sp)} \)
=> \(\begin{array}{l}{\Delta _r}H_{298}^0 = {\rm{(}}{E_b}(C \equiv C) + {E_b}(C - C) + 4.{E_b}(C - H) + {E_b}(H - H){\rm{)}}\\{\rm{ - (}}{E_b}(C = C) + {E_b}(C - C) + 6.{E_b}(C - H){\rm{)}}\end{array}\)
=> \({\Delta _r}H_{298}^0 = {\rm{(}}839 + 347 + 4.413 + 432{\rm{) - (614 + 347 + 6}}{\rm{.413) = - 169kJ}}\)
14.5
Tính nhiệt tạo thành chuẩn của HF và NO dựa vào năng lượng liên kết (Bảng 14.1 SGK), của F2, H2, HF, N2, O2, NO. Giải thích sự khác nhau về nhiệt tạo thành của HF và NO.
Phương pháp giải:
Dựa vào công thức \({\Delta _r}H_{298}^0 = \sum {{E_b}(cd)} - \sum {{E_b}(sp)} \) và bảng số liệu
Lời giải chi tiết:
- Biến thiên enthalpy của phản ứng H2(g) + F2(g) -> 2HF(g) là:
\({\Delta _r}H_{298}^0 = \sum {{E_b}(cd)} - \sum {{E_b}(sp)} \)
=> \({\Delta _r}H_{298}^0 = {E_b}(H - H) + {E_b}(F - F) - 2.{E_b}(H - F)\)
=> \({\Delta _r}H_{298}^0 = 432 + 159 - 2.565 = - 539kJ\) < 0
=> Phản ứng xảy ra
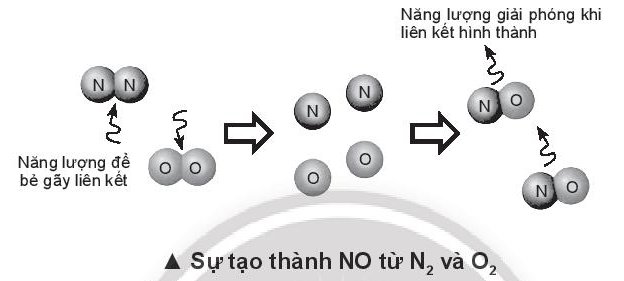
- Biến thiên enthalpy của phản ứng N2(g) + O2(g) " 2NO(g) là:
\({\Delta _r}H_{298}^0 = \sum {{E_b}(cd)} - \sum {{E_b}(sp)} \)
=> \({\Delta _r}H_{298}^0 = {E_b}(N \equiv N) + {E_b}(O = O) - 2.{E_b}(N \equiv O)\)
=> \({\Delta _r}H_{298}^0 = 945 + 498 - 2.631 = + 181kJ\) > 0
=> Phản ứng không xảy ra
- Giải thích: Do năng lượng liên kết giữa liên kết ba của 2 nguyên tử Nitrogen rất lớn nên cần cung cấp năng lượng từ bên ngoài để phá vỡ liên kết N≡N
14.6
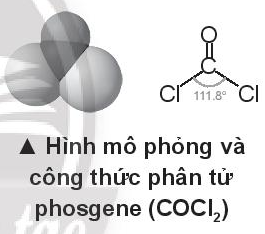
Phosgene là chất khí không màu, mùi cỏ mục, dễ hoá lỏng; khối lượng riêng 1,420 g/cm3 (ở 0°C); t = 8,2°C. Phosgene ít tan trong nước; dễ tan trong các dung môi hữu cơ, bị thuỷ phân chậm bằng hơi nước; không cháy, là sản phẩm công nghiệp quan trọng; dùng trong tổng hợp hữu cơ để sản xuất sản phẩm nhuộm, chất diệt cỏ, polyurethane,…
Phosgene là một chất độc. Ở nồng độ 0,005 mg/L đã nguy hiểm đối với người, trong khoảng 0,1 – 0,3 mg/L, gây tử vong sau khoảng 15 phút.
Phosgene được điều chế bằng cách cho hỗn hợp CO và Cl2, đi qua than hoạt tính. Biết Eb(Cl-Cl) = 243 kJ/mol; Eb(C-Cl) = 339 kJ/mol; Eb(C=O) = 745 kJ/mol; Eb(C≡O) = 1075 kJ/mol.
Hãy tính biến thiên enthalpy của phản ứng tạo thành phosgene từ CO và Cl2.
Phương pháp giải:
Dựa vào công thức \({\Delta _r}H_{298}^0 = \sum {{E_b}(cd)} - \sum {{E_b}(sp)} \)
Lời giải chi tiết:

14.7
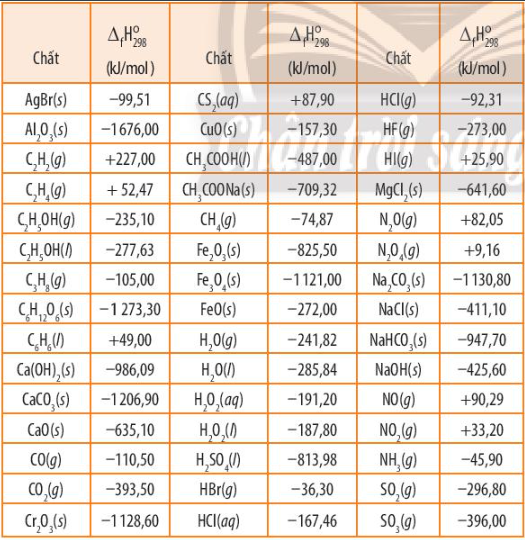
Kim loại nhôm có thể khử được oxide của nhiều nguyên tố. Dựa vào nhiệt tạo thành chuẩn của các chất (Bảng 13.1 SGK), tính biến thiên enthalpy của phản ứng nhôm khử 1 mol mỗi oxide sau
a) Fe3O4(s)
b) Cr2O3(s)
Phương pháp giải:
Dựa vào công thức tính: \({\Delta _r}H_{298}^0 = \sum {{\Delta _r}H_{298}^0(sp)} - \sum {{\Delta _r}H_{298}^0(cd)} \) và bảng số liệu
Lời giải chi tiết:
- Biến thiên enthalpy của phản ứng 8Al(s) + 3Fe3O4(s) 9Fe(s) + 4Al2O3(s) là:
\({\Delta _r}H_{298}^0 = \sum {{\Delta _r}H_{298}^0(sp)} - \sum {{\Delta _r}H_{298}^0(cd)} \)
=> \({\Delta _r}H_{298}^0 = 4.{\Delta _r}H_{298}^0(A{l_2}{O_3}) - 3.{\Delta _r}H_{298}^0(F{e_3}{O_4})\) (Do \({\Delta _r}H_{298}^0\) của đơn chất = 0)
=> \({\Delta _r}H_{298}^0 = 4.( - 1676,00) - 3.( - 1121,00) = - 3341kJ\)
=> Biến thiên enthalpy của phản ứng nhôm khử 1 mol Fe3O4 là
\({\Delta _r}H_{298}^0 = \frac{1}{3}.( - 3341) = - 1113,67kJ\)
- Biến thiên enthalpy của phản ứng 2Al(s) + Cr2O3(s) 2Cr(s) + Al2O3(s) là:
\({\Delta _r}H_{298}^0 = \sum {{\Delta _r}H_{298}^0(sp)} - \sum {{\Delta _r}H_{298}^0(cd)} \)
=> \({\Delta _r}H_{298}^0 = {\Delta _r}H_{298}^0(A{l_2}{O_3}) - {\Delta _r}H_{298}^0(C{r_2}{O_3})\) (Do \({\Delta _r}H_{298}^0\) của đơn chất = 0)
=> \({\Delta _r}H_{298}^0 = ( - 1676,00) - ( - 1128,60) = - 547,4kJ\)
=> Biến thiên enthalpy của phản ứng nhôm khử 1 mol Cr2O3 là \({\Delta _r}H_{298}^0 = - 547,4kJ\)
14.8
Cho 3 hydrocarbon X, Y, Z đều có 2 nguyên tử C trong phân tử. Số nguyên tử H trong các phân tử tăng dần theo thứ tự X, Y, Z.
a) Viết công thức cấu tạo của X, Y, Z.
b) Viết phương trình đốt cháy hoàn toàn X, Y, Z với hệ số nguyên tối giản.
c) Tính biến thiên enthalpy của mỗi phản ứng dựa vào enthalpy tạo thành tiêu chuẩn trong bảng sau:
|
Chất |
X(g) |
Y(g) |
Z(g) |
CO2(g) |
H2O(g) |
|
\({\Delta _f}H_{298}^0\)(kJ/mol) |
+227,0 |
+52,47 |
-84,67 |
-393,5 |
-241,82 |
d) Từ kết quả tính toán đưa ra kết luận về ứng dụng của phản ứng đốt cháy X, Y, Z trong thực tiễn.
Phương pháp giải:
- Trong hợp chất CxHyOz thì y luôn là số chẵn và y ≤ 2x + 2
- Công thức tính biến thiên enthalpy: \({\Delta _r}H_{298}^0 = \sum {{\Delta _f}H_{298}^0(sp)} - \sum {{\Delta _f}H_{298}^0(cd)} \)
Lời giải chi tiết:
a) - Số nguyên tử Hydrogen trong hợp chất ≤ 2.2 + 2 = 6 và phải là số chẵn
=> Các công thức của X, Y và Z lần lượt là: C2H2; C2H4 và C2H6
b) Phương trình đốt cháy:
2C2H2 + 5O2 4CO2 + 2H2O
C2H4 + 3O2 2CO2 + 2H2O
2C2H6 + 7O2 4CO2 + 6H2O
c) - Xét phương trình 2C2H2 + 5O2 4CO2 + 2H2O
\({\Delta _r}H_{298}^0 = \sum {{\Delta _f}H_{298}^0(sp)} - \sum {{\Delta _f}H_{298}^0(cd)} \)
=> \({\Delta _r}H_{298}^0 = 4.{\Delta _f}H_{298}^0(C{O_2}) + 2.{\Delta _f}H_{298}^0({H_2}O) - 2.{\Delta _f}H_{298}^0({C_2}{H_2})\)
(Do \({\Delta _f}H_{298}^0\) của đơn chất = 0)
=> \({\Delta _r}H_{298}^0 = 4.( - 393,5) + 2.( - 241,82) - 2.(227,0) = - 2511,64kJ\)
- Xét phương trình C2H4 + 3O2 2CO2 + 2H2O
\({\Delta _r}H_{298}^0 = \sum {{\Delta _f}H_{298}^0(sp)} - \sum {{\Delta _f}H_{298}^0(cd)} \)
=> \({\Delta _r}H_{298}^0 = 2.{\Delta _f}H_{298}^0(C{O_2}) + 2.{\Delta _f}H_{298}^0({H_2}O) - {\Delta _f}H_{298}^0({C_2}{H_4})\)
(Do \({\Delta _f}H_{298}^0\) của đơn chất = 0)
=> \({\Delta _r}H_{298}^0 = 2.( - 393,5) + 2.( - 241,82) - 52,47 = - 1323,11kJ\)
- Xét phương trình 2C2H6 + 7O2 4CO2 + 6H2O
\({\Delta _r}H_{298}^0 = \sum {{\Delta _f}H_{298}^0(sp)} - \sum {{\Delta _f}H_{298}^0(cd)} \)
=> \({\Delta _r}H_{298}^0 = 4.{\Delta _f}H_{298}^0(C{O_2}) + 6.{\Delta _f}H_{298}^0({H_2}O) - 2.{\Delta _f}H_{298}^0({C_2}{H_6})\)
(Do \({\Delta _f}H_{298}^0\) của đơn chất = 0)
=> \({\Delta _r}H_{298}^0 = 4.( - 393,5) + 6.( - 241,82) - 2.( - 84,67) = - 2855,58kJ\)
d) \({\Delta _r}H_{298}^0\) của cả 3 phương trình đều có giá trị lớn và < 0 " trong thực tiễn được dùng làm nhiên liệu.
14.9
Cho các phản ứng:
CaCO3(s) -> CaO(s) + CO2(g) \({\Delta _r}H_{298}^0 = + 178,49kJ\)
C2H5OH(l) + 3O2(g) -> 2CO2(g) + 3H2O(l) \({\Delta _r}H_{298}^0 = - 1370,70kJ\)
C(graphite, s) + O2(g) -> CO2(g) \({\Delta _r}H_{298}^0 = - 393,51kJ\)
a) Phản ứng nào có thể tự xảy ra (sau giai đoạn khơi mào ban đầu), phản ứng nào không thể tự xảy ra?
b) Khối lượng ethanol hay graphite cần dùng khi đốt cháy hoàn toàn đủ tạo lượng nhiệt cho quá trình nhiệt phân hoàn toàn 0,1 mol CaCO3. Giả thiết hiệu suất các quá trình đều là 100%.
Phương pháp giải:
a) Phản ứng nào có \({\Delta _r}H_{298}^0\) > 0 không thể tự xảy ra. Phản ứng nào có \({\Delta _r}H_{298}^0\) < 0 có thể tự xảy ra sau khi khơi mào.
b) Tính \({\Delta _r}H_{298}^0\) của quá trình nhiệt phân hoàn toàn 0,1 mol CaCO3. => Tính mol ethanol và graphite cần dùng => Tính khối lượng ethanol và graphite cần dùng
Lời giải chi tiết:
a) Phản ứng CaCO3(s) -> CaO(s) + CO2(g) không tự xảy ra do \({\Delta _r}H_{298}^0\) > 0 (cần cung cấp thêm năng lượng bên ngoài). Hai phản ứng còn lại tự xảy ra sau khi khơi mào do có \({\Delta _r}H_{298}^0\) < 0 (tự tạo thêm năng lượng khi phản ứng diễn ra)
b) \({\Delta _r}H_{298}^0\) của quá trình nhiệt phân hoàn toàn 0,1 mol CaCO3 là
\({\Delta _r}H_{298}^0 = 0,1.( + 178,49) = + 17,849kJ\)
- \({n_{{C_2}{H_5}OH}} = \frac{{17,849}}{{1370,70}} = 0,013\)mol -> \({m_{{C_2}{H_5}OH}} = 0,013.46 = 0,598\)gam
- \({n_C} = \frac{{17,849}}{{393,51}} = 0,045\)mol -> \({m_C} = 0,045.12 = 0,54\)gam
14.10
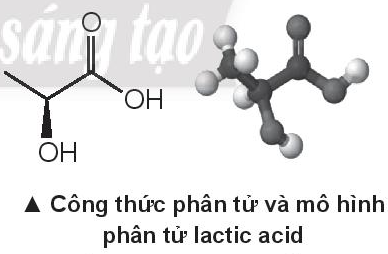
Lactic acid hay acid sữa là hợp chất hoá học đóng vai trò quan trọng trong nhiều quá trình sinh hoá, lần đầu tiên được phân tách vào năm 1780 bởi nhà hoá học Thuỵ Điển Carl Wilhelm Scheele. Lactic acid có công thức phân tử C3H6O3, công thức cấu tạo CH3-CH(OH)-COOH
Khi vận động mạnh cơ thể không đủ cung cấp oxygen, thì cơ thể sẽ chuyển hoá glucose thành lactic acid từ các tế bào để cung cấp năng lượng cho cơ thể (lactic acid tạo thành từ quá trình này sẽ gây mỏi cơ) theo phương trình sau:
C6H12O6(aq) -> 2C3H6O3(aq) \({\Delta _r}H_{298}^0 = - 150kJ\)
Biết rằng cơ thể chỉ cung cấp 98% năng lượng nhờ oxygen, năng lượng còn lại nhờ vào sự chuyển hoá glucose thành lactic acid.
Giả sử một người chạy bộ trong một thời gian tiêu tốn 300 kcal. Tính khối lượng lactic acid tạo ra từ quá trình chuyển hóa đó (biết 1 cal = 4,184 J).
Phương pháp giải:
Dựa vào công thức đổi cal sang J -> Tính năng lượng tạo thành của lactic acid -> Tính số mol lactic acid tạo thành -> Tính khối lượng lactic acid tạo thành
Lời giải chi tiết:
- Năng lượng của sự chuyển hoá glucose thành lactic acid là
2%.300kcal = 6 kcal = 6000 cal = 25104 J = 25,104 kJ
- Do C6H12O6(aq) -> 2C3H6O3(aq) có \({\Delta _r}H_{298}^0 = - 150kJ\)
=> \({n_{{C_3}{H_6}{O_3}}} = \frac{{25,104}}{{150}}.2 = 0,335\)mol => \({m_{{C_3}{H_6}{O_3}}} = 0,335.90 = 30,15\)gam
14.11
Chloromethane (CH3Cl), còn được gọi là methyl chloride, Refrigerant-40 hoặc HCC 40. CH3Cl từng được sử dụng rộng rãi như một chất làm lạnh. Hợp chất khí này rất dễ cháy, có thể không mùi hoặc có mùi thơm nhẹ.
Từ năng lượng của các liên kết (Bảng 14.1 SGK), hãy tính biến thiên enthalpy của phản ứng tạo thành chloromethane:
CH4(g) + Cl2(g) -> CH3Cl(g) + HCl(g)
Cho biết phản ứng dễ dàng xảy ra dưới ánh sáng mặt trời. Kết quả tính có mâu thuẫn với khả năng dễ xảy ra của phản ứng không?
Phương pháp giải:
Dựa vào công thức \({\Delta _r}H_{298}^0 = \sum {{E_b}(cd)} - \sum {{E_b}(sp)} \) và bảng số liệu
Lời giải chi tiết:
Biến thiên enthalpy của phản ứng CH4(g) + Cl2(g) " CH3Cl(g) + HCl(g) là:
\({\Delta _r}H_{298}^0 = \sum {{E_b}(cd)} - \sum {{E_b}(sp)} \)
=> \({\Delta _r}H_{298}^0 = {\rm{(}}4.{E_b}(C - H) + {E_b}(Cl - Cl){\rm{)}} - {\rm{(}}3.{E_b}(C - H) + {E_b}(C - Cl) + {E_b}(H - Cl){\rm{)}}\)
=> \({\Delta _r}H_{298}^0 = (4.413 + 243) - (3.413 + 339 + 427) = - 110kJ\) < 0
=> Phản ứng xảy ra " Kết quả tính toán phù hợp với thực tế phản ứng xảy ra dễ dàng trong điều kiện có ánh sáng
14.12
Một xe tải đang vận chuyển đất đèn (thành phần chính là CaC2 và CaO) gặp mưa xảy ra sự cố, xe tải đã bốc cháy.
a) Viết phản ứng của CaC2 và CaO với nước.
b) Xe tải bốc cháy do các phản ứng trên toả nhiệt kích thích phản ứng cháy của acetylene:
C2H2(g) + 2,5O2(g) -> 2CO2(g) + H2O(g)
Dựa vào Bảng 13.1 SGK, tính biến thiên enthalpy của các phản ứng trên. Cho biết phản ứng toả nhiệt hay thu nhiệt.
Phương pháp giải:
Dựa vào công thức tính: \({\Delta _r}H_{298}^0 = \sum {{\Delta _r}H_{298}^0(sp)} - \sum {{\Delta _r}H_{298}^0(cd)} \) và bảng số liệu
Lời giải chi tiết:
a) CaC2(s) + 2H2O(l) -> Ca(OH)2(aq) + C2H2(g)
CaO(s) + H2O(l) -> Ca(OH)2(aq)
b) - Biến thiên enthalpy của phản ứng C2H2(g) + 2,5O2(g) -> 2CO2(g) + H2O(g) là:
\({\Delta _r}H_{298}^0 = \sum {{\Delta _r}H_{298}^0(sp)} - \sum {{\Delta _r}H_{298}^0(cd)} \)
=> \({\Delta _r}H_{298}^0 = 2.{\Delta _f}H_{298}^0(C{O_2}) + {\Delta _f}H_{298}^0({H_2}O) - {\Delta _f}H_{298}^0({C_2}{H_2})\) (Do \({\Delta _r}H_{298}^0\) của đơn chất = 0)
=> \({\Delta _r}H_{298}^0 = 2.(- 393,50) + (- 241,82) - (+ 227,00) = - 1255,82kJ\) < 0
=> Phản ứng tỏa nhiệt
14.13
Cho phương trình hoá học của phản ứng:
C2H4(g) + H2O(l) -> C2H5OH(l)
Tính biến thiên enthalpy của phản ứng theo nhiệt tạo thành chuẩn của các chất (Bảng 13.1 SGK).
Phương pháp giải:
Dựa vào công thức tính: \({\Delta _r}H_{298}^0 = \sum {{\Delta _r}H_{298}^0(sp)} - \sum {{\Delta _r}H_{298}^0(cd)} \) và bảng số liệu
Lời giải chi tiết:
- Biến thiên enthalpy của phản ứng C2H4(g) + H2O(l) -> C2H5OH(l) là:
\({\Delta _r}H_{298}^0 = \sum {{\Delta _r}H_{298}^0(sp)} - \sum {{\Delta _r}H_{298}^0(cd)} \)
=> \({\Delta _r}H_{298}^0 = 2.{\Delta _f}H_{298}^0({C_2}{H_5}OH) - {\Delta _f}H_{298}^0({C_2}{H_4}) - {\Delta _f}H_{298}^0({H_2}O)\)
=> \({\Delta _r}H_{298}^0 = - 277,63 - (+ 52,47) - (- 285,84) = - 44,26kJ\)
14.14
Cho phản ứng phân huỷ hydrazine:
N2H4(g) -> N2(g) + 2H2(g)
a) Tính \({\Delta _r}H_{298}^0\) theo năng lượng liên kết của phản ứng trên.
b) Hydrazine (N2H4) là chất lỏng ở điều kiện thường (sôi ở 114°C, khối lượng riêng 1,021 g/cm3). Hãy đề xuất lí do N2H4 được sử dụng làm nhiên liệu trong động cơ tên lửa. Biết Eb(N-N) = 160 kJ/mol; Eb(N–H) = 391 kJ/mol, Eb(N≡N) = 945 kJ/mol; Eb(H-H) = 432 kJ/mol.
Phương pháp giải:
Dựa vào công thức \({\Delta _r}H_{298}^0 = \sum {{E_b}(cd)} - \sum {{E_b}(sp)} \) và bảng số liệu
Lời giải chi tiết:
a) - Biến thiên enthalpy của phản ứng N2H4(g) -> N2(g) + 2H2(g) là:
\({\Delta _r}H_{298}^0 = \sum {{E_b}(cd)} - \sum {{E_b}(sp)} \)
=> \({\Delta _r}H_{298}^0 = {E_b}(N - N) + 4.{E_b}(N - H) - {E_b}(N \equiv N) - 2.{E_b}(H - H)\)
=> \({\Delta _r}H_{298}^0 = 160 + 4.391 - 945 - 2.432 = - 85kJ\)
b) Các lí do N2H4 được sử dụng làm nhiên liệu trong động cơ tên lửa:
- N2H4 là chất lỏng nên dễ bảo quản (nếu là chất khí cần nén ở điều kiện áp suất cao dễ gây nguy hiểm và tốn công bảo quản)
- Phương trình có \({\Delta _r}H_{298}^0 = - 85kJ\)< 0 " Phản ứng tự xảy ra mà không cần cung cấp năng lượng
- 1 mol N2H4 ở dạng lỏng sau phản ứng sẽ sinh ra tổng cộng 3 mol khí " tạo được áp suất lớn để đẩy tên lửa bay lên
14.15
Quá trình hoà tan calcium chloride trong nước:
CaCl2(s) -> Ca2+(aq) + 2Cl-(aq) \({\Delta _r}H_{298}^0 = ?\)
|
Chất |
CaCl2 |
Ca2+ |
Cl- |
|
\({\Delta _f}H_{298}^0\)(kJ/mol) |
-795,0 |
-542,83 |
-167,16 |
Tính biến thiên enthalpy của quá trình.
Phương pháp giải:
Dựa vào công thức tính: \({\Delta _r}H_{298}^0 = \sum {{\Delta _r}H_{298}^0(sp)} - \sum {{\Delta _r}H_{298}^0(cd)} \)
Lời giải chi tiết:
- Biến thiên enthalpy của phản ứng CaCl2(s) -> Ca2+(aq) + 2Cl-(aq) là:
\({\Delta _r}H_{298}^0 = \sum {{\Delta _r}H_{298}^0(sp)} - \sum {{\Delta _r}H_{298}^0(cd)} \)
=> \({\Delta _r}H_{298}^0 = {\Delta _f}H_{298}^0(C{a^{2 + }}) + 2.{\Delta _f}H_{298}^0(C{l^ - }) - {\Delta _f}H_{298}^0(CaC{l_2})\)
=> \({\Delta _r}H_{298}^0 = - 542,83 + 2.(- 167,16) - (- 795,0) = - 82,15kJ\)
Luyện Bài Tập Trắc nghiệm Hóa 10 - Chân trời sáng tạo - Xem ngay
Các bài khác cùng chuyên mục
- Ôn tập chương 7 trang 83, 84 SBT Hóa 10 Chân trời sáng tạo
- Bài 18. Hydrogen halide và một số phản ứng của ion halide trang 79, 80, 81 SBT Hóa 10 Chân trời sáng tạo
- Bài 17. Tính chất vật lí và hóa học các đơn chất nhóm VIIA trang 75, 76, 77 SBT Hóa 10 Chân trời sáng tạo
- Ôn tập chương 6 trang 73, 74 SBT Hóa 10 Chân trời sáng tạo
- Bài 16. Các yếu tố ảnh hường đến tốc độ phản ứng hóa học trang 67, 68, 69 SBT Hóa 10 Chân trời sáng tạo
- Ôn tập chương 7 trang 83, 84 SBT Hóa 10 Chân trời sáng tạo
- Bài 18. Hydrogen halide và một số phản ứng của ion halide trang 79, 80, 81 SBT Hóa 10 Chân trời sáng tạo
- Bài 17. Tính chất vật lí và hóa học các đơn chất nhóm VIIA trang 75, 76, 77 SBT Hóa 10 Chân trời sáng tạo
- Ôn tập chương 6 trang 73, 74 SBT Hóa 10 Chân trời sáng tạo
- Bài 16. Các yếu tố ảnh hường đến tốc độ phản ứng hóa học trang 67, 68, 69 SBT Hóa 10 Chân trời sáng tạo












