Lớp electron thứ 3 có bao nhiêu phân lớp?
A. 1.
B. 2.
C. 3.
D. 4.
Dựa vào số phân lớp trong một lớp electron:
- 4 lớp đầu (1, 2, 3, 4) có số phân lớp trong mỗi lớp bằng số thứ tự của lớp đó
- 3 lớp sau (5, 6, 7) đều có 4 phân lớp
- Đáp án: C

Các bài tập cùng chuyên đề
Nguyên tử của nguyên tố potassium có 19 electron. Ở trạng thái cơ bản, potassium có số orbital chứa electron là
A. 8
B. 9
C. 11
D. 10
Trong lịch sử các thuyết về mô hình nguyên tử, có mô hình hành tinh nguyên tử và mô hình hiện đại nguyên tử. Theo em, trong hai hình bên, hình nào thể hiện mô hình hành tinh nguyên tử, hình nào thể hiện mô hình hiện đại của nguyên tử?
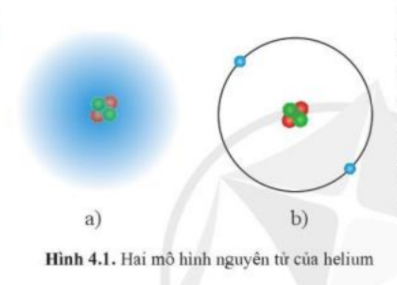
Dựa theo mô hình nguyên tử của Rutherford – Bohr, hãy vẽ mô hình nguyên tử các nguyên tố có Z từ 1 đến 11.
Theo em, xác suất tìm thấy electron trong toàn phần không gian bên ngoài đám mây là khoảng bao nhiêu phần trăm.
Những phát biểu nào sau đây là đúng khi nói về mô hình Rutherford – Bohr?
A. Electron quay xung quanh hạt nhân theo những quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời.
B. Electron không chuyển động theo quỹ đạo cố định mà trong cả khu vực không gian xung quanh hạt nhân.
C. Electron không bị hút vào hạt nhân do còn chịu tác dụng của lực quán tính li tâm.
Nguyên tử Li (Z = 3) có 2 electron ở lớp K và 1 electron ở lớp L. So sánh năng lượng của electron giữa hai lớp theo mô hình Rutherford – Bohr.
Sử dụng mô hình Rutherford – Bohr, hãy cho biết khi electron của nguyên tử H hấp thụ một năng lượng phù hợp, electron đó sẽ chuyển ra xa hay tiến gần vào hạt nhân hơn. Giải thích.
Quan sát Hình 4.1 và 4.2, so sánh điểm giống nhau và khác nhau giữa mô hình Rutherford – Bohr với mô hình hiện đại mô tả sự chuyển động của electron trong nguyên tử
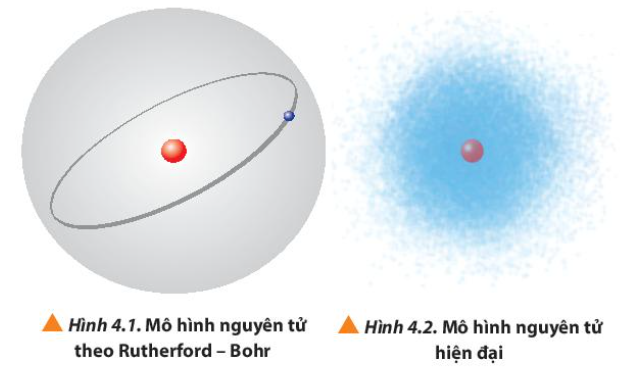
Hệ Mặt Trời gồm Mặt Trời ở trung tâm và các thiên thể quay quanh theo những quỹ đạo xác định. Hãy cho biết mô hình nguyên tử của nhà khoa học nào được gọi là mô hình hành tinh nguyên tử, tương tự như hệ Mặt Trời?

Nguyên tử O có 8 electron. Theo mô hình Rutherford – Bohr, nguyên tử O có số electron có cùng năng lượng ở lớp thứ nhất là
A. 2. B. 4. C. 6. D. 8.
Điền từ/ cụm từ thích hợp vào chỗ trống trong mô tả sau đây về mô hình hành tinh nguyên tử theo Rutherford – Bohr.
Khối lượng nguyên tử tập trung ở ...(1)... Electron quay xung quanh hạt nhân theo những ...(2)... xác định. Electron ở càng xa hạt nhân thì có năng lượng càng ...(3)... Khi nguyên tử hấp thụ năng lượng phù hợp, electron sẽ chuyển ...(4)... hạt nhân hơn.
Nguyên tử F có 9 electron. Theo mô hình Rutherford – Bohr, tỉ lệ số lượng electron trên lớp thứ hai so với số lượng electron trên lớp thứ nhất là
A. 2 : 12. B. 7 : 2. C. 5 : 2. D. 2 : 7.
Phát biểu nào sau đây không đúng khi nói về mô hình Rutherford – Bohr?
A. Electron trên lớp K có năng lượng cao hơn trên lớp L.
B. Electron trên lớp M có năng lượng cao hơn trên lớp K.
C. Electron ở lớp K gần hạt nhân hơn so với electron ở lớp L.
D. Electron ở lớp M xa hạt nhân hơn so với electron ở lớp L.
Đề bài:
Theo mô hình Rutherford - Bohr, khi một nguyên tử H hấp thụ một năng lượng đủ lớn, electron sẽ
A. chuyển từ lớp electron gần hạt nhân sang lớp xa hạt nhân hơn.
B. chuyển từ lớp electron xa hạt nhân về lớp gần hạt nhân hơn.
C. không thay đổi trạng thái.
D. có thể chuyển sang lớp khác bất kì.
Dựa vào mô hình nguyên tử Rutherford – Bohr, hãy cho biết phát biểu nào sau đây là đúng.
A. Số lượng electron tối đa trên các lớp là như nhau.
B. Năng lượng của các electron trên các lớp khác nhau có thể bằng nhau.
C. Khi quay quanh hạt nhân theo một quỹ đạo xác định, năng lượng của electron là không đổi.
D. Electron ở gần hạt nhân nhất có năng lượng cao nhất.
Theo mô hình nguyên tử Rutherford - Bohr, vị trí nào trong số các vị trí A, B, C, D trong hình sau mà electron không xuất hiện?
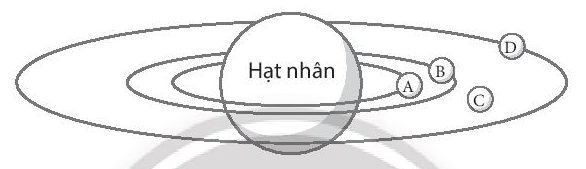
A. Vị trí A.
B. Vị trí B.
C. Vị trí C.
D. Vị trí D.
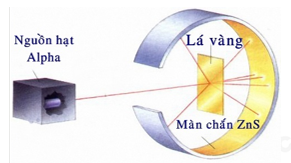
A. Chùm α truyền thẳng.
B. Chùm α bị bật ngược trở lại.
C. Chùm α bị lệch hướng.
D. Chùm α không thể bị xuyên qua.
Mỗi orbital nguyên tử chứa tối đa bao nhiêu electron?
-
A.
1 electron.
-
B.
2 electron.
-
C.
3 electron.
-
D.
4 electron.
Theo mô hình Rutherford – Bohr: Theo chiều từ hạt nhân ra ngoài lớp vỏ
-
A.
năng lượng của các electron giảm dần.
-
B.
năng lượng của các electron không đổi.
-
C.
năng lượng của các electron tăng dần.
-
D.
khối lượng của các electron tăng dần.
Hình ảnh dưới đây là hình dạng của những loại orbital nguyên tử nào?
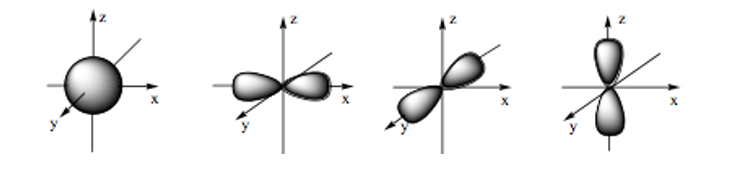
-
A.
s, d.
-
B.
d, f.
-
C.
s, p.
-
D.
p, f.
Trong lịch sử các thuyết về mô hình nguyên tử có mô hình hành tinh nguyên tử (mô hình Rutherford – Bohr) và mô hình hiện đại của nguyên tử.
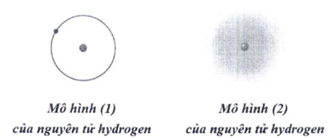
Với nguyên tử hydrogen, mô hình (1) là mô hình hiện đại, mô hình (2) là mô hình hành tinh nguyên tử.
Khái niệm về xác suất tìm thấy electron xuất phát từ mô hình hành tinh nguyên tử.
Theo mô hình (1), electron chuyển động trên quỹ đạo xác định xung quanh hạt nhân.
Khái niệm về orbital nguyên tử xuất phát từ mô hình hiện đại của nguyên tử.
Theo mô hình nguyên tử hiện đại
-
A.
các electron chuyển động rất nhanh xung quanh hạt nhân không theo một quỹ đạo xác định, tạo thành đám mây electron.
-
B.
orbital nguyên tử kà khu vực không gian xung quanh hạt nhân.
-
C.
các electron chuyển động trên những quỹ đạo tròn hay bầu dục xung quanh hạt nhân.
-
D.
các electron chuyển động rất nhanh cách xa hạt nhân.
Quan sát hình vẽ sau mô tả thí nghiệm tìm ra hạt nhân nguyên tử vào năm 1911 của nhà vật lý người New Zealand là E. Rutherford. Hãy cho biết phát biểu đúng?
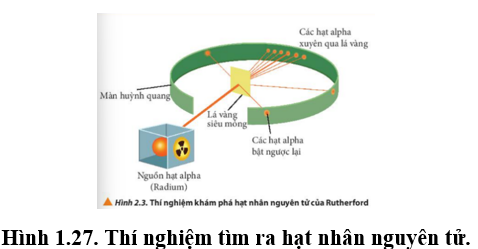
-
A.
Nguyên tử có cấu tạo rỗng nên các hạt α bật ngược trở lại.
-
B.
Hạt nhân nguyên tử mang điện tích âm nên hầu hết các hạt α xuyên qua lá vàng.
-
C.
Hạt nhân nguyên tử có kích thước rất lớn hơn với kích thước nguyên tử
-
D.
Nguyên tử có cấu tạo rỗng nên hầu hết các hạt α xuyên qua lá vàng.
Sự khác biệt cơ bản giữa mô hình Rutherford – Bohr và mô hình hiện đại về nguyên tử là
-
A.
electron chuyển động (Rutherford – Bohr) và electron không chuyển động (mô hình hiện đại).
-
B.
electron chuyển động theo những quỹ đạo giống như các hành tinh quay xung quanh Mặt trời (mô hình hiện đại) và electron chuyển động không theo quỹ đạo xác định (mô hình Rutherford – Bohr).
-
C.
electron chuyển động theo những quỹ đạo giống như các hành tinh quay xung quanh Mặt trời (mô hình Rutherford – Bohr) và electron chuyển động không theo quỹ đạo xác định (mô hình hiện đại).
-
D.
electron chuyển động xung quanh hạt nhân (mô hình Rutherford – Bohr) và electron chỉ chuyển động ở một khu vực nhất định bên ngoài hạt nhân (mô hình hiện đại).
Nguyên lí hay quy tắc nào bị vi phạm trong cấu hình theo ô orbital được cho dưới đây?
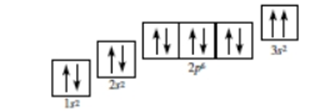
-
A.
Quy tắc của Hund.
-
B.
Không vi phạm nguyên lí, quy tắc nào.
-
C.
Nguyên lí Pauli.
-
D.
Quy tắc Klechkovski.
Mô hình cấu tạo ở hình bên dưới thuộc về nguyên tử nguyên tố nào?

Mô hình cấu tạo nguyên tử
-
A.
Carbon (Z = 6).
-
B.
Sodium (Z = 11).
-
C.
Oxygen (Z = 8).
-
D.
Lithium (Z = 3).







Danh sách bình luận