Khí hydrogen cháy trong không khí tạo thành nước theo phương trình hóa học sau:
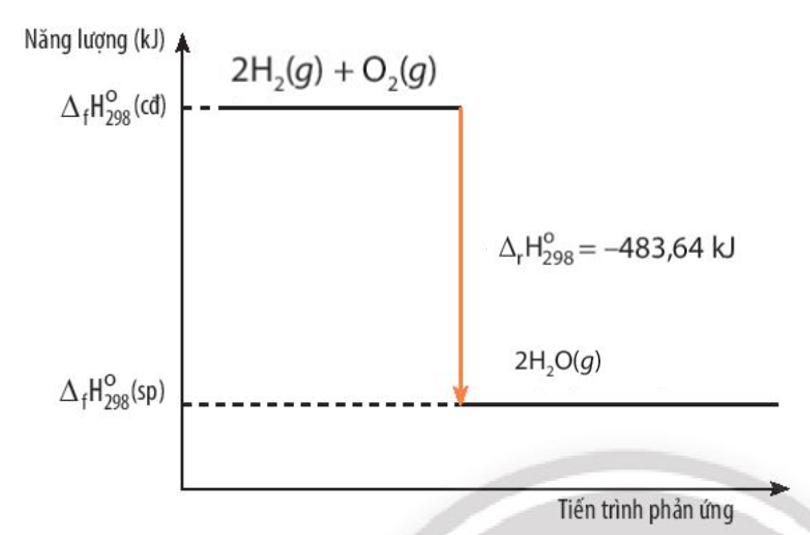
2H2(g) + O2(g) → 2H2O(g) \({\Delta _r}H_{298}^o\) = -483,64 kJ
a) Nước hay hỗn hợp của oxygen và hydrogen có năng lượng lớn hơn? Giải thích
b) Vẽ sơ đồ biến thiên năng lượng của phản ứng giữa hydrogen và oxygen
Áp dụng công thức: \({\Delta _r}H_{298}^o\)= \(\Sigma \)\({\Delta _f}H_{298}^o\)(sp) - \(\Sigma \)\({\Delta _f}H_{298}^o\)(bđ)
a) Xét phản ứng: 2H2(g) + O2(g) → 2H2O(g)
\({\Delta _r}H_{298}^o\)= \(\Sigma \)\({\Delta _f}H_{298}^o\)(sp) - \(\Sigma \)\({\Delta _f}H_{298}^o\)(bđ)
= 2.\({\Delta _f}H_{298}^o\)(H2O) - \({\Delta _f}H_{298}^o\)(O2) – 2. \({\Delta _f}H_{298}^o\)(H2) = -483,64 kJ < 0
=> Hỗn hợp của oxygen và hydrogen có năng lượng lớn hơn
b)

Các bài tập cùng chuyên đề
Từ số liệu Bảng 17.1, hãy xác định biến thiên enthalpy chuẩn của phản ứng đốt cháy ethane: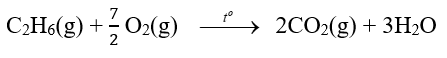
a) Cho biết năng lượng liên kết trong các phân tử O2, N2 và NO lần lượt là 494 kJ/mol, 945 kJ/mol và 607 kJ/mol. Tính biến thiên enthalpy chuẩn của phản ứng:
N2(g) + O2(g) → 2NO(g)
b) Giải thích vì sao nitrogen chỉ phản ứng với oxygen ở nhiệt độ cao hoặc khi có tia lửa điện.
Từ số liệu năng lượng liên kết ở Bảng 12.2, hãy tính biến thiên enthalpy của phản ứng đốt cháy butane theo năng lượng liên kết, biết sản phảm phản ứng đều ở thể khí.
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:

Biến thiên enthalpy của phản ứng C3H8(g) → CH4(g) + C2H4(g) có giá trị là
A. +103 kJ.
B. -103 kJ.
C. +80 kJ.
D. -80 kJ.
Methane là thành phần chính của khí thiên nhiên. Xét phản ứng đốt cháy methane:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) \({\Delta _r}H_{298}^o\) = -890,3 kJ
Biến nhiệt tạo thành chuẩn của CO2(g) và H2O(l) tương ứng là -393,5 và -285,8 kJ/mol.
Hãy tính nhiệt tạo thành chuẩn của khí methane.
Biết CH3COCH3có công thức cấu tạo:
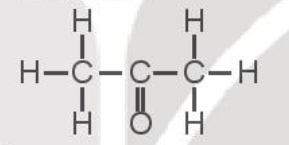
Từ số liệu năng lượng liên kết ở Bảng 12.2, hãy xác định biến thiên enthalpy của phản ứng đốt cháy acetone (CH3COCH3).
CH3COCH3(g) + 4O2(g) → 3CO2(g) + 3H2O (g)
Một bình gas (khí hóa lỏng) chứa hỗn hợp propane và butane với tỉ lệ mol 1:2. Xác định nhiệt lượng tỏa ra khi đốt cháy hoàn toàn 12 kg khí gas trên ở điều kiện chuẩn
Cho biết các phản ứng:
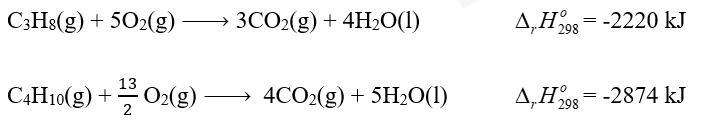
Trung bình mỗi ngày, một hộ gia đình cần đốt gas để cung cấp 10 000 kJ nhiệt ( hiệu suất hấp thụ nhiệt là 80%). Sau bao nhiêu ngày hộ gia đình trên sẽ sử dụng hết bình gas 12kg?
Tính ${\Delta _r},H_{298}^0$các phản ứng đốt cháy hoàn toàn 1 mol mỗi chất C2H4(g), C2H6(g), CO(g). Biết các sản phẩm thu được đều ở thể khí.
Cho phản ứng sau ở điều kiện chuẩn:
H-H(g) + F-F(g) -> 2H-F(g)
Tính năng lượng cần để phá vỡ các liên kết trong H2, F2 và năng lượng tỏa ra (theo kJ) khi hình thành liên kết trong HF cho phản ứng trên.
Xác định số lượng mỗi loại liên kết trong các phân tử trước và sau phản ứng của CH4 với Cl2.
Dựa vào năng lượng liên kết, tính ${\Delta _r},H_{298}^0$ các phản ứng sau:
a) Các phản ứng đốt cháy hoàn toàn 1 mol mỗi chất C2H4, C2H6, H2 ở thể khí.
b) F2(g) + H2O(g) → 2HF(g) + ½ O2(g)
Dự đoán các phản ứng trên là thuận lợi hay không thuận lợi.
Phản ứng quang hợp là phản ứng thu năng lượng dưới dạng ánh sáng:
6nCO2(g) + 6nH2O(l) → (C6H12O6)n(s) + 6nO2(g)
Hãy tính xem cần phải cung cấp bao nhiêu năng lượng dưới dạng ánh sáng cho phản ứng quang hợp để tạo thành 1 mol glucose C6H12O6(s), biết enthalpy tạo thành chuẩn của chất này là -1271,1 kJ.mol-1. Biến thiến enthalpy tạo thành chuẩn của các chất khác tra ở phụ lục 3, trang 119.
Cho phản ứng: N2(g) + 3H2(g) → 2NH3(g) ${\Delta _r},H_{298}^0$ = -92,22 kJ.
a) Trong nhà máy sản xuất NH3, ban đầu phải đốt nóng N2 và H2 để phản ứng diễn ra. Nhiệt tỏa ra từ phản ứng này lại được dùng để đốt nóng hỗn hợp N2 và H2 cho quá trình phản ứng tiếp theo. Cách làm này có ý nghĩa gì về khía cạnh kinh tế? Giải thích
b) Tính enthalpy tạo thành chuẩn của NH3.
Tính ${\Delta _r},H_{298}^0$ cho phản ứng sau dựa theo năng lượng liên kết.
CH4(g) + X2(g) → CH3X(g) + HX(g)
Với X = F, Cl, Br, I. Liên hệ giữa mức độ phản ứng (dựa theo ${\Delta _r},H_{298}^0$) với tính phi kim (F > Cl > Br > I). Tra các giá trị năng lượng liên kết của Phụ lục 2, trang 118
Khi đun bếp than, củi, để đun nấu nhanh hơn, người ta thường dùng quạt để thổi thêm không khí vào bếp. Cách làm này có làm thay đổi biến thiên enthalpy chuẩn của phản ứng C(s) + O2(g) → CO2(g) không? Giải thích.
Tính biến thiên enthalpy của phản ứng dựa vào năng lượng liên kết phải viết được công thức cấu tạo của tất cả các chất trong phản ứng để xác định số lượng và loại liên kết. Xác định số lượng mỗi loại liên kết trong các phân tử sau: CH4, CH3Cl, NH3, CO2.
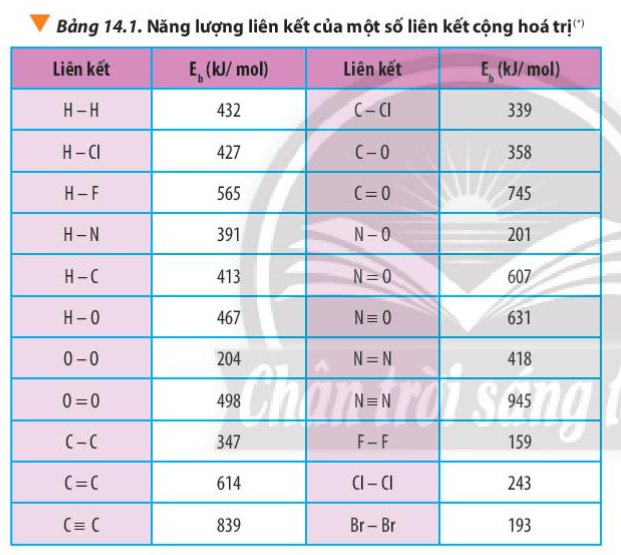
Dựa vào năng lượng liên kết ở Bảng 14.1, tính biến thiên enthalpy của phản ứng và giải thích vì sao nitrogen (N\( \equiv \)N) chỉ phản ứng với oxygen (O=O) ở nhiệt độ cao hoặc có tia lửa điện để tạo thành nitrogen monoxide (N=O).
N2(g) + O2(g) \(\xrightarrow{{{t^o}}}\) 2NO(g)
Xác định \({\Delta _r}H_{298}^o\) của phản ứng sau dựa vào giá trị Eb ở Bảng 14.1:
CH4(g) + Cl2(g) \(\xrightarrow{{askt}}\) CH3Cl(g) + HCl(g)
Hãy cho biết phản ứng trên tỏa nhiệt hay thu nhiệt?
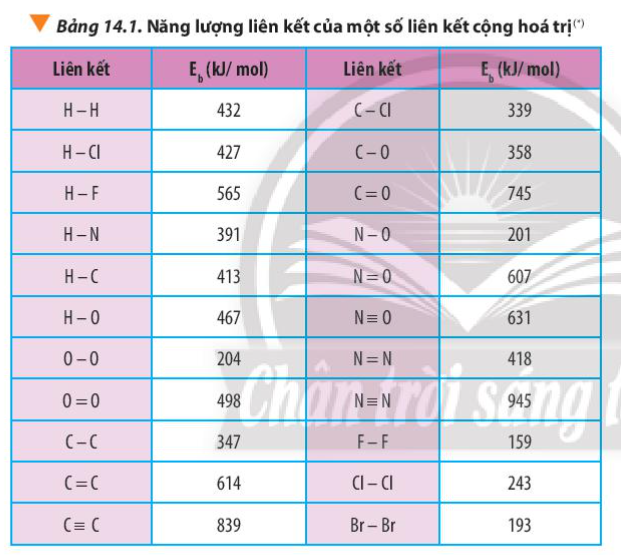
Dựa vào số liệu về năng lượng liên kết ở Bảng 14.1, hãy tính biến thiên enthalpy của 2 phản ứng sau:
2H2(g) + O2(g) \(\xrightarrow{{{t^o}}}\)2H2O(g) (1)
C7H16(g) + 11O2(g) \(\xrightarrow{{{t^o}}}\) 7CO2(g) + 8H2O(g) (2)
So sánh kết quả thu được, từ đó cho biết H2 hay C7H16 là nhiên liệu hiệu quả hơn cho tên lửa (biết trong C7H16 có 6 liên kết C-C và 16 liên kết C-H)

Tính \({\Delta _r}H_{298}^o\) của hai phản ứng sau:
3O2(g) → 2O3(g) (1)
2O3(g) → 3O2(g) (2)
Liên hệ giữa giá trị \({\Delta _r}H_{298}^o\) với độ bền của O3, O2 và giải thích, biết phân tử O3 gồm 1 liên kết đôi O=O và 1 liên kết đơn O-O
Tính biến thiên enthalpy của phản ứng phân hủy trinitroglycerin (C3H5O3(NO2)3), theo phương trình sau (biết nhiệt tạo thành của nitroglycerin là -370,15 kJ/mol):
4 C3H5O3(NO2)3(s) → 6N2(g) + 12CO2(g) + 10H2O(g) + O2(g)
Hãy giải thích vì sao trinitroglycerin được ứng dụng làm thành phần thuốc súng không khói
Giá trị biến thiên enthalpy của phản ứng có liên quan tới hệ số các chất trong phương trình nhiệt hóa học không? Giá trị enthalpy tạo thành thường được đo ở điều kiện nào?
Dựa vào giá trị enthalpy tạo thành ở Bảng 13.1, hãy tính giá trị \({\Delta _r}H_{298}^o\) của các phản ứng sau:
CS2(l) + 3O2(g) \(\xrightarrow{{{t^o}}}\) CO2(g) + 2SO2(g) (1)
4NH3(g) + 3O2 \(\xrightarrow{{{t^o}}}\) 2N2(g) + 6H2O(g) (2) \(\)
Tính \({\Delta _r}H_{298}^o\) của các phản ứng sau dựa theo năng lượng liên kết (sử dụng số liệu từ Bảng 14.1):
a) N2H4(g) → N2(g) + 2H2(g)
b) 4HCl(g) + O2(g) \(\xrightarrow{{{t^o}}}\) 2Cl2(g) + 2H2O(g)
Dựa vào Bảng 13.1, tính biến thiên enthalpy chuẩn của phản ứng đốt cháy hoàn toàn 1 mol benzene C6H6(l) trong khí oxygen, tạo thành CO2(g) và H2O(l). So sánh lượng nhiệt sinh ra khi đốt cháy hoàn toàn 1,0 g propane C3H8(g) với lượng nhiệt sinh ra khi đốt cháy hoàn toàn 1,0 g benzenne C6H6(l).
Cho phương trình nhiệt hóa học sau:
SO2(g) + ½ O2(g) \(\xrightarrow{{{t^o},{V_2}{O_5}}}\) SO3(g) \({\Delta _r}H_{298}^o\) = -98,5 kJ
a) Tính lượng nhiệt giải phóng ra khi chuyển 74,6 g SO2 thành SO3
b) Giá trị \({\Delta _r}H_{298}^o\) của phản ứng: SO3(g) → SO2(g) + ½ O2(g) là bao nhiêu?
Xét quá trình đốt cháy khí propane C3H8(g):
C3H8(g) + 5O2(g) \(\xrightarrow{{{t^o}}}\) 3CO2(g) + 4H2O(g)
Tính biến thiên enthalpy chuẩn của phản ứng dựa vào nhiệt tạo thành của hợp chất (Bảng 13.1) và dựa vào năng lượng liên kết (Bảng 14.1). So sánh hai giá trị đó và rút ra kết luận
Xét các phản ứng thế trong dãy halogen ở điều kiện chuẩn:
(1) F2(g) + NaCl(s) → NaF(s) + Cl2(g)
(2) Cl2(g) + NaBr(s) → NaCl(s) + Br2(l)
(3) Br2(l) + NaI(s) → NaBr(s) + I2(s)
(4) Cl2(g) + NaBr(aq) → NaCl(aq) + Br2(l)
Hay còn viết: Cl2(g) + Br−(aq) → Cl−(aq) + Br2(l)
(5) Br2(l) + NaI(aq) → NaBr(aq) + I2(s)
Hay còn viết: Br2(l) + I−(aq) → Br−(aq) + I2(s)
a) Từ các giá trị của enthalpy hình thành chuẩn, hãy tính biến thiên enthalpy chuẩn của các phản ứng thế trên.
|
Chất/ion |
NaF (s) |
NaI(s) |
Cl- (aq) |
Br- (aq) |
I- (aq) |
|
\({\Delta _f}H_{298}^0\) (kJmol-1) |
- 574, 0 |
-287,8 |
-167,2 |
-121,6 |
-55,2 |
(Các giá trị khác được cho trong Phụ lục 3, SGK Hóa học 10, Cánh Diều).
b) Nhận xét sự thuận lợi về phương diện nhiệt của các phản ứng thế trong dãy halogen. Kết quả này có phù hợp với quy luật biến đổi tính phi kim của dãy halogen trong bảng tuần hoàn các nguyên tố hóa học không?
Bằng cách tính biến thiên enthalpy chuẩn của quá trình sau dựa vào năng lượng liên kết, hãy chỉ ra ở điều kiện chuẩn, H3C – CH2 – OH hay H3C – O – CH3 bền hơn.
H3C – CH2 – OH (g) → H3C – O – CH3 (g)
Trong ngành công nghệ lọc hóa dầu, các alkane thường được loại bỏ hydrogen trong các phản ứng dehydro hóa để tạo ra những sản phẩm hydrocarbon không no có nhiều ứng dụng trong công nghiệp. Hãy tính biến thiên enthalpy chuẩn của các phản ứng sau dựa vào năng lượng liên kết. (Giá trị một số năng lượng liên kết được cho trong Phụ lục 2, SGK Hóa học 10, Cánh Diều)
a) H3C – CH2 – CH2 – CH3 → CH2 = CH – CH = CH2 + 2H2
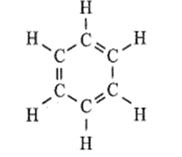
b) 6CH4 → C6H6 (1,3,5 – cyclohexatriene) + 9H2
Cho biết công thức cấu tạo của 1,3,5 – cyclohexatriene như sau:
Các phản ứng trên có thuận lợi về phương diện nhiệt hay không? Phản ứng theo chiều ngược lại có biến thiên enthalpy bằng bao nhiêu?







Danh sách bình luận