Em có nhận xét gì khi cặp electron chung trong liên kết lệch hẳn về một phía nguyên tử
- Cặp electron chung trong liên kết lệch hẳn về phía nguyên tử có độ âm điện lớn hơn
- Trong liên kết cộng hóa trị phân cực, cặp electron chung trong liên kết lệch hẳn về phía nguyên tử có độ âm điện lớn hơn
=> Nguyên tử có độ âm điện lớn hơn sẽ mang số oxi hóa âm, nguyên tử có độ âm điện nhỏ hơn sẽ mang số oxi hóa dương
- Ví dụ:
+ NH3: N có độ âm điện lớn hơn H => N trong NH3 có số oxi hóa = -3, H trong NH3 có số oxi hóa = +1
+ HCl: Cl có độ âm điện lớn H => Cl trong HCl có số oxi hóa = -1, H trong HCl có số oxi = +1

Các bài tập cùng chuyên đề
Dựa vào giá trị độ âm điện trong Bảng 6.2, dự đoán loại liên kết ( liên kết cộng hóa trị phân cực, liên kết cộng hóa trị không phân cực, liên kết ion) trong các phân tử MgCl2, AlCl3, HBr, O2, H2, NH3.
Cho dãy các oxide sau: Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7.
a) Độ phân cực của các liên kết trong dãy các oxide trên thay đổi như thế nào?
b) Dựa vào giá trị độ âm điện của các nguyên tố trong Bảng 6.2, cho biết loại liên kết ( ion, cộng hóa trị phân cực, cộng hóa trị không phân cực) trong từng phân tử oxide.
Dựa theo độ âm điện, hãy cho biết loại liên kết trong các phân tử: H2S, CH4, K2O, F2O, NaBr.
Vì sao liên kết cộng hóa trị trong các phân tử Cl2, O2, N2 là liên kết cộng hóa trị không phân cực?
Trong các phân tử HCl, NH3 và CO2, cặp electron chung lệch về phía nguyên tử nào? Giải thích
Xét phân tử H2O, những phát biểu nào sau đây là đúng?
A. Liên kết H - O là liên kết cộng hoá trị không phân cực.
B. Liên kết H - O là liên kết cộng hoá trị phân cực.
C. Cặp electron dùng chung trong liên kết H - O lệch về phía nguyên tử O.
D. Cặp electron dùng chung trong liên kết H - O lệch về phía nguyên tử H.
E. Cặp electron dùng chung trong liên kết H - O phân bố đều giữa hai nguyên tử.
G. Nguyên tử O còn hai cặp electron hoá trị riêng.
Ghép mỗi nguyên tử hoặc phân tử sau với một hoặc các đặc điểm tương ứng của nó: N2, Ar, CO, H2.
(1) Liên kết trong phân tử là liên kết cộng hoá trị không phân cực.
(2) Liên kết trong phân tử là liên kết cộng hoá trị phân cực.
(3) Các nguyên tử trong phân tử đều tuân theo quy tắc octet.
(4) Là khí trơ.
(5) Có hai cặp electron hoá trị riêng.
(6) Liên kết trong phân tử là liên kết đơn.
Dựa vào hiệu độ âm điện, hãy nối các liên kết hình thành giữa các nguyên tử cột A với loại liên kết tương ứng ở cột B.
|
Cột A |
Cột B |
|
a) Sr và F |
1. liên kết cộng hóa trị phân cực |
|
b) N và Cl |
2. liên kết cộng hóa trị không phân cực |
|
c) N và O |
3. liên kết ion |
Dựa vào hiệu độ âm điện giữa hai nguyên tố, cho biết liên kết trong phân tử nào sau đây là phân cực nhất.
A. HF. B. HCl. C. HBr. D. HI.
Số lượng cặp electron dùng chung trong các phân tử H2, O2, N2, F2 lần lượt là:
A. 1, 2, 3, 4.
B. 1, 2, 3, 1.
C. 2, 2, 2, 2.
D. 1, 2, 2, 1.
Hợp chất nào sau đây có liên kết cộng hoá trị phân cực?
A. H2.
B. CHCl3.
C. CH4.
D. N2.
Hợp chất nào sau đây có liên kết cộng hoá trị không phân cực?
A. LiCl.
B. CF2Cl2.
C. CHCl3.
D. N2.
a) Ở 25°C và 0,99 atm, khả năng tan của carbon dioxide (CO2) trong nước là 1,45 gam/L, kém hơn nhiều so với sulfur dioxide (SO2) là 94 gam/L. Giải thích nguyên nhân sự khác biệt.
b) Nhận xét độ tan của carbon dioxide trong nước theo nhiệt độ dựa trên đồ thị sau.
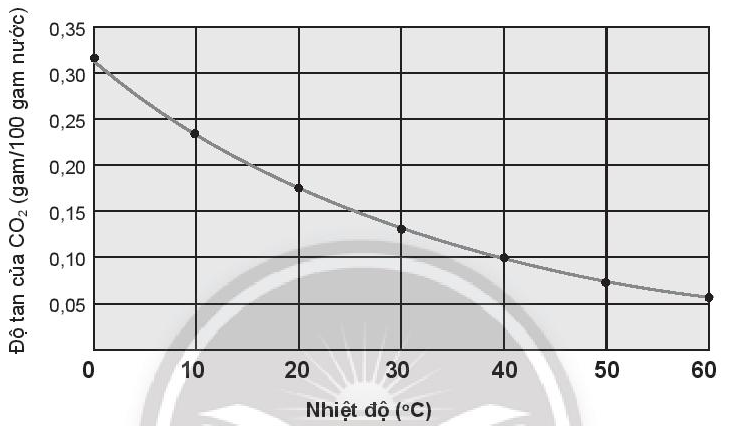
c) Nước giải khát có gas là gì? Vì sao người ta thường ướp lạnh các loại nước giải khát có gas trước khi sử dụng?
d) Vì sao trong những ngày hè nóng bức, cá thường phải ngoi lên mặt nước để thở, trong khi vào mùa lạnh, điều này không xảy ra?
Biết phân tử BF3 có cấu trúc phẳng, phân tử CCl4, có cấu trúc hình tứ diện đều. Hãy cho biết có bao nhiêu phân tử phân cực và không phân cực trong hình dưới đây? Giải thích.
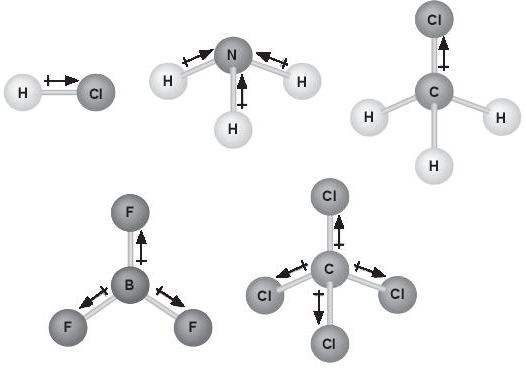
Các liên kết trong phân tử nitrogen được tạo thành do sự xen phủ của
A. các orbital s với nhau.
B. 2 orbital s và 1 orbital p với nhau.
C. 1 orbital s và 2 orbital p với nhau.
D. 3 orbital p giống nhau về hình dạng và kích thước, chỉ khác nhau về sự định hướng trong không gian.
Hợp chất nào sau đây chứa cả liên kết cộng hoá trị và liên kết ion?
A. CH2O.
B. CH4.
C. Na2O.
D. KOH.
|
Nguyên tố |
Độ âm điện |
Nguyên tố |
Độ âm điện |
|
Na |
0,93 |
O |
3,44 |
|
H |
2,20 |
Br |
2,96 |
|
C |
2,55 |
Cl |
3,16 |
|
N |
3,04 |
F |
3,98 |
Liên kết nào dưới đây là liên kết cộng hoá trị không phân cực?
A. Na-O.
B. O-H.
C. Na-C.
D. C-H.
Chất vừa có liên kết cộng hoá trị phân cực, vừa có liên kết cộng hoá trị không phân cực là
A. CO2.
B. H2O.
C. NH3.
D. C2F6.
Chất nào sau đây không có liên kết cộng hoá trị phân cực?
A. O2.
B. CO2.
C. NH3.
D. HCl.
Tổng số các phân tử có cực trong số các phân tử sau: Cl2, O2, CCl4, CO2 và SO2 là bao nhiêu?
A. 1.
B. 2.
C. 4.
D. 3.
Dựa vào giá trị của độ âm điện ở Bảng 6.2 trong sách giáo khoa Hóa học 10, hãy nêu bản chất liên kết trong các phân tử và ion sau: HClO, KHS, HCO3-, K2SO4.
Cho các chất sau: N2, H2, NH3, NaCl, HCl, H2O. Số chất mà phân tử chỉ chứa liên kết cộng hoá trị không phân cực là
A. 2. B. 4. C. 5. D. 3.
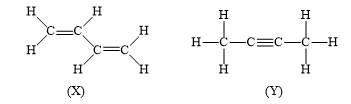
Cho hai chất hữu cơ X và Y có công thức cấu tạo sau:
Nhận xét nào sau đây là đúng?
A. X và Y có số liên kết σ và số liên kết π bằng nhau.
B. X có số liên kết σ và số liên kết π nhiều hơn Y.
C. X có số liên kết σ nhiều hơn, nhưng số liên kết π ít hơn Y.
D. X có số liên kết σ ít hơn, nhưng số liên kết π nhiều hơn Y.
Cho giá trị độ âm điện của một số nguyên tố sau: Na (0,93); Li (0,98), Mg (1,31); Al (1,61); P (2,19); S (2,58); Br (2,96) và C1 (3,16). Phân tử nào sau đây có liên kết ion
A. Na3P. B. MgS. C. AlCl3. D. LiBr.
: Liên kết ion khác với liên kết cộng hoá trị ở điểm nào sau đây?
A. Tính bão hoà lớp electron ở vỏ nguyên tử.
B. Tuân theo quy tắc octet.
C. Tạo ra hợp chất bền vững hơn.
D. Tính không định hướng.
Phát biểu nào sau đây không đúng về liên kết có trong phân tử HCl?
A. Giữa nguyên tử H và Cl có một liên kết đơn.
B. Các electron tham gia liên kết đồng thời bị hút về phía hai hạt nhân.
C. Phân tử có một moment lưỡng cực.
D. Một electron của nguyên tử hydrogen và một electron của nguyên tử chlorine được góp chung và cách đều hai nguyên tử.
Liên kết hóa học giữa các nguyên tử trong phân tử CH4 là loại liên kết nào sau đây (biết độ âm điện của nguyên tử H là 2,2 và C là 2,55)?
-
A.
Liên kết ion.
-
B.
Liên kết cộng hóa trị phân cực.
-
C.
Liên kết hiđro.
-
D.
Liên kết cộng hóa trị không phân cực.
Cho dãy các chất: O2, H2, NH3, KCl, HCl, H2O. Số chất trong dãy mà phân tử chỉ chứa liên kết cộng hóa trị không phân cực là
-
A.
3
-
B.
4
-
C.
5
-
D.
2







Danh sách bình luận