Hãy nêu công thức hóa học của hai hợp chất sodium và hai hợp chất potassium có nhiều ứng dụng trong thực tế mà em biết.
Dựa vào Hình 17.2.
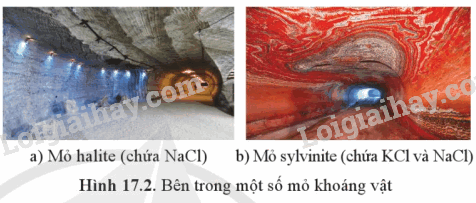
Hợp chất sodium:
+ NaCl có trong nước biển, dùng làm muối ăn, sản xuất sodium hydroxide, khí chlorine.
+ NaBr có trong rong biển, dùng để sản xuất bromie,…
Hợp chất potassium:
+ KCl có trong mỏ sylvinite dùng để sản xuất potassium hydroxide, khí chlorine.
+ KNO3 có trong phân kali dùng để làm phân bón cho cây trồng.

Các bài tập cùng chuyên đề
Tại sao các nguyên tố kim loại nhóm IA không tồn tại ở dạng đơn chất trong tự nhiên?
Một số đại lượng đặc trưng của các nguyên tố nhóm IA được trình bày trong Bảng 24.1.
Thực hiện các yêu cầu sau:
1. Nhận xét về xu hướng biến đổi bán kính nguyên tử của nguyên tố nhóm IA.
2. Cho biết: xu hướng biến đổi tính khử từ Li đến Cs; số oxi hoá đặc trưng của nguyên tử kim loại nhóm IA.
Các kim loại nhóm IA (nhóm kim loại kiềm) và hợp chất của chúng có nhiều ứng dụng như: sản xuất pin lithium, nước Javel, phân kali, tế bào quang điện, đồng hồ nguyên tử,....
Vậy, đơn chất nhóm IA có đặc điểm gì nổi bật về tính chất vật lí và tính chất hoá học? Các hợp chất nhóm IA quan trọng như xút, soda được sản xuất trong công nghiệp như thế nào?
Khi so sánh kim loại nhóm IA với các kim loại khác trong cùng chu kì, nhận định nào sau đây không đúng?
A. Có tính khử mạnh nhất. B. Có thế điện cực chuẩn âm nhất.
C. Có bán kính nguyên tử lớn nhất. D. Có nhiều electron hoá trị nhất.
Các kim loại kiềm khác nhau về những đặc điểm nào sau đây?
(1) Cấu hình electron của nguyên tử
(2) Số electron hóa trị của nguyên tử
(3) Số oxi hóa trong các hợp chất
(4) Mức độ thể hiện tính khử
Pháo hoa thường được sử dụng trong các dịp lễ, Tết. Để tạo màu cho pháo hoa, người ta dùng một số muối hay oxide kim loại, trong đó có hợp chất kim loại nhóm IA như lithium carbonate tạo màu đỏ, sodium nitrate tạo màu vàng,... Kim loại nhóm IA và hợp chất của chúng có những tính chất và ứng dụng nào?
Dựa vào cấu hình electron và bán kính nguyên tử (Bảng 17.1), hãy giải thích trong các hợp chất, kim loại nhóm IA đều thể hiện số oxi hoá +1.
Giải thích tại sao trong tự nhiên kim loại nhóm lA chỉ tồn tại ở dạng hợp chất.
Ở điều kiện thường các tinh thể kim loại nhóm IA đều có kiểu cấu trúc.
-
A.
Lập phương tâm khối.
-
B.
Lập phương tâm mặt.
-
C.
Lục phương.
-
D.
Lập phương đơn giản.
Để điều chế kim loại Na, người ta thực hiện phản ứng
-
A.
điện phân dung dịch NaOH.
-
B.
điện phân nóng chảy NaCl.
-
C.
cho dung dịch NaOH tác dụng với dung dịch HCl.
-
D.
cho dung dịch NaOH tác dụng với H2O.
Những đặc điểm chung nào của các kim loại kiềm (M) sau đây có thể giúp dự đoán chúng đều có tính khử mạnh?
(a) Kim loại M trong cặp oxi hóa – khử M+/M có thế điện cực chuẩn (\(E_{{M^ + }/M}^o\)) rất âm.
(b) Mềm và dễ nóng chảy.
(c) Có nhiều electron hóa trị nên dễ dàng nhường electron.
(d) Lực hút của hạt nhân đối với elctron hóa trị trong kim loại kiềm yếu hơn so với lực hút tương ứng ở các kim loại nhóm khác.
(e) Có cấu trúc tinh thể rỗng.
Những phát biểu nào sai đây là đúng về các nguyên tố nhóm IA.
(a) Có cấu hình electron lớp ngoài cùng là ns1 (n > 1).
(b) Có số oxi hóa là +1 hoặc +2 trong các hợp chất.
(c) Có tính khử mạnh.
(d) Có bán kính nguyên tử nhỏ.
(e) Còn được gọi là kim loại kiềm.
Trong tự nhiên, các nguyên tố nhóm IA chỉ tồn tại ở dạng hợp chất là do
A. các nguyên tố nhóm IA chỉ có thể tìm được trong nước ngầm, nước biển.
B. các nguyên tố nhóm IA đều là những kim loại hoạt động hóa học mạnh nên không tồn tại dạng đơn chất.
C. các nguyên tố nhóm IA thường kết hợp với nhau dể tạo thành các hợp kim bền.
D. các nguyên tố nhóm IA có độ âm điện lớn nên dễ dàng kết hợp với các nguyên tố khác.
Theo chiều tăng dần của điện tích hạt nhân nguyên tử, sự biến đổi tính chất của các nguyên tố nhóm IA nào sau đây đúng?
A. Bánh kính nguyên tử giảm dần.
B. Nhiệt độ nóng chảy tăng dần.
C. Độ cứng giảm dần.
D. Khối lượng riêng của đơn chất giảm dần.
Nguyên tử của các nguyên tố nhóm IA khác nhau về
A. số electron lớp ngoài cùng của nguyên tử
B. cấu hình electron nguyên tử
C. số oxi hóa của nguyên tử trong hợp chất
D. kiểu mạng tinh thể của đơn chất
Cho dãy các kim loại: Li, Na, Al, Ca, K và Rb. Số kim loại kiềm trong dãy là
A. 1 B. 2 C. 3 D. 4
Ở điều kiện thường các tinh thể kim loại nhóm IA đều có kiểu cấu trúc.
A. Lập phương tâm khối. B. Lập phương tâm mặt.
C. Lục phương. D. Lập phương đơn giản.
Ở trạng thái cơ bản nguyên tử K có cấu hình electron là [Ar]4s1. Trong bảng tuần hoàn, nguyên tố K thuộc nhóm.
A. IIIA. B. IA. C. IVA. D. IIA.
Kim loại Na ở chu kì 3, nhóm IA trong bảng tuần hoàn, cấu hình electron lớp ngoài cùng của nguyên tử Na ở trạng thái cơ bản là
A. 3s23p5. B. 3s2. C. 3s1. D. 3s23p1.
Trong tự nhiên, các nguyên tố nhóm IA chỉ tồn tại ở dạng hợp chất là do
A. các nguyên tố nhóm IA chỉ có thể tìm được trong nước ngầm, nước biển.
B. các nguyên tố nhóm IA đều là những kim loại hoạt động hóa học mạnh nên không tồn tại dạng đơn chất.
C. các nguyên tố nhóm IA thường kết hợp với nhau dể tạo thành các hợp kim bền.
D. các nguyên tố nhóm IA có độ âm điện lớn nên dễ dàng kết hợp với các nguyên tố khác.
Cho 15,6 gam một kim loại kiềm X tác dụng với nước (dư). Sau phản ứng thu được 4,958 lít khí (đkc). Phân tử khối của kim loại X bằng bao nhiêu?
Nguyên tố natri (sodium, Na) có số hiệu nguyên tử là 11 . Ở trạng thái cơ bản, cấu hình electron của ion \({\rm{N}}{{\rm{a}}^ + }\)là
-
A.
\(1{s^2}2{s^2}2{p^6}3{s^1}\).
-
B.
\(1{s^2}2{s^2}2{p^6}\).
-
C.
\(1{s^2}2{s^2}2{p^5}\).
-
D.
\(1{s^2}2{s^2}2{p^6}3{s^2}\).
Cấu hình electron của Sodium (Z = 11) là
-
A.
1s22s22p63s23p63d34s2
-
B.
1s22s22p63s1
-
C.
1s22s22p63s23p1
-
D.
1s22s22p6
Cho các cấu hình electron nguyên tử sau:
1) 1s22s22p63s1 2) 1s22s22p63s23p64s2 3) 1s22s1 4) 1s22s22p63s23p1
Các cấu hình đó lần lượt là của những nguyên tố:
-
A.
Ca (Z=20), Na(Z=11), Li(Z=3), Al(Z=13)
-
B.
Na(Z=11), Ca(Z=20), Li(Z=3), Al(Z=13)
-
C.
Na(Z=11), Li(Z=3), Al(Z=13), Ca(Z=20)
-
D.
Li(Z=3), Na(Z=11), Al(Z=13), Ca(Z=20)
Kim loại nào dưới đây là kim loại kiềm (thuộc nhóm IA)?
-
A.
Ba.
-
B.
Al.
-
C.
K.
-
D.
Ca.
Nguyên tố kim loại nhóm IA có cấu hình e lớp ngoài cùng là
-
A.
ns1.
-
B.
ns2.
-
C.
ns2np1.
-
D.
1s1.
Ở một số quốc gia, khoáng vật trona là nguyên liệu chính để sản xuất soda. Thành phần hóa học chính của khoáng vật trona là
-
A.
Na2CO3.NaHCO3.2H2O.
-
B.
3NaF.AlF3.
-
C.
NaNO3.
-
D.
NaCl.KCl.
Cho biết số hiệu nguyên tử của sodium là 11. Vị trí của sodium trong bảng tuần hoàn là
-
A.
chu kì 3, nhóm IA.
-
B.
chu kì 3, nhóm IB.
-
C.
chu kì 3, nhóm IIA.
-
D.
chu kì 2, nhóm IIA.
Kim loại nào sau đây thuộc nhóm IA trong bảng tuần hoàn?
-
A.
Ba.
-
B.
Fe.
-
C.
Na.
-
D.
Al.
Phân kali đỏ (chứa KCl ) là một loại phân bón đa lượng phổ biến trên thị trường vì giá thành rẻ, phù hợp rất nhiều loại đất khác nhau và hàm lượng potassium cao. Phân kali đỏ thường được sản xuất từ quặng sylvinite $\left( {{\rm{KCl}}.{\rm{NaCl}}} \right)$ bằng cách tách muối KCl ra khỏi quặng theo sơ đồ sau:
Quặng sylvinite → Dung dịch KCl bão hoà → Tinh thể KCl .
Phương pháp nào sau đây dùng để tách KCl ở trên?
-
A.
Sắc kí.
-
B.
Chưng cất.
-
C.
Chiết.
-
D.
Kết tinh.







Danh sách bình luận