Đề bài
Cho quá trình 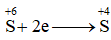 , đây là quá trình
, đây là quá trình
-
A.
oxi hóa.
-
B.
khử.
-
C.
nhận proton.
-
D.
tự oxi hóa khử.
Phương pháp giải
Dựa vào quá trình trao đổi electron của S
Lời giải của GV Loigiaihay.com
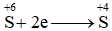
S đã nhận 2 electron => chất oxi hóa có quá trình khử
Đáp án B
Đáp án : B








Danh sách bình luận