Lý thuyết phản ứng hóa học - Khoa học tự nhiên 8 - Kết nối tri thức
Phản ứng hóa học là quá trình biến đổi từ chất này sang chất khác.
Tổng hợp đề thi học kì 2 lớp 8 tất cả các môn - Kết nối tri thức
Toán - Văn - Anh - Khoa học tự nhiên
I. Biến đổi vật lý và biến đổi hóa học
- Biến đổi vật lý là quá trình chuyển từ trạng thái này sang trạng thái khác mà không tạo thành chất mới. Ví dụ: quá trình hòa tan, đông đặc, …
- Biến đổi hóa học là quá trình biến đổi có sự tạo thành chất mới. Ví dụ: nung đá vôi, …
II. Phản ứng hóa học
1. Khái niệm
-
Phản ứng hóa học là quá trình biến đổi từ chất này sang chất khác.
-
Chất ban đầu bị biến đổi là chất phản ứng (chất tham gia ).
-
Chất mới sinh ra là chất sản phẩm.
-
Ví dụ:
Iron + Sulfur → Iron (II) sulfur
chất tham gia chất tham gia chất sản phẩm
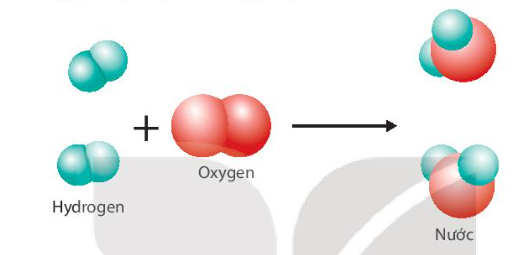
2. Diễn biến trong phản ứng hóa học
-
Trong các phản ứng hóa học, xảy ra sự phá vỡ các liên kết trong phân tử chất đầu, hình thành các liên kết mới tạo ra các phân tử mới.
3. Hiện tượng kèm theo các phản ứng hóa học
-
Phản ứng hóa học xảy ra khi có chất mới được tạo thành có tính chất mới khác với chất ban đầu.
-
Dấu hiệu nhận biết: thay đổi màu sắc, có chất khí, kết tủa,...
III. Năng lượng của phản ứng hóa học
1. Phản ứng tỏa nhiệt, phản ứng thu nhiệt
- Phản ứng tỏa nhiệt giải phóng năng lượng (dạng nhiệt) ra môi trường xung quanh. Ví dụ: Phản ứng đốt cháy đèn cồn.
- Phản ứng thu nhiệt nhận năng lượng (dạng nhiệt) trong quá trình phản ứng. Vì dụ: Phản ứng phân hủy copper(II) hydroxide.
2. Ứng dụng của phản ứng tỏa nhiệt
-
Cung cấp năng lượng cho sinh hoạt, sản xuất, vận hành động cơ, thiết bị, phương tiện giao thông….
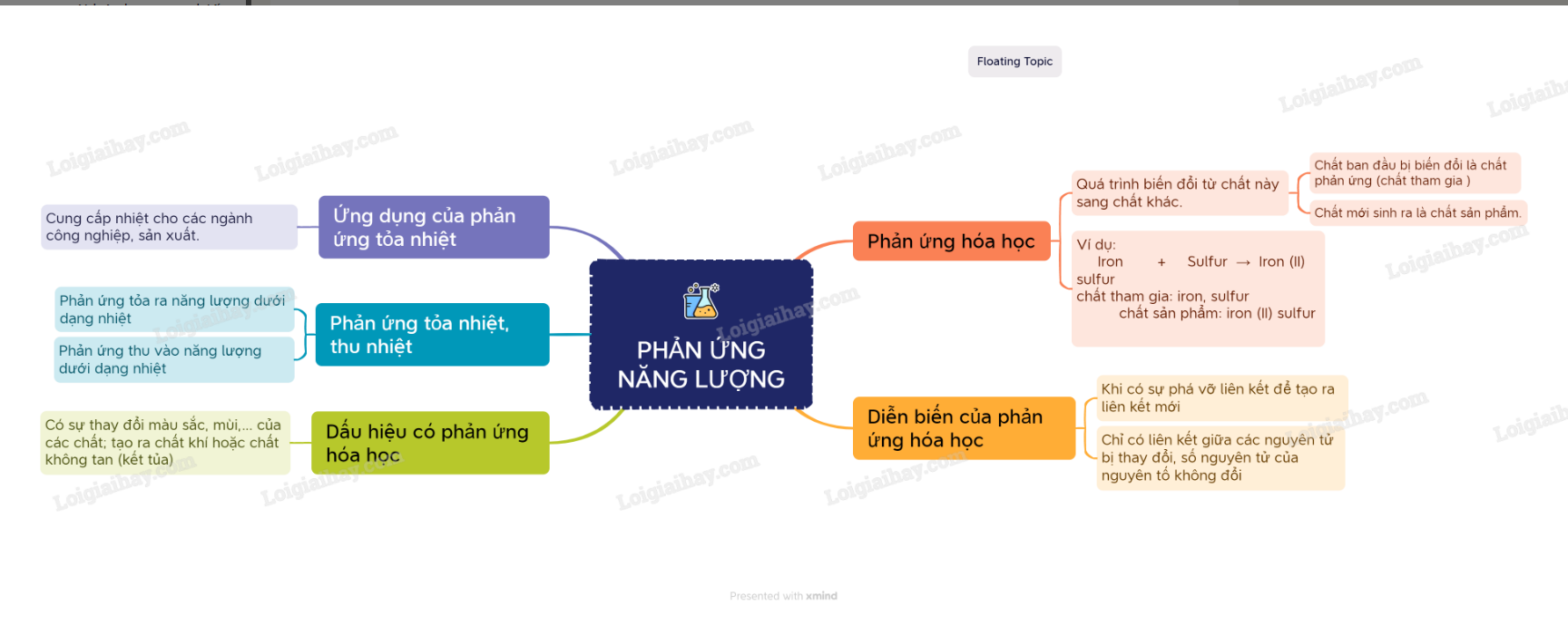
SƠ ĐỒ TƯ DUY
Luyện Bài Tập Trắc nghiệm KHTN 8 - Kết nối tri thức - Xem ngay
Các bài khác cùng chuyên mục
- Lý thuyết Bảo vệ môi trường - Khoa học tự nhiên 8 Kết nối tri thức
- Lý thuyết Cân bằng tự nhiên - Khoa học tự nhiên 8 Kết nối tri thức
- Lý thuyết Sinh quyển - Khoa học tự nhiên 8 Kết nối tri thức
- Lý thuyết Hệ sinh thái - Khoa học tự nhiên 8 Kết nối tri thức
- Lý thuyết Quần xã sinh vật - Khoa học tự nhiên 8 Kết nối tri thức












Danh sách bình luận