Lý thuyết bài 12: Liên kết Hydrogen và tương tác Van der waals
Liên kết Hydrogen và tương tác Van der waals
Lý thuyết: Liên kết Hydrogen và tương tác Van der waals
I. Liên kết hydrogen
Các phân tử nước cũng như một số phân tử khác chứa hydrogen như HF, NH3, … có thể liên kết được với nhau bởi liên kết hydrogen.
1. Khái niệm:
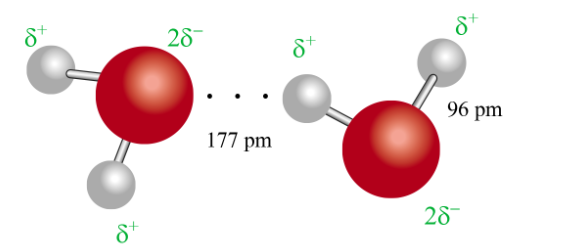
Liên kết hydrogen là một loại liên kết yếu được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron hóa trị riêng.
Liên kết hydro giữa hai phân tử nước
Các nguyên tử có độ âm điện lớn thường gặp: N, O, F
- Liên kết hydrogen thường được kí hiệu là dấu ba chấm (….) rải đều từ nguyên tử H đến nguyên tử tạo liên kết hydrogen với nó.
Trong đó X, Y là các nguyên tử N, O, F
2. Ảnh hưởng của liên kết hydrogen tới tính chất vật lí của nước
a) Đặc điểm tập hợp:
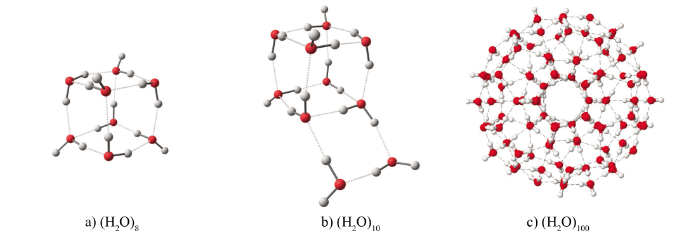
Phân tử nước tập hợp với nhau thành một cụm phân tử.
Một số cụm phân tử nước
b) Nhiệt độ nóng chảy và nhiệt độ sôi
- Phân tử nước liên kết chặt chẽ với nhau bởi các liên kết hydrogen => nhiệt độ sôi và nhiệt độ nóng chảy cao hơn so với nhiều chất có khối lượng phân tử lớn hơn nước.
II. Tương tác Van der waals
1. Khái niệm:
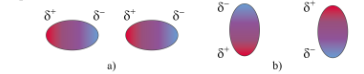
Là một loại liên kết yếu, hình thành do tương tác hút tĩnh điện giữa các cực trái dấu của phân tử
Các khả năng tương tác hút tĩnh điện giữa các cực trái dấu của hai phân tử
2. Ảnh hưởng của tương tác van der waals tới tính chất vật lí của các chất
- Tương tác van der waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi các chất, nhưng ảnh hưởng yếu hơn hydrogen
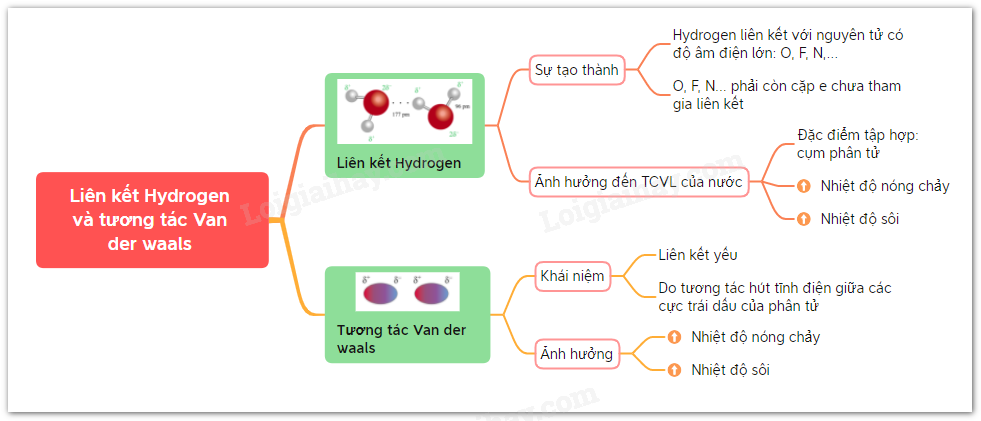
Sơ đồ tư duy





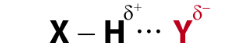







Danh sách bình luận