 Giải bài tập hóa học 9, Hóa 9 - Để học tốt hóa học 9
Giải bài tập hóa học 9, Hóa 9 - Để học tốt hóa học 9
 Đề kiểm tra 45 phút (1 tiết) - Chương 5 - Hóa học 9
Đề kiểm tra 45 phút (1 tiết) - Chương 5 - Hóa học 9
Đề kiểm tra 45 phút (1 tiết) – Đề số 9 – Chương 5 – Hóa học 9
Đáp án và lời giải chi tiết đề thi kiểm tra 45 phút (1 tiết) – Đề số 9 – Chương 5 – Hóa học 9
Đề bài
(10 câu: mỗi câu 1 điểm)
Câu 1: Công thức phân tử của glucozo, saccarozo, axit gluconic, tinh bột lần lượt là:
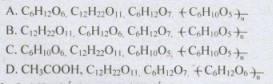
Câu 2: Một chất hữu cơ X khi đốt cháy 0,1 mol X thu được 0,6 mol CO2. X là
A.C2H6 B.C2H5OH
C.CH3COOH D.C6H12O6
Câu 3: Cho sơ đồ: Glucozo (1) -> rượu etylic (2) -> axit axetic
Điều kiện ở các quá trình (1), (2) lần lượt là:
A.men rượu, men giấm
B.nước, axit
C.không khí, xúc tác
D.Ag2O/NH3
Câu 4: Để phân biệt glucozo với saccarozo người ta dùng dung dịch
A.NaOH B.C2H5OH
C.Ag2O/NH3 D.CH3COOH
Câu 5: Khi lên men glucozo, lượng C2H5OH thu được là 4,6 gam thì thể tích khí CO2 thoát ra bằng (đktc, C = 12, O = 16, H = 1)
A.4,28 lít B.2,24 lít
C.5,6 lít D.4,48 lít
Câu 6: Cho các chất: C2H5OH, CH3COOH, C6H12O6, (C17H35COO)3C3H5, CH3 – COO – C2H5. Những chất có phản ứng thủy phân là:
\(\eqalign{ & A.{C_2}{H_5}OH,C{H_3}COOH,{C_6}{H_{12}}{O_6} \cr & B.{C_2}{H_5}OH,C{H_3}COOH,C{H_3} - COO - {C_2}{H_5} \cr & C.{C_2}{H_5}OH,{({C_{17}}{H_{35}}COO)_3}{C_3}{H_5},{C_6}{H_{12}}{O_6} \cr & D.{({C_{17}}{H_{35}}COO)_3}{C_3}{H_5},C{H_3} - COO - {C_2}{H_5} \cr} \)
Câu 7: Một chất hữu cơ có công thức đơn giản nhất là CH2O. Khối lượng mol phân tử trong khoảng 175 gam và 190 gam.
Công thức phân tử của chất đó là: (Ch H = 1, C = 12, O = 16)
A.C2H4O2 B.C5H10O5
C.C6H12O6 D.(C6H10O5)n
Câu 8: Để nhận biết các dung dịch: rượu etylic, axit axetic, glucozo người ta có thể dùng chất nào trong các chất sau?
A.quỳ tím và kẽm
B.CaCO3 và AgNO3 trong NH3
C.AgNO3 trong NH3
D.Bạc và HCl
Câu 9: Lên men 18 gam glucozo với hiệu suất 40%. Thể tích dung dịch rượu etylic 100 thu được là: (biết \({D_{{C_2}{H_5}OH}} = 0,8g.ml,\)\(\,H = 1,C = 12,O = 16)\)
A.46ml B.92ml
C.460ml D.23ml
Câu 10: Lượng C6H12O6 có trong 150ml dung dịch glucozo 3% (cho dung dịch glucozo khối lượng riêng = 1g/cm3, H = 1, C = 12, O = 16) là
A.5,0 gam B.4,5 gam
C.4 gam D.30 gam.
Lời giải chi tiết
1.Đáp án
|
Câu |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
Đáp án |
A |
D |
A |
C |
B |
D |
C |
B |
A |
B |
2.Lời giải
Câu 1: (A)
Công thức phân tử của glucozo, saccarozo, axit gluconic, tinh bột lần lượt là: C6H12O6, C12H22O11, C6H12O7, (C6H10O5)n.
Câu 2: (D)
Phân tử chất X có 6 nguyên tử C phải là C6H12O6.
Câu 3: (A)
Gluconic (1) \(\to\) rượu etylic (2) \(to\) axit axetic.
Điều kiện ở các quá trình (1), (2) lần lượt là:men rượu, men giấm.
Câu 4: (C)
Glucozo tác dụng với dung dịch Ag2O/NH3 cho Ag.
Saccarozo không tác dụng với dung dịch Ag2O/NH3.
Câu 5: (B)
Glucozo lên men cho C2H5OH và CO2 có số mol bằng nhau.
\(\eqalign{ & {n_{{C_2}{H_5}OH}} = {{4,6} \over {46}} = 0,1mol. \cr & \Rightarrow {V_{C{O_2}}} = 2,24lit(dktc). \cr} \)
Câu 6: (D)
Những chất có phản ứng thủy phân:
(C17H35COO)3C3H5, CH3 – COO – C2H5.
Câu 7: (C)
Công thức phân tử (CH2O)n. Khối lượng mol phân tử trong khoảng \(175 < 30n<190\)
\( \Rightarrow 5,8 < n < 6,33 \Rightarrow n = 6.\)
Vậy CTPT là: C6H12O6.
Câu 8: (B)
AgNO3 trong NH3 nhận ra glucozo, CaCO3 nhận ra axit axetic.
Câu 9: (A)
\(\eqalign{ & {C_6}{H_{12}}{O_6} \to 2{C_2}{H_5}OH + 2C{O_2} \cr & {V_{{C_2}{H_5}OH}} = {{18} \over {180.0,8}}.0,4.2.46 = 4,6ml \cr & \Rightarrow {V_{{C_2}{H_5}OH}}({10^0}) = 4,6.10 = 46ml \cr} \)
Câu 10: (B)
Khối lượng dung dịch C6H12O6 \(= 150\; g\)
\(\Rightarrow \) Khối lượng C6H12O6 \(= 150.0,03 = 4,5 g\).
Loigiaihay.com
- Đề kiểm tra 45 phút (1 tiết) – Đề số 10 – Chương 5 – Hóa học 9
- Đề kiểm tra 45 phút (1 tiết) – Đề số 11 – Chương 5 – Hóa học 9
- Đề kiểm tra 45 phút (1 tiết) – Đề số 8 – Chương 5 – Hóa học 9
- Đề kiểm tra 45 phút (1 tiết) – Đề số 7 – Chương 5 – Hóa học 9
- Đề kiểm tra 45 phút (1 tiết) – Đề số 6 – Chương 5 – Hóa học 9
>> Xem thêm
Các bài khác cùng chuyên mục
- Đề số 9 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 8 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 7 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 6 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Phương pháp giải bài tập về độ rượu
- Đề số 9 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 8 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 7 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Đề số 6 - Đề kiểm tra giữa học kì I - Hóa học 9 có đáp án và lời giải chi tiết
- Phương pháp giải bài tập về độ rượu











