Câu hỏi
Cho 4,68 gam hỗn hợp X gồm Cu và Fe3O4 tác dụng hết với 500 ml dung dịch HCl 0,1M (dư 25% so với lượng cần phản ứng) thu được dung dịch Y và một phần chất rắn không tan. Thêm dung dịch AgNO3 đến dư vào bình phản ứng, thu được kết tủa Z. Biết rằng sản phẩm khử của N+5 là khí NO, các phản ứng xảy ra hoàn toàn. Khối lượng của kết tủa Z là
- A 7,985 gam.
- B 18,785 gam.
- C 17,350 gam.
- D 18,160 gam.
Phương pháp giải:
Lượng HCl dư 25% so với lượng cần phản ứng nên tính được lượng HCl đã phản ứng.
HCl chỉ phản ứng với Fe3O4 theo PTHH: Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
=> nFe3O4 = nHCl pư/8 = ? => mCu
Do Cu dư nên sau phản ứng tạo muối Fe2+.
Xác định thành phần của dd Y.
Khi cho AgNO3 dư vào bình thì chú ý có cả Cu.
Bảo toàn electron tìm được số mol Ag. BTNT Cl tìm được số mol AgCl.
Từ đó tính được khối lượng kết tủa thu được.
Lời giải chi tiết:
nHCl đã dùng = 0,05 mol
Đặt nHCl pư = x mol
Lượng HCl dư 25% so với lượng cần phản ứng nên ta có: nHCl đã dùng = nHCl pư + nHCl dư
hay 0,05 = x + 25%.x = 0,05 => x = 0,04 mol
HCl chỉ phản ứng với Fe3O4 theo PTHH: Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
=> nFe3O4 = nHCl pư/8 = 0,005 mol
=> mCu = mX - mFe3O4 = 4,68 - 0,005.232 = 3,52 gam => nCu = 0,055 mol
Do Cu dư nên sau phản ứng tạo muối Fe2+.
Dung dịch Y gồm: \(\left\{ \matrix{
F{e^{2 + }}:0,015(BTNT:Fe) \hfill \cr
C{u^{2 + }} \hfill \cr
{H^ + }:0,01 \hfill \cr
C{l^ - }:0,05 \hfill \cr} \right.\)
BTĐT => nCu2+(dd Y) = (nCl- - 2nFe2+ - nH+)/2 = (0,05 - 0,015.2 - 0,01)/2 = 0,005 mol
=> nCu dư = nCu bđ - nCu2+(dd Y) = 0,055 - 0,005 = 0,05 mol
Khi cho AgNO3 dư vào bình phản ứng (chú ý bình có cả Cu):
nNO = nH+/4 = 0,0025 mol
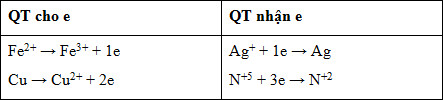
BTe: nFe2+ + 2nCu = nAg + 3nNO => 0,015 + 2.0,05 = nAg + 3.0,0025 => nAg = 0,1075 mol
Như vậy kết tủa gồm: Ag (0,1075 mol) và AgCl (0,05 mol)
=> m kết tủa = 0,1075.108 + 0,05.143,5 = 18,785 gam
Đáp án B







