Đề thi học kì 2 Hóa 9 - Đề số 4
Tổng hợp đề thi học kì 2 lớp 9 tất cả các môn
Toán - Văn - Anh - Lí - Hóa - Sinh - Sử - Địa - GDCD
Đề bài
Ứng dụng nào sau đây không phải ứng dụng của etilen?
-
A.
Điều chế PE.
-
B.
Điều chế rượu etylic
-
C.
Điều chế khí ga.
-
D.
Dùng để ủ trái cây mau chín.
Rượu etylic và axit axetic đều tác dụng được với
-
A.
Na2CO3.
-
B.
NaOH.
-
C.
NaCl.
-
D.
Na.
Đun nóng axit axetic với rượu etylic có axit sunfuric làm xúc tác thì người ta thu được một chất lỏng không màu, mùi thơm, không tan trong nước và nổi trên mặt nước. Sản phẩm đó là
-
A.
metyl clorua.
-
B.
natri axetat.
-
C.
etyl axetat.
-
D.
etilen
Dãy các chất nào sau đây đều làm mất màu dung dịch brom?
-
A.
CH4 ; C6H6.
-
B.
C2H4 ; C2H6.
-
C.
CH4 ; C2H4
-
D.
C2H4 ; C2H2.
Chọn câu đúng trong các câu sau:
-
A.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất có trong tự nhiên.
-
B.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất của cacbon.
-
C.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất hữu cơ.
-
D.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các chất trong cơ thể sống.
Chất hữu cơ X khi thủy phân trong dung dịch H2SO4 loãng thì thu được 1 sản phẩm duy nhất, X là :
-
A.
Tinh bột
-
B.
Chất béo
-
C.
Protein
-
D.
Etyl axetat
Xà phòng được điều chế bằng cách nào?
-
A.
Phân hủy chất béo.
-
B.
Thủy phân chất béo trong môi trường axit.
-
C.
Hòa tan chất béo trong dung môi hữu cơ.
-
D.
Thủy phân chất béo trong môi trường kiềm.
Nguyên tố X có cấu tạo như sau: điện tích hạt nhân là 11+, 3 lớp electron, lớp ngoài cùng có 1 electron. Tính chất hóa học cơ bản của X là
-
A.
Tính kim loại mạnh.
-
B.
Tính phi kim mạnh.
-
C.
X là khí hiếm.
-
D.
Tính kim loại yếu.
Đốt cháy chất hữu cơ X (X là một trong số các chất tinh bột, saccarozơ, glucozơ, protein) thấy sản phẩm tạo ra là CO2, H2O và N2. Vậy X có thể là
-
A.
tinh bột.
-
B.
saccarozơ.
-
C.
glucozơ.
-
D.
protein.
Ứng dụng nào không phải là ứng dụng của glucozơ?
-
A.
Làm thực phẩm dinh dưỡng và thuốc tăng lực
-
B.
Tráng gương, tráng phích
-
C.
Nguyên liệu sản xuất rượu etylic
-
D.
Nguyên liệu sản xuất PVC
Tính chất nào không phải của benzen ?
-
A.
Tác dụng với Br2 (to, Fe).
-
B.
Tác dụng với HNO3 /H2SO4 (đ).
-
C.
Tác dụng với dung dịch KMnO4.
-
D.
Tác dụng với Cl2 (as).
Một số protein tan được trong nước tạo thành dung dịch keo, khi đun nóng hoặc cho thêm hóa chất vào dung dịch này thường xảy ra kết tủa protein. Hiện tượng đó gọi là
-
A.
sự oxi hóa.
-
B.
sự khử.
-
C.
sự cháy.
-
D.
sự đông tụ
Công thức phân tử của saccarozơ là
-
A.
C6H12O6
-
B.
C6H12O7
-
C.
C12H22O11
-
D.
(-C6H10O5-)n
Trong các khí sau : CH4, H2, Cl2, O2. Khí nào khi trộn với nhau tạo ra hỗn hợp nổ ?
-
A.
CH4 và Cl2.
-
B.
H2 và O2.
-
C.
CH4 và O2.
-
D.
cả B và C đều đúng
Cho rượu etylic nguyên chất tác dụng với kali dư. Số phản ứng hóa học xảy ra là
-
A.
1.
-
B.
2.
-
C.
3.
-
D.
4.
Số công thức cấu tạo của C4H10 là
-
A.
1
-
B.
3
-
C.
2
-
D.
4
Một hợp chất X chứa 3 nguyên tố C, H, O có tỉ lệ khối lượng mC : mH : mO = 21 : 2 : 4. Hợp chất X có công thức đơn giản nhất trùng với CTPT. CTPT X là:
-
A.
C7H8O
-
B.
C8H10O
-
C.
C6H6O2
-
D.
C7H8O2.
Một hợp chất hữu cơ Y khi đốt cháy hoàn toàn thu được CO2 và H2O có số mol bằng nhau. Đồng thời số mol oxi tối thiểu cần dùng bằng 4 lần số mol của Y. Biết trong Y chỉ chứa 1 nguyên tử O. Công thức phân tử của Y là
-
A.
C2H6O
-
B.
C4H8O
-
C.
C3H6O
-
D.
C3H8O.
Đốt cháy hoàn toàn một ankan thu được 2,24 lít khí CO2 và 3,6 gam H2O. Công thức phân tử của ankan là
-
A.
CH4.
-
B.
C2H6.
-
C.
C3H8.
-
D.
C4H10.
Cho các hợp chất sau: CH4, C2H6, C2H4, H2. Có bao nhiêu chất tác dụng với dung dịch nước brom ở nhiệt độ thường?
-
A.
1
-
B.
2
-
C.
3
-
D.
4
Có 3 bình, mỗi bình chứa 1 trong các khí sau: metan, axetilen, khí cacbonic. Đánh số A, B, C vào các bình này và tiến hành các thí nghiệm với từng chất khí. Kết quả thí nghiệm được ghi ở bảng sau:
|
Thuốc thử |
A |
B |
C |
|
Dung dịch brom |
Không hiện tượng |
Mất màu |
Không hiện tượng |
|
Dung dịch nước vôi trong |
Không hiện tượng |
Không hiện tượng |
Vẩn đục |
Hãy cho biết 3 bình A, B, C chứa lần lượt những khí nào?
-
A.
Bình A chứa axetilen, bình B chứa metan, bình C chứa cacbonic.
-
B.
Bình A chứa metan, bình B chứa axetilen, bình C chứa cacbonic.
-
C.
Bình A chứa axetilen, bình B chứa cacbonic, bình C chứa metan.
-
D.
Bình A chứa cacbonic, bình B chứa metan, bình C chứa axetilen.
Tính khối lượng benzen cần dùng để điều chế 23,55 gam brombenzen. Biết hiệu suất phản ứng đạt 85%.
-
A.
11,7 gam.
-
B.
13,77 gam.
-
C.
14,625 gam.
-
D.
9,945 gam
Thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 13,8 gam rượu etylic nguyên chất là
-
A.
5,60.
-
B.
22,4.
-
C.
8,36.
-
D.
20,16.
Thể tích ancol etylic 92o cần dùng là bao nhiêu để điều chế được 2,24 lít C2H4 (đktc). Cho biết hiệu suất phản ứng đạt 62,5% và D = 0,8 g/ml.
-
A.
8 ml
-
B.
10 ml
-
C.
12,5 ml
-
D.
3,9 ml
Giấm ăn là dung dịch của axit axetic trong nước, trong đó nồng độ axit axetic từ 2-5%. Lượng axit axetic tối thiểu có trong 1 lít giấm ăn (Dgiấm ăn = 1,01 g/ml) là
-
A.
2,20 gam
-
B.
20,2 gam
-
C.
12,2 gam
-
D.
19,2 gam
Lên men m gam glucozơ với hiệu suất 90%, lượng khí CO2 sinh ra hấp thụ hết vào dung dịch nước vôi trong, thu được 10 gam kết tủa. Khối lượng dung dịch sau phản ứng giảm 3,4 gam so với khối lượng nước vôi trong ban đầu. Giá trị của m là
-
A.
20
-
B.
30
-
C.
12
-
D.
15
Để tráng bạc một số ruột phích, người ta phải thuỷ phân 34,2 gam saccarozơ rồi tiến hành phản ứng tráng gương. Tính lượng Ag tạo thành sau phản ứng, biết hiệu suất cả quá trình tráng gương là 80%?
-
A.
27,64 gam
-
B.
43,90 gam
-
C.
34,56 gam
-
D.
56,34 gam
Thủy phân 1 kg sắn chứa 20% tinh bột trong môi trường axit. Với hiệu suất phản ứng 85%, lượng glucozơ thu được là
-
A.
261,43 gam.
-
B.
200,8 gam.
-
C.
188,89 gam.
-
D.
192,5 gam.
Trùng hợp 22,4 lít C2H4 (đktc), nếu hiệu suất phản ứng là 80% thì khối lượng polime thu được là bao nhiêu? Biết hệ số trùng hợp là 500.
-
A.
2,24 gam
-
B.
4,48 gam
-
C.
2,80 gam
-
D.
3,36 gam
Trùng hợp 0,5 tấn etilen với hiệu suất 90% thì khối lượng polietilen thu được là
-
A.
0,5 tấn.
-
B.
5 tấn.
-
C.
4,5 tấn.
-
D.
0,45 tấn.
Lời giải và đáp án
Ứng dụng nào sau đây không phải ứng dụng của etilen?
-
A.
Điều chế PE.
-
B.
Điều chế rượu etylic
-
C.
Điều chế khí ga.
-
D.
Dùng để ủ trái cây mau chín.
Đáp án : C
Ứng dụng không phải của etilen là: Điều chế khí ga.
Rượu etylic và axit axetic đều tác dụng được với
-
A.
Na2CO3.
-
B.
NaOH.
-
C.
NaCl.
-
D.
Na.
Đáp án : D
Xem lại tính chất hóa học của rượu etylic và axit axetic
Rượu etylic và axit axetic đều tác dụng được với kim loại Na
2C2H5OH + 2Na → 2C2H5ONa + H2
2CH3COOH + 2Na → 2CH3COONa + H2
Đun nóng axit axetic với rượu etylic có axit sunfuric làm xúc tác thì người ta thu được một chất lỏng không màu, mùi thơm, không tan trong nước và nổi trên mặt nước. Sản phẩm đó là
-
A.
metyl clorua.
-
B.
natri axetat.
-
C.
etyl axetat.
-
D.
etilen
Đáp án : C
PTHH: CH3COOH + C2H5-OH $\overset{{{H}_{2}}\text{S}{{O}_{4\,d,{{t}^{o}}}}}{\mathop{\rightleftarrows }}\,$ CH3COOC2H5 + H2O
=> sản phẩm thu được là: etyl axetat
Dãy các chất nào sau đây đều làm mất màu dung dịch brom?
-
A.
CH4 ; C6H6.
-
B.
C2H4 ; C2H6.
-
C.
CH4 ; C2H4
-
D.
C2H4 ; C2H2.
Đáp án : D
2 chất đều làm mất màu dung dịch brom là: C2H4 ; C2H2.
Chọn câu đúng trong các câu sau:
-
A.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất có trong tự nhiên.
-
B.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất của cacbon.
-
C.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất hữu cơ.
-
D.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các chất trong cơ thể sống.
Đáp án : C
Câu đúng là: Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất hữu cơ
Chất hữu cơ X khi thủy phân trong dung dịch H2SO4 loãng thì thu được 1 sản phẩm duy nhất, X là :
-
A.
Tinh bột
-
B.
Chất béo
-
C.
Protein
-
D.
Etyl axetat
Đáp án : A
Chất hữu cơ X khi thủy phân trong dung dịch H2SO4 loãng thì thu được 1 sản phẩm duy nhất, X là tinh bột
(-C6H10O5-)n + nH2O $\xrightarrow{axit,\,{{t}^{o}}}$ nC6H12O6 (glucozơ)
Xà phòng được điều chế bằng cách nào?
-
A.
Phân hủy chất béo.
-
B.
Thủy phân chất béo trong môi trường axit.
-
C.
Hòa tan chất béo trong dung môi hữu cơ.
-
D.
Thủy phân chất béo trong môi trường kiềm.
Đáp án : D
Xà phòng được điều chế bằng cách: Thủy phân chất béo trong môi trường kiềm.
Nguyên tố X có cấu tạo như sau: điện tích hạt nhân là 11+, 3 lớp electron, lớp ngoài cùng có 1 electron. Tính chất hóa học cơ bản của X là
-
A.
Tính kim loại mạnh.
-
B.
Tính phi kim mạnh.
-
C.
X là khí hiếm.
-
D.
Tính kim loại yếu.
Đáp án : A
Xem lại lí thuyết sự biến đổi tính chất trong một chu kì
Từ vị trí này ta biết:
+ Nguyên tố X có số hiệu nguyên tử là 11, đó là Na.
+ Nguyên tố X ở chu kì 3, do đó có 3 lớp electron.
+ Nguyên tố X ở nhóm I có 1e lớp vỏ ngoài cùng, nguyên tố A ở đầu chu kì nên có tính kim loại mạnh.
Đốt cháy chất hữu cơ X (X là một trong số các chất tinh bột, saccarozơ, glucozơ, protein) thấy sản phẩm tạo ra là CO2, H2O và N2. Vậy X có thể là
-
A.
tinh bột.
-
B.
saccarozơ.
-
C.
glucozơ.
-
D.
protein.
Đáp án : D
Đốt cháy chất hữu cơ X (X là một trong số các chất tinh bột, saccarozơ, glucozơ, protein) thấy sản phẩm tạo ra là CO2, H2O và N2 => X chứa C, H, O và N
=> X là protein
Ứng dụng nào không phải là ứng dụng của glucozơ?
-
A.
Làm thực phẩm dinh dưỡng và thuốc tăng lực
-
B.
Tráng gương, tráng phích
-
C.
Nguyên liệu sản xuất rượu etylic
-
D.
Nguyên liệu sản xuất PVC
Đáp án : D
Ứng dụng không phải của glucozơ là: Nguyên liệu sản xuất PVC
Tính chất nào không phải của benzen ?
-
A.
Tác dụng với Br2 (to, Fe).
-
B.
Tác dụng với HNO3 /H2SO4 (đ).
-
C.
Tác dụng với dung dịch KMnO4.
-
D.
Tác dụng với Cl2 (as).
Đáp án : C
Tính chất không phải của benzen là tác dụng với dung dịch KMnO4
Một số protein tan được trong nước tạo thành dung dịch keo, khi đun nóng hoặc cho thêm hóa chất vào dung dịch này thường xảy ra kết tủa protein. Hiện tượng đó gọi là
-
A.
sự oxi hóa.
-
B.
sự khử.
-
C.
sự cháy.
-
D.
sự đông tụ
Đáp án : D
Một số protein tan được trong nước tạo thành dung dịch keo, khi đun nóng hoặc cho thêm hóa chất vào dung dịch này thường xảy ra kết tủa protein. Hiện tượng đó gọi là sự đông tụ.
Công thức phân tử của saccarozơ là
-
A.
C6H12O6
-
B.
C6H12O7
-
C.
C12H22O11
-
D.
(-C6H10O5-)n
Đáp án : C
Xem lại lí thuyết saccarozơ
Công thức phân tử của saccarozơ là C12H22O11
Trong các khí sau : CH4, H2, Cl2, O2. Khí nào khi trộn với nhau tạo ra hỗn hợp nổ ?
-
A.
CH4 và Cl2.
-
B.
H2 và O2.
-
C.
CH4 và O2.
-
D.
cả B và C đều đúng
Đáp án : D
Các hỗn hợp khí khi trộn với nhau tạo ra hỗn hợp nổ là: H2 và O2 và CH4 và O2.
Cho rượu etylic nguyên chất tác dụng với kali dư. Số phản ứng hóa học xảy ra là
-
A.
1.
-
B.
2.
-
C.
3.
-
D.
4.
Đáp án : A
Rượu etylic nguyên chất là C2H5OH => chỉ xảy ra 1 phản ứng với K
2C2H5OH + 2K → 2C2H5OK + H2 ↑
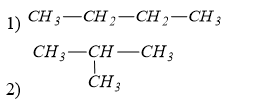
Số công thức cấu tạo của C4H10 là
-
A.
1
-
B.
3
-
C.
2
-
D.
4
Đáp án : C
có ∆ = 0 => HCHC no, mạch hở
Một hợp chất X chứa 3 nguyên tố C, H, O có tỉ lệ khối lượng mC : mH : mO = 21 : 2 : 4. Hợp chất X có công thức đơn giản nhất trùng với CTPT. CTPT X là:
-
A.
C7H8O
-
B.
C8H10O
-
C.
C6H6O2
-
D.
C7H8O2.
Đáp án : A
+) x : y : z = $\frac{{{m}_{C}}}{12}:\frac{{{m}_{H}}}{1}:\frac{{{m}_{O}}}{16}$
Gọi CTPT của X là CxHyOz
=> x : y : z = $\frac{{{m}_{C}}}{12}:\frac{{{m}_{H}}}{1}:\frac{{{m}_{O}}}{16}=\frac{21}{12}:\frac{2}{1}:\frac{4}{16}=1,75:2:0,25=7:8:1$
=> CTPT của X là C7H8O (vì CTPT trùng với CTĐGN)
Một hợp chất hữu cơ Y khi đốt cháy hoàn toàn thu được CO2 và H2O có số mol bằng nhau. Đồng thời số mol oxi tối thiểu cần dùng bằng 4 lần số mol của Y. Biết trong Y chỉ chứa 1 nguyên tử O. Công thức phân tử của Y là
-
A.
C2H6O
-
B.
C4H8O
-
C.
C3H6O
-
D.
C3H8O.
Đáp án : C
CxHyO + \(\frac{{2{\rm{x + 0,5y - 1}}}}{2}\)O2 $\xrightarrow{{{t}^{o}}}$ xCO2 + \(\frac{y}{2}\)H2O
1 mol → \(\frac{{2{\rm{x + 0,5y - 1}}}}{2}\)mol → x mol → \(\frac{y}{2}\) mol
Phản ứng thu được số mol CO2 và H2O bằng nhau => x = \(\frac{y}{2}\) (1)
Số mol oxi cần dùng bằng 4 lần số mol của Y => \(\frac{{2{\rm{x + 0,5y - 1}}}}{2}\)= 4 (2)
Từ (1) vào (2) => x và y
Gọi CTPT của Y có dạng CxHyO
Vì đầu bài chỉ cho các tỉ lệ, không cho số mol cụ thể => giả sử đốt cháy 1 mol Y
CxHyO + \(\frac{{2{\rm{x + 0,5y - 1}}}}{2}\)O2 $\xrightarrow{{{t}^{o}}}$ xCO2 + \(\frac{y}{2}\)H2O
1 mol → \(\frac{{2{\rm{x + 0,5y - 1}}}}{2}\)mol → x mol → \(\frac{y}{2}\) mol
Phản ứng thu được số mol CO2 và H2O bằng nhau => x = \(\frac{y}{2}\) (1)
Số mol oxi cần dùng bằng 4 lần số mol của Y => \(\frac{{2{\rm{x + 0,5y - 1}}}}{2}\)= 4 (2)
Thay (1) vào (2) ta có: \(\frac{{2.\frac{y}{2}{\rm{ + 0,5y - 1}}}}{2}\)= 4 => 1,5y – 1 = 8 => y = 6
Thay y = 6 vào (1) => x = 3
=> CTPT của Y là C3H6O
Đốt cháy hoàn toàn một ankan thu được 2,24 lít khí CO2 và 3,6 gam H2O. Công thức phân tử của ankan là
-
A.
CH4.
-
B.
C2H6.
-
C.
C3H8.
-
D.
C4H10.
Đáp án : A
Cách 1: Tìm n theo PTHH
PTHH: ${C_n}{H_{2n + 2}} + (\frac{{3n + 1}}{2}){O_2} \to nC{O_2} + (n + 1){H_2}O$
+) từ số mol CO2 và số mol H2O => nhân chéo n
Cách 2: ${n_{ankan}} = {n_{{H_2}O}} - {n_{C{O_2}}}$
${n_{C{O_2}}} = \frac{{2,24}}{{22,4}} = 0,1(mol)$${n_{{H_2}O}} = \frac{{3,6}}{{18}} = 0,2(mol)$
Cách 1:
PTHH: ${C_n}{H_{2n + 2}} + (\frac{{3n + 1}}{2}){O_2} \to nC{O_2} + (n + 1){H_2}O$
Theo pt: $n$ $n + 1$
Theo đb: 0,1 0,2
=> 0,2.n = 0,1.(n + 1) => n = 1
Vậy CTPT của ankan là: CH4
Cách 2:
$\begin{array}{l}{n_{ankan}} = {n_{{H_2}O}} - {n_{C{O_2}}}\\ \Rightarrow {n_{ankan}} = 0,2 - 0,1 = 0,1(mol)\\ \Rightarrow n = \frac{{0,1}}{{0,1}} = 1\end{array}$
Vậy CTPT của ankan là: $C{H_4}$
Cho các hợp chất sau: CH4, C2H6, C2H4, H2. Có bao nhiêu chất tác dụng với dung dịch nước brom ở nhiệt độ thường?
-
A.
1
-
B.
2
-
C.
3
-
D.
4
Đáp án : A
Chất tác dụng với dung dịch nước brom là C2H4 vì trong phân tử C2H4 có liên kết đôi
CH2 = CH2 + Br2 → CH2Br=CH2Br
Có 3 bình, mỗi bình chứa 1 trong các khí sau: metan, axetilen, khí cacbonic. Đánh số A, B, C vào các bình này và tiến hành các thí nghiệm với từng chất khí. Kết quả thí nghiệm được ghi ở bảng sau:
|
Thuốc thử |
A |
B |
C |
|
Dung dịch brom |
Không hiện tượng |
Mất màu |
Không hiện tượng |
|
Dung dịch nước vôi trong |
Không hiện tượng |
Không hiện tượng |
Vẩn đục |
Hãy cho biết 3 bình A, B, C chứa lần lượt những khí nào?
-
A.
Bình A chứa axetilen, bình B chứa metan, bình C chứa cacbonic.
-
B.
Bình A chứa metan, bình B chứa axetilen, bình C chứa cacbonic.
-
C.
Bình A chứa axetilen, bình B chứa cacbonic, bình C chứa metan.
-
D.
Bình A chứa cacbonic, bình B chứa metan, bình C chứa axetilen.
Đáp án : B
Cần nắm được tính chất hóa học đặc trưng của khí metan, khí cacbonic và khí axetilen
Khí làm mất màu dung dịch brom là axetilen => Bình B chứa axetilen
Khí làm vẩn đục nước vôi trong là cacbonic => Bình C chứa cacbonic
Khí không phản ứng với cả 2 chất là metan => Bình A chứa metan
Tính khối lượng benzen cần dùng để điều chế 23,55 gam brombenzen. Biết hiệu suất phản ứng đạt 85%.
-
A.
11,7 gam.
-
B.
13,77 gam.
-
C.
14,625 gam.
-
D.
9,945 gam
Đáp án : B
+) Tính số mol benzen theo PT: C6H6 + Br2 $\xrightarrow{F\text{e}}$ C6H5Br + HBr
+) Vì hiệu suất chỉ đạt 85% => khối lượng benzen cần dùng
${{n}_{{{C}_{6}}{{H}_{5}}Br}}~=~\frac{23,55}{157}=0,15\text{ }mol$
Phương trình phản ứng:
C6H6Br + Br2 $\xrightarrow{F\text{e}}$ C6H5Br + HBr
0,15 ← 0,15 ← 0,15 (mol)
mbenzen theo lí thuyết = 0,15.78 = 11,7 gam.
Vì hiệu suất chỉ đạt 85% => khối lượng benzen cần dùng là: mbenzen = \(\frac{{11,7}}{{85\% }} = 13,77\,gam\)
Thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 13,8 gam rượu etylic nguyên chất là
-
A.
5,60.
-
B.
22,4.
-
C.
8,36.
-
D.
20,16.
Đáp án : D
+) Tính số mol C2H5OH
+) Tính số mol Oxi theo PT: C2H5OH + 3O2 $\xrightarrow{{{t}^{o}}}$ 2CO2 + 3H2O
${{n}_{{{C}_{2}}{{H}_{5}}OH}}=\frac{13,8}{46}=0,3\,mol$
C2H5OH + 3O2 $\xrightarrow{{{t}^{o}}}$ 2CO2 + 3H2O
0,3 mol → 0,9 mol
$=>{{V}_{{{O}_{2}}}}=0,9.22,4=20,16$ lít
Thể tích ancol etylic 92o cần dùng là bao nhiêu để điều chế được 2,24 lít C2H4 (đktc). Cho biết hiệu suất phản ứng đạt 62,5% và D = 0,8 g/ml.
-
A.
8 ml
-
B.
10 ml
-
C.
12,5 ml
-
D.
3,9 ml
Đáp án : B
+) Độ rượu = $\frac{{{V}_{{{C}_{2}}{{H}_{5}}OH}}\,}{{{V}_{\text{dd}\,r\text{uou (}{{\text{C}}_{2}}{{H}_{5}}OH+{{H}_{2}}O)}}}.100%$
+) m = V . D
C2H5OH → C2H4 + H2O
nC2H4 = 0,1 (mol) = nC2H5OH nguyên chất lý thuyết
Trên thực tế hiệu suất phản ứng là 62,5%
=> ${{n}_{{{C}_{2}}{{H}_{5}}OH}}$thực tế = $\frac{0,1}{62,5\%}$= 0,16 mol
=> ${{m}_{{{C}_{2}}{{H}_{5}}OH}}$ = 7,36 gam
D = 0,8 g/ml => thể tích C2H5OH nguyên chất cần dùng là $V=\frac{7,36}{0,8}=9,2\text{ }ml$
Độ của rượu được tính bằng số ml rượu nguyên chất trong 100 ml dung dịch rượu.
Áp dụng điều này => cứ 100ml dung dịch rượu 92 độ có 92 ml rượu nguyên chất.
Vậy để có 9,2 ml rượu nguyên chất cần thể tích dd rượu là V = 10ml.
Giấm ăn là dung dịch của axit axetic trong nước, trong đó nồng độ axit axetic từ 2-5%. Lượng axit axetic tối thiểu có trong 1 lít giấm ăn (Dgiấm ăn = 1,01 g/ml) là
-
A.
2,20 gam
-
B.
20,2 gam
-
C.
12,2 gam
-
D.
19,2 gam
Đáp án : B
+) mgiấm ăn = Vgiấm ăn . Dgiấm ăn
+) mchất tan = $\frac{{{m}_{dd}}.C%}{100%}$ => 1010.2% ≤ mgiấm ăn ≤ 1010.5%
Ta có: Vgiấm ăn = 1 lít = 1000 ml
=> khối lượng giấm ăn là: mgiấm ăn = Vgiấm ăn . Dgiấm ăn = 1000.1,01 = 1010 gam
Mà trong dung dịch giấm ăn nồng độ axit axetic từ 2-5%
=> khối lượng axit axetic là: 1010.2% ≤ mgiấm ăn ≤ 1010.5%
=> 20,2 ≤ mgiấm ăn ≤ 50,5 gam
Xét 4 đáp án chỉ có 20,2 gam thỏa mãn
Lên men m gam glucozơ với hiệu suất 90%, lượng khí CO2 sinh ra hấp thụ hết vào dung dịch nước vôi trong, thu được 10 gam kết tủa. Khối lượng dung dịch sau phản ứng giảm 3,4 gam so với khối lượng nước vôi trong ban đầu. Giá trị của m là
-
A.
20
-
B.
30
-
C.
12
-
D.
15
Đáp án : D
+) mdung dịch giảm = ${{m}_{CaC{{\text{O}}_{3}}}}-{{m}_{C{{O}_{2}}}}$ => Tính ${{m}_{C{{O}_{2}}~}}$
C6H12O6 $\xrightarrow{men\,ruou}$ 2C2H5OH + 2CO2 (1)
+) nglucozơ (LT) $=~\frac{1}{2}.{{n}_{C{{O}_{2}}}}$ => mglucozơ (LT)
+) hiệu suất phản ứng $H=90\%=>{{ m }_{TT}}=\frac{{{m}_{LT}}}{90\%}$
Ta có: mdung dịch giảm = ${{m}_{CaC{{\text{O}}_{3}}}}-{{m}_{C{{O}_{2}}}}$ => ${{m}_{C{{O}_{2}}~}}={{m}_{CaC{{O}_{3}}~}}$– mdung dịch giảm = 10 – 3,4 = 6,6 gam
${{n}_{C{{O}_{2}}}}~=\frac{6,6}{44}=0,15\text{ }mol$
C6H12O6 $\xrightarrow{men\,ruou}$ 2C2H5OH + 2CO2 (1)
Theo PTHH (1) ta có: nglucozơ (LT) $=~\frac{1}{2}.{{n}_{C{{O}_{2}}}}=\frac{1}{2}.0,15=0,075\text{ }mol$
=> mglucozơ (LT) = 0,075.180 = 13,5 gam
Vì hiệu suất phản ứng $H=90\%~=>{{m}_{gluc\text{o}zo(TT)}}=\frac{13,5}{90\%}=15\,gam$
Để tráng bạc một số ruột phích, người ta phải thuỷ phân 34,2 gam saccarozơ rồi tiến hành phản ứng tráng gương. Tính lượng Ag tạo thành sau phản ứng, biết hiệu suất cả quá trình tráng gương là 80%?
-
A.
27,64 gam
-
B.
43,90 gam
-
C.
34,56 gam
-
D.
56,34 gam
Đáp án : C
C12H22O11 + H2O $\xrightarrow{axit,\,{{t}^{o}}}$ C6H12O6 + C6H12O6
Vì glucozơ và fructozơ đều có phản ứng tráng gương và có công thức phân tử giống nhau, nên ta gộp thành 1 phương trình:
C6H12O6 + Ag2O $\xrightarrow{N{{H}_{3}}}$ C6H12O7 + 2Ag
msaccarozơ = $~\frac{34,2}{342}=0,1\text{ }mol$
C12H22O11 + H2O $\xrightarrow{axit,\,{{t}^{o}}}$ C6H12O6 + C6H12O6 (1)
0,1 mol → 0,1mol → 0,1 mol
Vì glucozơ và fructozơ đều có phản ứng tráng gương và có công thức phân tử giống nhau, nên ta gộp thành 1 phương trình:
C6H12O6 + Ag2O $\xrightarrow{N{{H}_{3}}}$ C6H12O7 + 2Ag
0,2 mol → 0,4 mol
=> mAg = 0,4.108.80% = 34,56 gam
Thủy phân 1 kg sắn chứa 20% tinh bột trong môi trường axit. Với hiệu suất phản ứng 85%, lượng glucozơ thu được là
-
A.
261,43 gam.
-
B.
200,8 gam.
-
C.
188,89 gam.
-
D.
192,5 gam.
Đáp án : C
+) Tính mtinh bột nguyên chất
(-C6H10O5-)n + nH2O $\xrightarrow{axit,\,{{t}^{o}}}$ nC6H12O6 (glucozơ)
→ khối lượng glucozơ LT
Vì hiệu suất phản ứng đạt 85% => ${{m}_{{{C}_{6}}{{H}_{12}}{{O}_{6}}(TT)}}={{m}_{{{C}_{6}}{{H}_{12}}{{O}_{6}}(LT)}}.85\%$
Trong 1 kg sắn chứa 20% tinh bột => mtinh bột nguyên chất = 1.20% = 0,2 kg = 200 gam
(-C6H10O5-)n + nH2O $\xrightarrow{axit,\,{{t}^{o}}}$ nC6H12O6 (glucozơ)
162n gam 180n gam
200 gam → $\frac{200.180n}{162n}=\frac{2000}{9}$ gam
=> ${{m}_{{{C}_{6}}{{H}_{12}}{{O}_{6}}(LT)}}=\frac{2000}{9}\,gam$
Vì hiệu suất phản ứng đạt 85%
=> ${{m}_{{{C}_{6}}{{H}_{12}}{{O}_{6}}(TT)}}={{m}_{{{C}_{6}}{{H}_{12}}{{O}_{6}}(LT)}}.85%=\frac{2000}{9}.85%=188,89\,gam$%=188,89 gam
Trùng hợp 22,4 lít C2H4 (đktc), nếu hiệu suất phản ứng là 80% thì khối lượng polime thu được là bao nhiêu? Biết hệ số trùng hợp là 500.
-
A.
2,24 gam
-
B.
4,48 gam
-
C.
2,80 gam
-
D.
3,36 gam
Đáp án : A
500CH2=CH2 → (-CH2-CH2-)500
500 1
0,1 mol → 2.10-4 mol
+) Mpolime = 28.500 => mpolietilen (LT) = 2.10-4.14000
+) mpolime (TT) = mpolime (LT) . H%
Số mol etilen là: ${{n}_{{{C}_{2}}{{H}_{4}}}}=\frac{2,24}{22,4}=0,1\,mol$
Khối lượng của etilen là: m = 0,1.28 = 2,8 gam
Vì hệ số trùng hợp của etilen là 500 nên ta có phương trình
500CH2=CH2 → (-CH2-CH2-)500
500 1
0,1 mol → 2.10-4 mol
Ta có: Mpolime = 28.500 = 14000
=> mpolietilen (LT) = 2.10-4.14000 = 2,8 gam
Với hiệu suất là 80% thì khối lượng polime thu được là:
mpolime (TT) = mpolime (LT) . H% = 2,8.80% = 2,24 gam
Trùng hợp 0,5 tấn etilen với hiệu suất 90% thì khối lượng polietilen thu được là
-
A.
0,5 tấn.
-
B.
5 tấn.
-
C.
4,5 tấn.
-
D.
0,45 tấn.
Đáp án : D
nCH2=CH2 $\xrightarrow{{{t}^{o}},\,xt}$ (-CH2-CH2-)n
+) Áp dụng bảo toàn khối lượng: mpolietilen (LT) = metilen
+) Hiệu suất phản ứng là 90% => mpolietilen thực tế
nCH2=CH2 $\xrightarrow{{{t}^{o}},\,xt}$ (-CH2-CH2-)n
Áp dụng bảo toàn khối lượng: mpolietilen = metilen
=> khối lượng polietilen theo lí thuyết là: 0,5 tấn
Vì hiệu suất phản ứng là 90% => khối lượng polietilen thực tế thu được là
mpolietilen thực tế = 0,5.90% = 0,45 tấn
















