Đề khảo sát chất lượng đầu năm Hóa 11 - Đề số 6
Đề bài
Kim loại nào sau đây tác dụng với HCl loãng và tác dụng với clo cho cùng loại muối?
-
A.
Cu.
-
B.
Fe.
-
C.
Ag.
-
D.
Zn.
Cho 0,448 lít khí SO2 (ở đktc) hấp thụ hết vào 250 ml dung dịch NaOH 0,5M. Cô cạn dung dịch sau phản ứng thu được muối có khối lượng là
-
A.
2,82 gam.
-
B.
2,64 gam.
-
C.
2,52 gam.
-
D.
2,32 gam.
Phản ứng hóa học nào sau đây sai?
-
A.
CuO + H2SO4 → CuSO4 + H2O.
-
B.
Ba(OH)2 + H2SO4 → BaSO4 + 2H2O.
-
C.
2Ag + 2HCl → 2AgCl + H2.
-
D.
Fe + 2HCl → FeCl2 + H2.
Đặc điểm nào sau đây là đặc điểm chung của nhóm halogen?
-
A.
Vừa có tính oxi hóa vừa có tính khử.
-
B.
Ở điều kiện thường là chất khí.
-
C.
Có tính oxi hóa mạnh.
-
D.
Tác dụng được với nước.
Cho 46,1 gam hỗn hợp Fe2O3, MgO, ZnO tan vừa đủ trong 1,7 lít dung dịch H2SO4 0,5M thu được hỗn hợp muối sunfat có khối lượng là
-
A.
111,1 gam.
-
B.
113,1 gam.
-
C.
112,1 gam.
-
D.
114,1 gam.
Oxi hóa m gam sắt bằng oxi thu được 75,2 gam hỗn hợp A gồm Fe3O4, Fe2O3, FeO và Fe dư. Cho toàn bộ A phản ứng với H2SO4 đặc nóng đủ thu được dung dịch chỉ chứa muối sắt(III) sunfat và 6,72 lít SO2 (ở đktc). Giá trị của m là
-
A.
56 gam.
-
B.
11,2 gam.
-
C.
22,4 gam.
-
D.
44,8 gam.
Cho phản ứng: Al + H2SO4 đặc Al2(SO4)3 + H2S + H2O.
Tổng hệ số nguyên (có tỉ lệ tối giản) phương trình hóa học của phản ứng trên là
-
A.
42.
-
B.
50.
-
C.
55.
-
D.
52.
Các kim loại thụ động với H2SO4 đặc nguội là
-
A.
Cu, Al.
-
B.
Cu, Fe.
-
C.
Al, Fe.
-
D.
Cu, Zn.
Trong phòng thí nghiệm, khí hiđro sunfua được điều chế bằng phản ứng nào sau đây?
-
A.
FeS + HNO3 loãng.
-
B.
FeS + HNO3 đặc.
-
C.
FeS + HCl.
-
D.
FeS + H2SO4 đặc.
Các nguyên tố nhóm VIA có cấu hình electron lớp ngoài cùng là
-
A.
ns2np4.
-
B.
ns2np6.
-
C.
ns2np5.
-
D.
ns2np3.
Hòa tan hoàn toàn 9,3 gam hỗn hợp Zn và Fe bằng dung dịch HCl dư thu được 3,36 lít khí ở đktc. Thành phần % khối lượng của Zn trong hỗn hợp đầu là
-
A.
30,11%.
-
B.
69,89%.
-
C.
59,67%.
-
D.
69,69%.
Để làm khô khí SO2 có lẫn hơi nước, người ta có thể dùng
-
A.
H2SO4 đặc.
-
B.
CuO.
-
C.
CaO.
-
D.
dung dịch NaOH.
Phát biểu nào sau đây không đúng?
-
A.
Dung dịch HF hoà tan được SiO2.
-
B.
Muối AgI không tan trong nước, muối AgF tan trong nước.
-
C.
Flo có tính oxi hoá mạnh hơn clo.
-
D.
Trong các hợp chất, ngoài số oxi hoá -1, flo và clo còn có số oxi hoá +1, +3, +5, +7.
Có 4 dung dịch: NaOH, H2SO4, HCl, Ba(OH)2. Dùng thuốc thử nào sau đây để nhận biết được các dung dịch trên?
-
A.
NaCl.
-
B.
Quỳ tím.
-
C.
HNO3.
-
D.
KOH.
Dùng loại bình nào sau đây để đựng dung dịch HF?
-
A.
Bình thủy tinh màu nâu.
-
B.
Bình nhựa (chất dẻo).
-
C.
Bình thủy tinh không màu.
-
D.
Bình thủy tinh màu xanh.
Dãy chất nào sau đây chỉ có tính oxi hoá?
-
A.
O2, SO2, Cl2, H2SO4.
-
B.
S, F2, H2S, O3.
-
C.
O3, F2, H2SO4.
-
D.
HCl, H2S, SO2, SO3.
Nước Gia-ven là hỗn hợp các chất nào sau đây?
-
A.
HCl, HClO, H2O.
-
B.
NaCl, NaClO4, H2O.
-
C.
NaCl, NaClO, H2O.
-
D.
NaCl, NaClO3, H2O.
Người ta thường sử dụng chất nào dưới đây để thu gom thuỷ ngân rơi vãi?
-
A.
Khí ozon.
-
B.
Bột lưu huỳnh.
-
C.
Khí oxi.
-
D.
Bột sắt.
Hòa tan hoàn toàn 3,6 gam Mg trong dung dịch HCl dư, sau phản ứng thu được V lít H2 (ở đktc). V có giá trị là
-
A.
3,36 lít.
-
B.
2,24 lít.
-
C.
4,48 lít.
-
D.
6,72 lít.
Để điều chế clo trong phòng thí nghiệm, cần dùng các hóa chất
-
A.
KMnO4 và NaCl.
-
B.
MnO2 và dung dịch HCl đặc.
-
C.
NaCl và nước.
-
D.
Cho H2 tác dụng với Cl2 có ánh sáng.
Dãy các chất phản ứng được với axit HCl là
-
A.
CaCO3, Al2O3, Ba(OH)2, Zn.
-
B.
Cu, CaO, SO2, Fe.
-
C.
Ag, MgO, NaOH, SO2.
-
D.
SO2, Na2O, KOH, NaBr.
Cho 11,3 gam hỗn hợp Mg và Zn tác dụng với H2SO4 loãng vừa đủ thu được 6,72 lít khí H2 (ở đktc). Cô cạn dung dịch sau phản ứng thu được lượng muối khan là
-
A.
40,1 gam.
-
B.
41,1 gam.
-
C.
41,2 gam.
-
D.
14,2 gam.
Dãy các axit halogenhidric được xếp theo chiều tăng dần tính axit là
-
A.
HI < HCl < HF < HBr.
-
B.
HF < HBr < HI < HCl.
-
C.
HI < HF < HCl < HBr.
-
D.
HF < HCl < HBr < HI.
Cho 17,7 gam hỗn hợp gồm Al và Cu trong lượng dư dung dịch H2SO4 đặc, nóng thu được 13,44 lít khí SO2 (ở đktc, sản phẩm khử duy nhất). Phần trăm khối lượng của Cu trong hỗn hợp ban đầu là
-
A.
64,24%.
-
B.
33,58%.
-
C.
45,76%.
-
D.
54,24%.
Cặp chất nào sau đây không tác dụng với oxi khi đun nóng?
-
A.
P, S.
-
B.
Fe, Cu.
-
C.
C, H2.
-
D.
Ag, Pt.
Tiến hành các thí nghiệm sau:
(1) O3 tác dụng với dung dịch KI.
(2) Axit HF tác dụng với SiO2.
(3) khí SO2 tác dụng với dung dịch KOH.
(4) MnO2 tác dụng với dung dịch HCl đặc, đun nóng.
(5) Thổi khí F2 vào hơi nước.
(6) Sục khí H2S vào dung dịch Br2.
Số thí nghiệm tạo ra đơn chất là
-
A.
4.
-
B.
3.
-
C.
2.
-
D.
5.
Clorua vôi có công thức phân tử là
-
A.
CaCl2.
-
B.
CaOCl.
-
C.
Ca(OCl)2.
-
D.
CaOCl2.
Nung nóng hỗn hợp gồm 5,6 gam Fe với 4 gam bột S trong bình kín một thời gian thu được hỗn hợp X gồm FeS, FeS2, Fe và S dư. Cho X tan hết trong dung dịch H2SO4 đặc nóng dư thu được V lít khí SO2 (ở đktc, sản phẩm khử duy nhất). Giá trị của V là
-
A.
8,96 lít.
-
B.
11,65 lít.
-
C.
3,36 lít.
-
D.
11,76 lít.
Các nguyên tố nhóm halogen có cấu hình electron lớp ngoài cùng là
-
A.
ns2np5.
-
B.
ns2np6.
-
C.
ns2np3.
-
D.
ns2np4.
Hòa tan hoàn toàn 17,4 gam hỗn hợp kim loại X gồm Mg, Al và Cu bằng dung dịch H2SO4 đặc, nóng thu được dung dịch Y và thoát ra 12,32 lít SO2 (ở đktc, sản phẩm khử duy nhất). Cô cạn dung dịch Y được m gam muối khan. Giá trị của m là
-
A.
52,6.
-
B.
70,2.
-
C.
71,3.
-
D.
67,4.
Lời giải và đáp án
Kim loại nào sau đây tác dụng với HCl loãng và tác dụng với clo cho cùng loại muối?
-
A.
Cu.
-
B.
Fe.
-
C.
Ag.
-
D.
Zn.
Đáp án : D
HS ghi nhớ:
- Kim loại tác dụng được với dung dịch HCl loãng là kim loại đứng trước H trong dãy hoạt động hóa học của kim loại.
- Kim loại tác dụng với HCl loãng và tác dụng với clo cho cùng loại muối là kim loại chỉ thể hiện 1 hóa trị trong các hợp chất.
- Loại Cu, Ag vì chúng đứng sau H trong dãy hoạt động hóa học nên không phản ứng được với HCl.
- Loại Fe vì:
Fe + 2HCl → FeCl2 + H2
2Fe + 3Cl2 → 2FeCl3
- Kim loại Zn thỏa mãn vì tác dụng với HCl và Cl2 đều thu được ZnCl2:
Zn + 2HCl → ZnCl2 + H2
Zn + Cl2 → ZnCl2
Cho 0,448 lít khí SO2 (ở đktc) hấp thụ hết vào 250 ml dung dịch NaOH 0,5M. Cô cạn dung dịch sau phản ứng thu được muối có khối lượng là
-
A.
2,82 gam.
-
B.
2,64 gam.
-
C.
2,52 gam.
-
D.
2,32 gam.
Đáp án : C
Dựa vào tỉ lệ số mol k = nNaOH/nSO2 để xác định sản phẩm tạo thành:
- Nếu k < 1 thì thu được NaHSO3 và SO2 dư.
- Nếu k = 1 thì thu được sản phẩm là NaHSO3.
- Nếu 1 < k < 2 thì thu được sản phẩm là NaHSO3 và Na2SO3.
- Nếu k = 2 thì thu được sản phẩm Na2SO3.
- Nếu k > 2 thì thu được sản phẩm Na2SO3 và NaOH còn dư.
Ta có: nSO2 = 0,02 mol; nNaOH = 0,25.0,5 = 0,125 mol
Ta có tỉ lệ k = nNaOH/nSO2 = 0,125 : 0,02 = 6,25 > 2.
Do đó SO2 tác dụng với NaOH theo PTHH sau:
SO2 + 2NaOH → Na2SO3 + H2O
⟹ nNa2SO3 = nSO2 = 0,02 mol → mNa2SO3 = 0,02.126 = 2,52 gam
Phản ứng hóa học nào sau đây sai?
-
A.
CuO + H2SO4 → CuSO4 + H2O.
-
B.
Ba(OH)2 + H2SO4 → BaSO4 + 2H2O.
-
C.
2Ag + 2HCl → 2AgCl + H2.
-
D.
Fe + 2HCl → FeCl2 + H2.
Đáp án : C
Dựa vào tính chất hóa học của H2SO4 và HCl để chọn phản ứng hóa học sai.
Phản ứng hóa học 2Ag + 2HCl → 2AgCl + H2 sai vì Ag là kim loại sau H trong dãy hoạt động hóa học của kim loại nên không tác dụng với HCl.
Đặc điểm nào sau đây là đặc điểm chung của nhóm halogen?
-
A.
Vừa có tính oxi hóa vừa có tính khử.
-
B.
Ở điều kiện thường là chất khí.
-
C.
Có tính oxi hóa mạnh.
-
D.
Tác dụng được với nước.
Đáp án : C
Lí thuyết về halogen.
Phát biểu A sai vì F2 chỉ có tính oxi hóa, không có tính khử.
Phát biểu B sai vì chỉ có F2, Cl2 là chất khí ở điều kiện thường, còn Br2 là chất lỏng, I2 là chất rắn ở điều kiện thường.
Phát biểu C đúng vì các nguyên tố nhóm halogen có 7 electron ở lớp ngoài cùng, nên dễ nhận thêm 1e để đạt cấu hình e bền vững của khí hiếm, nên có tính oxi hóa mạnh.
Phát biểu D sai vì chỉ có F2, Cl2, Br2 tác dụng được với nước, còn I2 không tác dụng
Cho 46,1 gam hỗn hợp Fe2O3, MgO, ZnO tan vừa đủ trong 1,7 lít dung dịch H2SO4 0,5M thu được hỗn hợp muối sunfat có khối lượng là
-
A.
111,1 gam.
-
B.
113,1 gam.
-
C.
112,1 gam.
-
D.
114,1 gam.
Đáp án : D
Dùng định luật bảo toàn khối lượng ta có: mmuối sunfat = moxit + maxit - mH2O.
Các phương trình hóa học xảy ra:
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
MgO + H2SO4 → MgSO4 + H2O
ZnO + H2SO4 → ZnSO4 + H2O
Từ các PTHH: nH2O = nH2SO4 = 1,7.0,5 = 0,85 mol
Dùng bảo toàn khối lượng ta có: moxit + mH2SO4 = mmuối sunfat + mH2O
→ mmuối sunfat = moxit + mH2SO4 - mH2O = 46,1 + 0,85.98 - 0,85.18 = 114,1 (gam).
Oxi hóa m gam sắt bằng oxi thu được 75,2 gam hỗn hợp A gồm Fe3O4, Fe2O3, FeO và Fe dư. Cho toàn bộ A phản ứng với H2SO4 đặc nóng đủ thu được dung dịch chỉ chứa muối sắt(III) sunfat và 6,72 lít SO2 (ở đktc). Giá trị của m là
-
A.
56 gam.
-
B.
11,2 gam.
-
C.
22,4 gam.
-
D.
44,8 gam.
Đáp án : A
Quy đổi hỗn hợp X chứa sắt và các oxit sắt thành Fe (x mol) và O (y mol).
- Lập phương trình về tổng khối lượng hỗn hợp X
- Lập phương trình dựa vào định luật bảo toàn e
Giải hệ tìm được x, y ⟹ số mol Fe ban đầu ⟹ giá trị của m.
Quy đổi hỗn hợp X về Fe (x mol) và O (y mol).
⇒ 56x + 16y = 75,2 (1)
Mặt khác ta có: nSO2 = 6,72 : 22,4 = 0,3 mol
Quá trình nhường e:
Fe0 → Fe+3 + 3e
x → 3x (mol)
O0 + 2e → O-2
y → 2y (mol)
Quá trình nhận e:
S+6 + 2e → S+4
0,6 ← 0,3 (mol)
Áp dụng định luật bảo toàn electron: 3x = 2y + 0,6 (2)
Giải (1) và (2) ta được: x = 1; y = 1,2
Vậy m = mFe = 1.56 = 56 (gam)
Cho phản ứng: Al + H2SO4 đặc Al2(SO4)3 + H2S + H2O.
Tổng hệ số nguyên (có tỉ lệ tối giản) phương trình hóa học của phản ứng trên là
-
A.
42.
-
B.
50.
-
C.
55.
-
D.
52.
Đáp án : A
Cân bằng phản ứng oxi hóa - khử bằng phương pháp thăng bằng electron:
1. Xác định số oxi hóa của những nguyên tố có số oxi hóa thay đổi.
2. Viết quá trình oxi hóa và quá trình khử, cân bằng mỗi quá trình.
3. Tìm hệ số thích hợp sao cho tổng số electron do chất khử nhường bằng tổng số electron do chất oxi hóa nhận.
4. Đặt hệ số của chất oxi hóa và chất khử vào sơ đồ phản ứng. Hoàn thành phương trình hóa học.
Xác định số oxi hóa của các nguyên tố thay đổi:
\(\begin{array}{*{20}{c}}{\mathop { \times 3}\limits^{} }\\{\mathop { \times 8}\limits^{} }\end{array}\left| {\begin{array}{*{20}{l}}{\mathop S\limits^{ + 6} {\rm{ + 8e}} \to \mathop S\limits^{ - 2} }\\{\mathop {Al}\limits^0 {\rm{\;}} \to \mathop {Al}\limits^{ + 3} {\rm{ + 3e}}}\end{array}} \right.\)
⟹ PTHH: 8Al + 15H2SO4 đặc 4Al2(SO4)3 + 3H2S + 12H2O.
Tổng hệ số tối giản (nguyên) trong phản ứng là 8 + 15 + 4 + 3 + 12 = 42.
Các kim loại thụ động với H2SO4 đặc nguội là
-
A.
Cu, Al.
-
B.
Cu, Fe.
-
C.
Al, Fe.
-
D.
Cu, Zn.
Đáp án : C
Ghi nhớ một số kim loại bị thụ động với H2SO4 đặc nguội: Al, Fe, Cr.
Các kim loại thụ động với H2SO4 đặc nguội là: Al, Fe.
Trong phòng thí nghiệm, khí hiđro sunfua được điều chế bằng phản ứng nào sau đây?
-
A.
FeS + HNO3 loãng.
-
B.
FeS + HNO3 đặc.
-
C.
FeS + HCl.
-
D.
FeS + H2SO4 đặc.
Đáp án : C
Nguyên tắc điều chế H2S trong phòng thí nghiệm:
Cho muối sunfua (trừ PbS, CuS, Ag2S,...) + dung dịch axit mạnh như HCl, H2SO4 loãng.
Trong phòng thí nghiệm, khí hiđrosunfua được điều chế bằng phản ứng:
FeS + 2HCl → FeCl2 + H2S ↑
Các nguyên tố nhóm VIA có cấu hình electron lớp ngoài cùng là
-
A.
ns2np4.
-
B.
ns2np6.
-
C.
ns2np5.
-
D.
ns2np3.
Đáp án : A
- Các nguyên tố nhóm A có số thứ tự nhóm = số electron lớp ngoài cùng.
- Suy ra cấu hình electron lớp ngoài cùng.
Các nguyên tố nhóm VIA có cấu hình electron lớp ngoài cùng là ns2np4.
Hòa tan hoàn toàn 9,3 gam hỗn hợp Zn và Fe bằng dung dịch HCl dư thu được 3,36 lít khí ở đktc. Thành phần % khối lượng của Zn trong hỗn hợp đầu là
-
A.
30,11%.
-
B.
69,89%.
-
C.
59,67%.
-
D.
69,69%.
Đáp án : B
- Đặt ẩn là số mol mỗi kim loại trong hỗn hợp đầu.
- Viết các PTHH, đặt ẩn vào PTHH.
- Lập hệ phương trình về khối lượng hỗn hợp và số mol khí để tìm số mol Zn và số mol Fe.
- Từ đó tìm được thành phần % khối lượng của Zn trong hỗn hợp đầu.
Giả sử 9,3 gam hỗn hợp có chứa x mol Zn và y mol Fe.
⟹ 65x + 56y = 9,3 gam (1)
Các PTHH:
Zn + 2 HCl → ZnCl2 + H2
x → x (mol)
Fe + 2 HCl → FeCl2 + H2
y → y (mol)
⟹ nH2 = x + y = 0,15 mol (2)
Giải hệ phương trình (1) và (2) ta được x = 0,1 và y = 0,05
⟹ %mZn = \(\frac{{0,1.65}}{{9,3}}.100\% \) = 69,89%
Để làm khô khí SO2 có lẫn hơi nước, người ta có thể dùng
-
A.
H2SO4 đặc.
-
B.
CuO.
-
C.
CaO.
-
D.
dung dịch NaOH.
Đáp án : A
Nguyên tắc chọn chất làm khô là:
+ Chất làm khô có khả năng hút nước
+ Chất làm khô không phản ứng với chất cần làm khô.
Chất dùng để làm khô khí SO2 là khí có khả năng hút nước và không phản ứng với khí SO2.
Trong các chất đề bài cho, H2SO4 đặc và CaO đều có khả năng hút nước. Tuy nhiên do CaO phản ứng được với khí SO2 nên không dùng để làm khô.
Do đó để làm khô khí SO2 có lẫn hơi nước, người ta dùng H2SO4 đặc.
Phát biểu nào sau đây không đúng?
-
A.
Dung dịch HF hoà tan được SiO2.
-
B.
Muối AgI không tan trong nước, muối AgF tan trong nước.
-
C.
Flo có tính oxi hoá mạnh hơn clo.
-
D.
Trong các hợp chất, ngoài số oxi hoá -1, flo và clo còn có số oxi hoá +1, +3, +5, +7.
Đáp án : D
Dựa vào tính chất của các halogen và hợp chất của halogen để tìm phát biểu không đúng.
Phát biểu D không đúng vì flo chỉ có số oxi hóa -1 trong các hợp chất.
Có 4 dung dịch: NaOH, H2SO4, HCl, Ba(OH)2. Dùng thuốc thử nào sau đây để nhận biết được các dung dịch trên?
-
A.
NaCl.
-
B.
Quỳ tím.
-
C.
HNO3.
-
D.
KOH.
Đáp án : B
Dựa vào tính chất hóa học của các loại chất để lựa chọn thuốc thử.
- Cho quỳ tím vào 4 dung dịch trên:
+ Dung dịch làm quỳ tím hóa xanh là NaOH và Ba(OH)2 (nhóm 1).
+ Dung dịch làm quỳ tím hóa đỏ là HCl và H2SO4 (nhóm 2).
- Cho từng chất ở nhóm 1 vào từng chất ở nhóm 2:
+ Nếu xuất hiện kết tủa trắng thì chất đã lấy ở nhóm 1 là Ba(OH)2, còn chất đã lấy ở nhóm 2 là H2SO4.
PTHH: Ba(OH)2 + H2SO4 → BaSO4↓ + 2H2O
+ Chất còn lại ở nhóm 1 là NaOH, chất còn lại ở nhóm 2 là HCl
Dùng loại bình nào sau đây để đựng dung dịch HF?
-
A.
Bình thủy tinh màu nâu.
-
B.
Bình nhựa (chất dẻo).
-
C.
Bình thủy tinh không màu.
-
D.
Bình thủy tinh màu xanh.
Đáp án : B
Dựa vào tính chất hóa học của dung dịch HF.
Dung dịch HF tác dụng được với SiO2 theo phương trình hóa học:
4HF + SiO2 → SiF4 + 2H2O
Do đó nếu đựng dung dịch HF trong các bình thủy tinh (thành phần SiO2) thì sẽ ăn mòn các bình này.
Vậy nên ta dùng bình nhựa để đựng dung dịch HF.
Dãy chất nào sau đây chỉ có tính oxi hoá?
-
A.
O2, SO2, Cl2, H2SO4.
-
B.
S, F2, H2S, O3.
-
C.
O3, F2, H2SO4.
-
D.
HCl, H2S, SO2, SO3.
Đáp án : C
Chất chỉ có tính oxi hóa là chất chỉ có khả năng nhận electron.
Dãy chất O3, F2, H2SO4 chỉ có tính oxi hoá.
Nước Gia-ven là hỗn hợp các chất nào sau đây?
-
A.
HCl, HClO, H2O.
-
B.
NaCl, NaClO4, H2O.
-
C.
NaCl, NaClO, H2O.
-
D.
NaCl, NaClO3, H2O.
Đáp án : C
Dựa vào thành phần của nước Gia-ven.
Nước Gia-ven là hỗn hợp NaCl, NaClO, H2O.
Người ta thường sử dụng chất nào dưới đây để thu gom thuỷ ngân rơi vãi?
-
A.
Khí ozon.
-
B.
Bột lưu huỳnh.
-
C.
Khí oxi.
-
D.
Bột sắt.
Đáp án : B
Dựa vào tính chất hóa học của các chất.
Người ta thường sử dụng bột lưu huỳnh để thu gom thuỷ ngân rơi vãi vì lưu huỳnh tác dụng với thủy ngân ngay ở điều kiện thường theo PTHH: Hg + S → HgS ↓
Hòa tan hoàn toàn 3,6 gam Mg trong dung dịch HCl dư, sau phản ứng thu được V lít H2 (ở đktc). V có giá trị là
-
A.
3,36 lít.
-
B.
2,24 lít.
-
C.
4,48 lít.
-
D.
6,72 lít.
Đáp án : A
- Viết PTHH.
- Từ số mol của Mg suy ra số mol của khí H2.
- Tính thể tích khí ở đktc dựa vào công thức: V = n.22,4
Ta có nMg = 3,6 : 24 = 0,15 mol.
PTHH: Mg + 2HCl → MgCl2 + H2
Theo PTHH ta có: nH2 = nMg = 0,15 mol.
Vậy V = VH2 = 0,15.22,4 = 3,36 lít
Để điều chế clo trong phòng thí nghiệm, cần dùng các hóa chất
-
A.
KMnO4 và NaCl.
-
B.
MnO2 và dung dịch HCl đặc.
-
C.
NaCl và nước.
-
D.
Cho H2 tác dụng với Cl2 có ánh sáng.
Đáp án : B
Nguyên tắc điều chế clo trong phòng thí nghiệm là cho HCl đặc tác dụng với các chất oxi hóa mạnh như KMnO4, KClO3, MnO2, CaOCl2, ...
Nguyên tắc điều chế clo trong phòng thí nghiệm là cho HCl đặc tác dụng với các chất oxi hóa mạnh như KMnO4, KClO3, MnO2, CaOCl2, ...
Do đó để điều chế clo trong phòng thí nghiệm, cần dùng các hóa chất MnO2 và dung dịch HCl đặc.
PTHH: 4HCl đặc + MnO2 → MnCl2 + Cl2 ↑ + 2H2O.
Dãy các chất phản ứng được với axit HCl là
-
A.
CaCO3, Al2O3, Ba(OH)2, Zn.
-
B.
Cu, CaO, SO2, Fe.
-
C.
Ag, MgO, NaOH, SO2.
-
D.
SO2, Na2O, KOH, NaBr.
Đáp án : A
Dựa vào tính chất hóa học của axit HCl.
- A thỏa mãn vì CaCO3, Al2O3, Ba(OH)2, Zn đều phản ứng được với axit HCl.
PTHH
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Al2O3 + 6HCl → 2AlCl3 + 3H2O
Ba(OH)2 + 2HCl→ BaCl2 + 2H2O
Zn + 2HCl →ZnCl2 + H2
- B loại Cu, SO2.
- C loại Ag, SO2.
- D loại SO2, NaBr.
Cho 11,3 gam hỗn hợp Mg và Zn tác dụng với H2SO4 loãng vừa đủ thu được 6,72 lít khí H2 (ở đktc). Cô cạn dung dịch sau phản ứng thu được lượng muối khan là
-
A.
40,1 gam.
-
B.
41,1 gam.
-
C.
41,2 gam.
-
D.
14,2 gam.
Đáp án : A
- Dùng bảo toàn nguyên tố H ⟹ nH2SO4 = nH2
- Dùng định luật bảo toàn khối lượng ta có: mmuối sunfat = mkim loại + maxit - mH2.
Ta có: KL + H2SO4 → Muối sunfat + H2
Áp dụng bảo toàn nguyên tố H ⟹ nH2SO4 = nH2 = 6,72 : 22,4 = 0,3 mol
Áp dụng định luật bảo toàn khối lượng ⟹ mMg, Zn + mH2SO4 = mmuối sunfat + mH2
→ mmuối sunfat = mMg, Zn + mH2SO4 - mH2 = 11,3 + 0,3.98 - 0,3.2 = 40,1 (gam).
Dãy các axit halogenhidric được xếp theo chiều tăng dần tính axit là
-
A.
HI < HCl < HF < HBr.
-
B.
HF < HBr < HI < HCl.
-
C.
HI < HF < HCl < HBr.
-
D.
HF < HCl < HBr < HI.
Đáp án : D
Tính axit càng tăng khi khả năng phân li ra ion H+ càng tăng.
Đi từ HF đến HI, bán kính nguyên tử tăng dần từ F đến I nên khả năng phân cắt liên kết H-X tăng dần từ HF đến HI.
Do đó dãy các axit halogenhidric được xếp theo chiều tăng dần tính axit là: HF < HCl < HBr < HI.
Cho 17,7 gam hỗn hợp gồm Al và Cu trong lượng dư dung dịch H2SO4 đặc, nóng thu được 13,44 lít khí SO2 (ở đktc, sản phẩm khử duy nhất). Phần trăm khối lượng của Cu trong hỗn hợp ban đầu là
-
A.
64,24%.
-
B.
33,58%.
-
C.
45,76%.
-
D.
54,24%.
Đáp án : D
Cách 1: Dùng định luật bảo toàn electron: ne cho = ne nhận
Cách 2: Tính toán theo PTHH
2Al + 6H2SO4 → Al2(SO4)3 + 3SO2 + 6H2O
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
Lập hệ phương trình về khối lượng của hỗn hợp và số mol SO2 để tìm số mol Al và Cu.
Từ đó tính được phần trăm khối lượng của Cu trong hỗn hợp ban đầu.
Giả sử 17,7 gam hỗn hợp có chứa x mol Al và y mol Cu.
⟹ 27x + 64y = 17,7 gam (1)
2Al + 6H2SO4 → Al2(SO4)3 + 3SO2 + 6H2O
x → 1,5x (mol)
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
y → y (mol)
⟹ nSO2 = 1,5x + y = 0,6 mol (2)
Giải hệ phương trình (1) và (2) ta được x = 0,3 và y = 0,15
Vậy thành phần % khối lượng của Cu trong hỗn hợp đầu là:
%mCu = \(\frac{{0,15.64}}{{17,7}}.100\% \) = 54,24%
Cặp chất nào sau đây không tác dụng với oxi khi đun nóng?
-
A.
P, S.
-
B.
Fe, Cu.
-
C.
C, H2.
-
D.
Ag, Pt.
Đáp án : D
Dựa vào tính chất hóa học của oxi.
Cặp chất Ag, Pt không tác dụng với oxi khi đun nóng.
Tiến hành các thí nghiệm sau:
(1) O3 tác dụng với dung dịch KI.
(2) Axit HF tác dụng với SiO2.
(3) khí SO2 tác dụng với dung dịch KOH.
(4) MnO2 tác dụng với dung dịch HCl đặc, đun nóng.
(5) Thổi khí F2 vào hơi nước.
(6) Sục khí H2S vào dung dịch Br2.
Số thí nghiệm tạo ra đơn chất là
-
A.
4.
-
B.
3.
-
C.
2.
-
D.
5.
Đáp án : B
- Đơn chất là các chất được tạo nên từ 1 nguyên tố hóa học.
- Viết phương trình hóa học của các thí nghiệm và tìm thí nghiệm tạo ra đơn chất.
(1) O3 + 2KI + H2O → O2 + 2KOH + I2 ⟹ Tạo đơn chất O2, I2
(2) 4HF + SiO2 → SiF4 + 2H2O ⟹ Không tạo đơn chất
(3) SO2 + KOH → KHSO3 ⟹ Không tạo đơn chất
(4) MnO2 + 4HCl đặc → MnCl2 + Cl2 + 2H2O ⟹ Tạo đơn chất Cl2
(5) 2F2 + 2H2O→ 4HF + O2 ⟹ Tạo đơn chất O2
(6) H2S + 4Br2 + 4H2O → 8HBr + H2SO4 ⟹ Không tạo đơn chất
Vậy các thí nghiệm (1), (4), (5) tạo thành đơn chất (có 3 thí nghiệm).
Clorua vôi có công thức phân tử là
-
A.
CaCl2.
-
B.
CaOCl.
-
C.
Ca(OCl)2.
-
D.
CaOCl2.
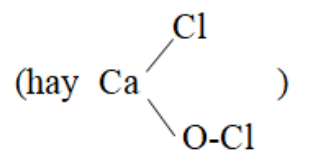
Đáp án : D
Lý thuyết về hợp chất của kim loại kiềm thổ.
Clorua vôi có công thức phân tử là CaOCl2.
Nung nóng hỗn hợp gồm 5,6 gam Fe với 4 gam bột S trong bình kín một thời gian thu được hỗn hợp X gồm FeS, FeS2, Fe và S dư. Cho X tan hết trong dung dịch H2SO4 đặc nóng dư thu được V lít khí SO2 (ở đktc, sản phẩm khử duy nhất). Giá trị của V là
-
A.
8,96 lít.
-
B.
11,65 lít.
-
C.
3,36 lít.
-
D.
11,76 lít.
Đáp án : D
- Quy đổi hỗn hợp X thành Fe và S
- Tính số mol Fe, S
- Viết quá trình cho - nhận electron:
Fe0 → Fe+3 + 3e S+6 + 2e → S+4 (SO2)
0,1 → 0,3 2x ← x ← x
S0 → S+4 (SO2) + 4e
0,125 → 0,125 → 0,5
+ Áp dụng định luật bảo toàn electron ⟹giá trị của X
+ Tính tổng số mol SO2 (do S0 sinh ra và do S+6 sinh ra) ⟹ giá trị của V
Quy đổi hỗn hợp X thành Fe và S
Ta có: nFe = 0,1 mol; nS = 0,125 mol
Quá trình cho - nhận electron:
Fe0 → Fe+3 + 3e S+6 + 2e → S+4 (SO2)
0,1 → 0,3 2x ← x ← x
S0 → S+4 (SO2) + 4e
0,125 → 0,125 → 0,5
Áp dụng định luật bảo toàn electron: 0,3 + 0,5 = 2x ⟹ x = 0,4
⟹ ∑nSO2 = 0,125 + x = 0,525 mol
⟹ V = 0,525.22,4 = 11,76 lít
Các nguyên tố nhóm halogen có cấu hình electron lớp ngoài cùng là
-
A.
ns2np5.
-
B.
ns2np6.
-
C.
ns2np3.
-
D.
ns2np4.
Đáp án : A
Lý thuyết chung về nhóm halogen.
Các nguyên tố nhóm halogen có cấu hình electron lớp ngoài cùng là ns2np5.
Hòa tan hoàn toàn 17,4 gam hỗn hợp kim loại X gồm Mg, Al và Cu bằng dung dịch H2SO4 đặc, nóng thu được dung dịch Y và thoát ra 12,32 lít SO2 (ở đktc, sản phẩm khử duy nhất). Cô cạn dung dịch Y được m gam muối khan. Giá trị của m là
-
A.
52,6.
-
B.
70,2.
-
C.
71,3.
-
D.
67,4.
Đáp án : B
Công thức tính nhanh bài toán KL + H2SO4 đặc, nóng:
\({n_{S{O_4}^{2 - }\left( {muoi} \right)}} = \frac{1}{2}.{n_e}\)
\({n_{{H_2}S{O_4}pu}} = 2{n_{S{O_2}}} + 4{n_S} + 5{n_{{H_2}S}}\)
Cách chứng minh:
Khi cho kim loại M (hóa trị cao nhất là n) phản ứng với H2SO4 đặc nóng:
2M → M2(SO4)n
2 mol 1 mol
Ta thấy: ne = 2n (mol) và nSO4 2-(muối) = n (mol)
\( \to {n_{S{O_4}^{2 - }\left( {muoi} \right)}} = \frac{1}{2}.{n_e}\) (*)
Mặt khác: ne = 2nSO2 + 6nS + 8nH2S
BTNT "S": nH2SO4 pư = nSO4(muối) + nSO2 + nS + nH2S
⟹ nH2SO4 pư = 0,5.(2nSO2 + 6nS + 8nH2S) + nSO2 + nS + nH2S = 2nSO2 + 4nS + 5nH2S
Vậy: \({n_{{H_2}S{O_4}pu}} = 2{n_{S{O_2}}} + 4{n_S} + 5{n_{{H_2}S}}\) (**)
Ta có: nSO2 = 12,32: 22,4 = 0,55 mol
Sử dụng công thức tính nhanh (xem thêm ở phương pháp giải) ta có:
\({n_{S{O_4}^{2 - }\left( {muoi} \right)}} = \frac{1}{2}.{n_e} = \frac{1}{2}.2{n_{S{O_2}}} = {n_{S{O_2}}} = 0,55\left( {mol} \right)\)
Khối lượng muối khan thu được là mmuối = mkim loại + mSO4(muối) = 17,4 + 0,55.96 = 70,2 gam
Các bài khác cùng chuyên mục
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 3
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 7+8: Hidrocacbon thơm và Ancol - Phenol - Ete - Đề số 1
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 3
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 2
- Đề kiểm tra 1 tiết Hóa 11 chương 5+6: Hidrocacbon no và hidrocacbon không no - Đề số 1

















