Đề thi giữa kì 2 Hóa 9 - Đề số 5
Tổng hợp đề thi học kì 2 lớp 9 tất cả các môn
Toán - Văn - Anh - Lí - Hóa - Sinh - Sử - Địa - GDCD
Đề bài
Các nguyên tố xếp ở chu kì 6 có số lớp electron trong nguyên tử:
-
A.
3
-
B.
5
-
C.
6
-
D.
7
Trong các khí sau : CH4, H2, Cl2, O2. Khí nào khi trộn với nhau tạo ra hỗn hợp nổ ?
-
A.
CH4 và Cl2.
-
B.
H2 và O2.
-
C.
CH4 và O2.
-
D.
cả B và C đều đúng
Chọn câu đúng trong các câu sau:
-
A.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất có trong tự nhiên.
-
B.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất của cacbon.
-
C.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất hữu cơ.
-
D.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các chất trong cơ thể sống.
Dãy công thức hoá học của oxit tương ứng với các nguyên tố hoá học thuộc chu kì 3 là:
-
A.
Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7
-
B.
Na2O, MgO, K2O, SiO2, P2O5, SO3, Cl2O7
-
C.
Na2O, MgO, K2O, SO2, P2O5, SO3, Cl2O7
-
D.
K2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7
Hóa chất dùng để tách etilen khỏi hỗn hợp etan và etilen là
-
A.
dung dịch NaOH.
-
B.
dung dịch HCl
-
C.
dung dịch brom.
-
D.
dung dịch AgNO3.
Tính chất vật lý của axetilen là
-
A.
chất khí không màu, không mùi, ít tan trong nước, nặng hơn không khí.
-
B.
chất khí không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
-
C.
chất khí không màu, không mùi, tan tốt trong nước, nhẹ hơn không khí .
-
D.
chất khí không màu, mùi hắc, ít tan trong nước, nặng hơn không khí.
Dãy các chất sau là hiđrocacbon:
-
A.
CH4, C2H2, C2H5Cl
-
B.
C6H6, C3H4, HCHO
-
C.
C2H2, C2H5OH, C6H12
-
D.
C3H8, C3H4, C3H6
Cấu tạo phân tử axetilen gồm
-
A.
hai liên kết đơn và một liên kết ba.
-
B.
hai liên kết đơn và một liên kết đôi.
-
C.
một liên kết ba và một liên kết đôi.
-
D.
hai liên kết đôi và một liên kết ba.
Có bao nhiêu phát biểu đúng trong số các phát biểu sau:
a) Metan cháy với oxi tạo hơi nước và khí lưu huỳnh đioxit.
b) Phản ứng hóa học giữa metan và clo được gọi là phản ứng thế.
c) Trong phản ứng hóa học, giữa metan và clo, chỉ có duy nhất một nguyên tử hiđro của metan có thể được thay thế bởi nguyên tử clo.
d) Hỗn hợp gồm hai thể tích metan và một thể tích oxi là hỗn hợp nổ mạnh.
-
A.
1
-
B.
2
-
C.
3
-
D.
4
Tính chất vật lí của etilen là
-
A.
Chất lỏng, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí.
-
B.
Chất khí, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí.
-
C.
Chất khí, không màu, không mùi, ít tan trong nước và nặng hơn không khí.
-
D.
Chất khí, không màu, không mùi, tan tốt trong nước và nhẹ hơn không khí.
Dựa vào dữ kiện nào trong các dữ kiện sau đây để có thể nói một chất là vô cơ hay hữu cơ?
-
A.
Trạng thái (rắn, lỏng, khí).
-
B.
Màu sắc.
-
C.
Độ tan trong nước.
-
D.
Thành phần nguyên tố.
Trong phân tử hợp chất hữu cơ cacbon, hiđro, oxi có hoá trị lần lượt là:
-
A.
2,1,2
-
B.
4,1,2
-
C.
6,1,2
-
D.
4,2,2
Trong bảng tuần hoàn các nguyên tố, số chu kì nhỏ và số chu kì lớn:
-
A.
3 và 3
-
B.
4 và 3
-
C.
4 và 4
-
D.
3 và 4
Cho benzen + Cl2 (as) ta thu được dẫn xuất clo A. Vậy A là:
-
A.
C6H5Cl.
-
B.
C6H4Cl2.
-
C.
C6H6Cl6.
-
D.
C6H3Cl3.
Số thứ tự nhóm trong bảng hệ thống tuần hoàn cho biết:
-
A.
Số electron lớp ngoài cùng.
-
B.
Số thứ tự của nguyên tố.
-
C.
Số hiệu nguyên tử.
-
D.
Số lớp electron.
Biết nguyên tố X có số hiệu là 17, chu kì 3, nhóm VII. Hãy cho biết cấu tạo nguyên tử và tính chất của nguyên tố X?
-
A.
X có 3 lớp e, lớp ngoài cùng có 7e, X là phi kim mạnh.
-
B.
X có 4 lớp e, lớp ngoài cùng có 17e, X là phi kim mạnh.
-
C.
X có 3 lớp e, lớp ngoài cùng có 7e, X là kim loại mạnh.
-
D.
X có 4 lớp e, lớp ngoài cùng có 17e, X là kim loại mạnh.
Số công thức cấu tạo mạch hở có thể có của C4H8 là
-
A.
3
-
B.
4
-
C.
5
-
D.
6
Hiđrocacbon X có 83,33% khối lượng Cacbon. Số đồng phân cấu tạo của X là:
-
A.
4
-
B.
3
-
C.
2
-
D.
1
Một hợp chất X chứa 3 nguyên tố C, H, O có tỉ lệ khối lượng mC : mH : mO = 21 : 2 : 4. Hợp chất X có công thức đơn giản nhất trùng với CTPT. CTPT X là:
-
A.
C7H8O
-
B.
C8H10O
-
C.
C6H6O2
-
D.
C7H8O2.
Axit axetic có công thức là C2H4O2. Phần trăm nguyên tố C trong phân tử axit axetic là
-
A.
30%.
-
B.
40%.
-
C.
50%.
-
D.
60%
Đốt cháy hoàn toàn một ankan thu được 2,24 lít khí CO2 và 3,6 gam H2O. Công thức phân tử của ankan là
-
A.
CH4.
-
B.
C2H6.
-
C.
C3H8.
-
D.
C4H10.
Đốt cháy hoàn toàn 11,2 lít khí metan. Biết các thể tích khí đo ở điều kiện tiêu chuẩn.Thể tích khí oxi cần dùng và thể tích khí cacbonic tạo thành lần lượt là
-
A.
22,4 lít và 22,4 lít.
-
B.
11,2 lít và 22,4 lít.
-
C.
22,4 lít và 11,2 lít.
-
D.
11,2 lít và 22,4 lít
Đốt cháy hoàn toàn hỗn hợp gồm 2 ankan là đồng đẳng kế tiếp thu được 2,24 lít khí CO2 và 2,34 gam H2O. Xác định CTPT của 2 ankan.
-
A.
CH4 và C2H6.
-
B.
C2H6 và C3H8.
-
C.
C3H8 và C4H10.
-
D.
CH4 và C3H8
Cho 2,8 lít hỗn hợp metan và etilen (đktc) lội qua dung dịch brom (dư), người ta thu được 4,7 gam đibroetan. Phần trăm thể tích của khí metan là
-
A.
20%.
-
B.
40%.
-
C.
80%.
-
D.
60%
Đốt cháy hết 36 gam hỗn hợp khí C3H6 và C2H6 trong O2 dư thu được 56 lít CO2 (đktc). Thể tích khí C3H6 ở đktc là
-
A.
11,2 lít
-
B.
22,4 lít.
-
C.
33,6 lít.
-
D.
44,8 lít.
Đốt cháy V lít etilen thu được 9 gam hơi nước. Thể tích không khí cần dùng (ở đktc), biết O2 chiếm 20% thể tích không khí?
-
A.
84,0 lít.
-
B.
16,8 lít.
-
C.
56,0 lít.
-
D.
44,8 lít
Cho 0,448 lít (đktc) hỗn hợp khí gồm C2H4, C2H2 tác dụng hết với dung dịch brom dư, khối lượng brom đã tham gia phản ứng là 4,8 gam. Số mol khí C2H4 trong hỗn hợp ban đầu là
-
A.
0,02.
-
B.
0,01.
-
C.
0,015.
-
D.
0,005.
Đốt cháy hoàn toàn 1 mol khí axetilen thì cần bao nhiêu lít không khí (các khí đo ở đktc, biết rằng oxi chiếm 20% thể tích không khí) ?
-
A.
300 lít.
-
B.
280 lít.
-
C.
240 lít.
-
D.
120 lít.
Cho brom phản ứng với benzen tạo ra brombenzen (bột sắt làm xúc tác). Tính khối lượng benzen cần dùng để điều chế 15,7 gam brombenzen. Biết hiệu suất của quá trình phản ứng là 80%.
-
A.
9,75 gam.
-
B.
6,24 gam.
-
C.
7,80 gam.
-
D.
10,53 gam
Đốt cháy hoàn toàn 2,24 lít anken A trong oxi dư thu được hỗn hợp khí B. Cho B lần lượt đi qua bình 1 đựng H2SO4 đặc và bình 2 đựng Ca(OH)2 dư. Thấy khối lượng bình 1 tăng 5,4 gam, bình 2 có 30 gam kết tủa. CTPT của A là
-
A.
C2H4.
-
B.
C3H6.
-
C.
C4H8.
-
D.
C5H10
Lời giải và đáp án
Các nguyên tố xếp ở chu kì 6 có số lớp electron trong nguyên tử:
-
A.
3
-
B.
5
-
C.
6
-
D.
7
Đáp án : C
Các nguyên tố xếp ở chu kì 6 có số lớp electron trong nguyên tử là 6
Trong các khí sau : CH4, H2, Cl2, O2. Khí nào khi trộn với nhau tạo ra hỗn hợp nổ ?
-
A.
CH4 và Cl2.
-
B.
H2 và O2.
-
C.
CH4 và O2.
-
D.
cả B và C đều đúng
Đáp án : D
Các hỗn hợp khí khi trộn với nhau tạo ra hỗn hợp nổ là: H2 và O2 và CH4 và O2.
Chọn câu đúng trong các câu sau:
-
A.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất có trong tự nhiên.
-
B.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất của cacbon.
-
C.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất hữu cơ.
-
D.
Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các chất trong cơ thể sống.
Đáp án : C
Câu đúng là: Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu các hợp chất hữu cơ
Dãy công thức hoá học của oxit tương ứng với các nguyên tố hoá học thuộc chu kì 3 là:
-
A.
Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7
-
B.
Na2O, MgO, K2O, SiO2, P2O5, SO3, Cl2O7
-
C.
Na2O, MgO, K2O, SO2, P2O5, SO3, Cl2O7
-
D.
K2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7
Đáp án : A
Xem lại bảng tuần hoàn hóa học
Dãy công thức hoá học của oxit tương ứng với các nguyên tố hoá học thuộc chu kì 3 là: Na2O, MgO, Al2O3, SiO2, P2O5, SO3, Cl2O7
Hóa chất dùng để tách etilen khỏi hỗn hợp etan và etilen là
-
A.
dung dịch NaOH.
-
B.
dung dịch HCl
-
C.
dung dịch brom.
-
D.
dung dịch AgNO3.
Đáp án : C
Cho hỗn hợp khí qua dung dịch brom dư, etilen bị giữ lại, thu được etan không phản ứng thoát ra ngoài
CH2=CH2 + Br2 → CH2Br=CH2Br
Tính chất vật lý của axetilen là
-
A.
chất khí không màu, không mùi, ít tan trong nước, nặng hơn không khí.
-
B.
chất khí không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
-
C.
chất khí không màu, không mùi, tan tốt trong nước, nhẹ hơn không khí .
-
D.
chất khí không màu, mùi hắc, ít tan trong nước, nặng hơn không khí.
Đáp án : B
Tính chất vật lý của axetilen là :
- Là chất khí, không màu, không mùi, nhẹ hơn không khí (d = $\frac{26}{29}$)
- Ít tan trong nước
Dãy các chất sau là hiđrocacbon:
-
A.
CH4, C2H2, C2H5Cl
-
B.
C6H6, C3H4, HCHO
-
C.
C2H2, C2H5OH, C6H12
-
D.
C3H8, C3H4, C3H6
Đáp án : D
Dãy các chất sau là hiđrocacbon là: C3H8, C3H4, C3H6
Cấu tạo phân tử axetilen gồm
-
A.
hai liên kết đơn và một liên kết ba.
-
B.
hai liên kết đơn và một liên kết đôi.
-
C.
một liên kết ba và một liên kết đôi.
-
D.
hai liên kết đôi và một liên kết ba.
Đáp án : A
- Công thức cấu tạo của axetilen:
=> cấu tạo phân tử axetilen gồm:
+ Có 1 liên kết ba giữa 2 nguyên tử cacbon
+ Trong liên kết ba có 2 liên kết kém bền, dễ bị đứt lần lượt trong phản ứng hóa học
Có bao nhiêu phát biểu đúng trong số các phát biểu sau:
a) Metan cháy với oxi tạo hơi nước và khí lưu huỳnh đioxit.
b) Phản ứng hóa học giữa metan và clo được gọi là phản ứng thế.
c) Trong phản ứng hóa học, giữa metan và clo, chỉ có duy nhất một nguyên tử hiđro của metan có thể được thay thế bởi nguyên tử clo.
d) Hỗn hợp gồm hai thể tích metan và một thể tích oxi là hỗn hợp nổ mạnh.
-
A.
1
-
B.
2
-
C.
3
-
D.
4
Đáp án : A
Phát biểu đúng: b). Vậy số phát biểu đúng là 1
Các phát biểu sai là:
a) Metan cháy với oxi tạo hơi nước và khí lưu huỳnh đioxit => Sai vì tạo khí cacbonic (CO2) chứ không phải là lưu huỳnh đioxit
c) Trong phản ứng hóa học giữa Metan và Clo, chỉ có duy nhất một nguyên tử Hiđro của Metan có thể được thay thế bởi nguyên tử Clo => Sai.
d) Hỗn hợp gồm hai thể tích Metan và một thể tích Oxi là hỗn hợp nổ mạnh => Sai, hỗn hợp nổ gồm một thể tích Metan và hai phần thể tích Oxi
Tính chất vật lí của etilen là
-
A.
Chất lỏng, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí.
-
B.
Chất khí, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí.
-
C.
Chất khí, không màu, không mùi, ít tan trong nước và nặng hơn không khí.
-
D.
Chất khí, không màu, không mùi, tan tốt trong nước và nhẹ hơn không khí.
Đáp án : B
Tính chất vật lí của etilen là: Chất khí, không màu, không mùi, ít tan trong nước và nhẹ hơn không khí.
Dựa vào dữ kiện nào trong các dữ kiện sau đây để có thể nói một chất là vô cơ hay hữu cơ?
-
A.
Trạng thái (rắn, lỏng, khí).
-
B.
Màu sắc.
-
C.
Độ tan trong nước.
-
D.
Thành phần nguyên tố.
Đáp án : D
Dựa vào thành phần nguyên tố (trường hợp d) để xác định một hợp chất là vô cơ hay hữu cơ.
Trong phân tử hợp chất hữu cơ cacbon, hiđro, oxi có hoá trị lần lượt là:
-
A.
2,1,2
-
B.
4,1,2
-
C.
6,1,2
-
D.
4,2,2
Đáp án : B
Xem lại đặc điểm cấu tạo hợp chất hữu cơ
Trong phân tử hợp chất hữu cơ cacbon, hiđro, oxi có hoá trị lần lượt là: 4,1,2
Trong bảng tuần hoàn các nguyên tố, số chu kì nhỏ và số chu kì lớn:
-
A.
3 và 3
-
B.
4 và 3
-
C.
4 và 4
-
D.
3 và 4
Đáp án : D
Trong bảng tuần hoàn các nguyên tố gồm 7 chu kì. Trong đó 3 chu kì nhỏ (chu kì 1, 2, 3) và 4 chu kì lớn (chu kì 4, 5, 6, 7).
Cho benzen + Cl2 (as) ta thu được dẫn xuất clo A. Vậy A là:
-
A.
C6H5Cl.
-
B.
C6H4Cl2.
-
C.
C6H6Cl6.
-
D.
C6H3Cl3.
Đáp án : C
Cho benzen + Cl2 (as) ta thu được dẫn xuất clo A.
C6H6 + 3Cl2 $\xrightarrow{as}$ C6H6Cl6
Số thứ tự nhóm trong bảng hệ thống tuần hoàn cho biết:
-
A.
Số electron lớp ngoài cùng.
-
B.
Số thứ tự của nguyên tố.
-
C.
Số hiệu nguyên tử.
-
D.
Số lớp electron.
Đáp án : A
Số thứ tự nhóm trong bảng hệ thống tuần hoàn cho biết: Số electron lớp ngoài cùng
Biết nguyên tố X có số hiệu là 17, chu kì 3, nhóm VII. Hãy cho biết cấu tạo nguyên tử và tính chất của nguyên tố X?
-
A.
X có 3 lớp e, lớp ngoài cùng có 7e, X là phi kim mạnh.
-
B.
X có 4 lớp e, lớp ngoài cùng có 17e, X là phi kim mạnh.
-
C.
X có 3 lớp e, lớp ngoài cùng có 7e, X là kim loại mạnh.
-
D.
X có 4 lớp e, lớp ngoài cùng có 17e, X là kim loại mạnh.
Đáp án : A
- Nguyên tố X có số hiệu nguyên tử là 17 => đó là Cl
- Nguyên tố X có số hiệu nguyên tử là 17 => điện tích hạt nhân là 17+, có 17 proton, 17 electron
- Nguyên tố X ở chu kì 3 => có 3 lớp electron
- Nguyên tố X thuộc nhóm VII => lớp e ngoài cùng có 7e
Vì X ở cuối chu kì 3 nên X là phi kim mạnh
Số công thức cấu tạo mạch hở có thể có của C4H8 là
-
A.
3
-
B.
4
-
C.
5
-
D.
6
Đáp án : A
có ∆ = 1 => π = 1 (vì v = 0) => trong phân tử có 1 liên kết đôi
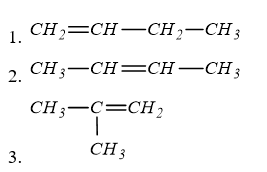
Hiđrocacbon X có 83,33% khối lượng Cacbon. Số đồng phân cấu tạo của X là:
-
A.
4
-
B.
3
-
C.
2
-
D.
1
Đáp án : B
Gọi CTPT của X có dạng CxHy (y ≤ 2x + 2)
+) %mH = 100% - %mC
+) x : y =$\frac{{{m_C}}}{{12}}:\frac{{{m_H}}}{1} = \frac{{83,33}}{{12}}:\frac{{16,67}}{1}$
+) Xét điều kiện: y ≤ 2x + 2 => n
+) \(\Delta = \frac{{2.5 + 2 - 12}}{2} = 0\) => C5H12 là hiđrocacbon no, mạch hở => CTCT
X là hiđrocacbon => X chỉ chứa C và H
Gọi CTPT của X có dạng CxHy (y ≤ 2x + 2)
=> %mH = 100% - %mC = 100% - 83,33% = 16,67%
=> x : y = \[\frac{{{m_C}}}{{12}}:\frac{{{m_H}}}{1} = \frac{{83,33}}{{12}}:\frac{{16,67}}{1} = 6,944:16,67 = 1:2,4 = 5:12\]
=> CTPT của X có dạng: (C5H12)n hay C5nH12n
Vì y ≤ 2x + 2 => 12n ≤ 5n + 7 => n ≤ 1 => n = 1
=> CTPT của X là C5H12
Ta có: \(\Delta = \frac{{2.5 + 2 - 12}}{2} = 0\) => C5H12 là hiđrocacbon no, mạch hở
Các CTCT của X là:

Một hợp chất X chứa 3 nguyên tố C, H, O có tỉ lệ khối lượng mC : mH : mO = 21 : 2 : 4. Hợp chất X có công thức đơn giản nhất trùng với CTPT. CTPT X là:
-
A.
C7H8O
-
B.
C8H10O
-
C.
C6H6O2
-
D.
C7H8O2.
Đáp án : A
+) x : y : z = $\frac{{{m}_{C}}}{12}:\frac{{{m}_{H}}}{1}:\frac{{{m}_{O}}}{16}$
Gọi CTPT của X là CxHyOz
=> x : y : z = $\frac{{{m}_{C}}}{12}:\frac{{{m}_{H}}}{1}:\frac{{{m}_{O}}}{16}=\frac{21}{12}:\frac{2}{1}:\frac{4}{16}=1,75:2:0,25=7:8:1$
=> CTPT của X là C7H8O (vì CTPT trùng với CTĐGN)
Axit axetic có công thức là C2H4O2. Phần trăm nguyên tố C trong phân tử axit axetic là
-
A.
30%.
-
B.
40%.
-
C.
50%.
-
D.
60%
Đáp án : B
\(\% {m_C} = \frac{{2.{M_C}}}{{{M_{{C_2}{H_4}{O_2}}}}}.100\% \)
Khối lượng mol của C2H4O2 là: \({M_{{C_2}{H_4}{O_2}}}\)= 12.2 + 4 + 16.2 = 60
\( = > \% {m_C} = \frac{{12.2}}{{60}}.100\% = 40\% \)
Đốt cháy hoàn toàn một ankan thu được 2,24 lít khí CO2 và 3,6 gam H2O. Công thức phân tử của ankan là
-
A.
CH4.
-
B.
C2H6.
-
C.
C3H8.
-
D.
C4H10.
Đáp án : A
Cách 1: Tìm n theo PTHH
PTHH: ${C_n}{H_{2n + 2}} + (\frac{{3n + 1}}{2}){O_2} \to nC{O_2} + (n + 1){H_2}O$
+) từ số mol CO2 và số mol H2O => nhân chéo n
Cách 2: ${n_{ankan}} = {n_{{H_2}O}} - {n_{C{O_2}}}$
${n_{C{O_2}}} = \frac{{2,24}}{{22,4}} = 0,1(mol)$${n_{{H_2}O}} = \frac{{3,6}}{{18}} = 0,2(mol)$
Cách 1:
PTHH: ${C_n}{H_{2n + 2}} + (\frac{{3n + 1}}{2}){O_2} \to nC{O_2} + (n + 1){H_2}O$
Theo pt: $n$ $n + 1$
Theo đb: 0,1 0,2
=> 0,2.n = 0,1.(n + 1) => n = 1
Vậy CTPT của ankan là: CH4
Cách 2:
$\begin{array}{l}{n_{ankan}} = {n_{{H_2}O}} - {n_{C{O_2}}}\\ \Rightarrow {n_{ankan}} = 0,2 - 0,1 = 0,1(mol)\\ \Rightarrow n = \frac{{0,1}}{{0,1}} = 1\end{array}$
Vậy CTPT của ankan là: $C{H_4}$
Đốt cháy hoàn toàn 11,2 lít khí metan. Biết các thể tích khí đo ở điều kiện tiêu chuẩn.Thể tích khí oxi cần dùng và thể tích khí cacbonic tạo thành lần lượt là
-
A.
22,4 lít và 22,4 lít.
-
B.
11,2 lít và 22,4 lít.
-
C.
22,4 lít và 11,2 lít.
-
D.
11,2 lít và 22,4 lít
Đáp án : C
+) Tính số mol CO2 và số mol O2 theo PT: CH4 + 2O2 $\xrightarrow{{{t}^{o}}}$ CO2 + 2H2O
\({n_{C{H_4}}} = \frac{{11,2}}{{22,4}} = 0,5\,mol\)
CH4 + 2O2 $\xrightarrow{{{t}^{o}}}$ CO2 + 2H2O
0,5 → 1 → 0,5 mol
$=>{{V}_{{{O}_{2}}}}=1.22,4=22,4$ lít
${{V}_{C{{O}_{2}}}}=0,5.22,4=11,2$ lít
Đốt cháy hoàn toàn hỗn hợp gồm 2 ankan là đồng đẳng kế tiếp thu được 2,24 lít khí CO2 và 2,34 gam H2O. Xác định CTPT của 2 ankan.
-
A.
CH4 và C2H6.
-
B.
C2H6 và C3H8.
-
C.
C3H8 và C4H10.
-
D.
CH4 và C3H8
Đáp án : C
+) Tính theo công thức: ${n_{ankan}} = {n_{{H_2}O}} - {n_{C{O_2}}} \Rightarrow \bar n$
${n_{C{O_2}}} = \frac{{2,24}}{{22,4}} = 0,1(mol)$${n_{{H_2}O}} = \frac{{2,34}}{{18}} = 0,13(mol)$
Pthh:
${C_{\bar n}}{H_{2\bar n + 2}} + (\frac{{3\bar n + 1}}{2}){O_2} \to \bar nC{O_2} + (\bar n + 1){H_2}O$
$\begin{array}{l}{n_{ankan}} = {n_{{H_2}O}} - {n_{C{O_2}}}\\ \Rightarrow {n_{ankan}} = 0,13 - 0,1 = 0,03(mol)\\ \Rightarrow \bar n = \frac{{0,1}}{{0,03}} = 3,3333\end{array}$
$ \Rightarrow $ 2 ankan là: C3H8 , C4H10
Cho 2,8 lít hỗn hợp metan và etilen (đktc) lội qua dung dịch brom (dư), người ta thu được 4,7 gam đibroetan. Phần trăm thể tích của khí metan là
-
A.
20%.
-
B.
40%.
-
C.
80%.
-
D.
60%
Đáp án : C
PTHH: C2H4 + Br2 → C2H4Br2
0,025 ← 0,025
\( = > {V_{{C_2}{H_4}}} = > {V_{C{H_4}}}\)\( = > \% {V_{C{H_4}}}\)
\({m_{{C_2}{H_4}B{{\rm{r}}_2}}} = 4,7\,gam\, = > {n_{{C_2}{H_4}B{{\rm{r}}_2}}} = \frac{{4,7}}{{188}} = 0,025\,mol\)
PTHH: C2H4 + Br2 → C2H4Br2
0,025 ← 0,025
\( = > {V_{{C_2}{H_4}}} = 0,025.22,4 = 0,56\,lit\, = > {V_{C{H_4}}} = 2,8 - 0,56 = 2,24\,lit\)
\( = > \% {V_{C{H_4}}} = \frac{{2,24}}{{2,8}}.100\% = 80\% \)
Đốt cháy hết 36 gam hỗn hợp khí C3H6 và C2H6 trong O2 dư thu được 56 lít CO2 (đktc). Thể tích khí C3H6 ở đktc là
-
A.
11,2 lít
-
B.
22,4 lít.
-
C.
33,6 lít.
-
D.
44,8 lít.
Đáp án : A
Gọi số mol của C3H6 và C2H4 lần lượt là x và y mol
=> mhỗn hợp = PT(1)
C3H6 + $\frac{9}{2}$O2 $\xrightarrow{{{t}^{o}}}$ 3CO2 + 3H2O
x mol → 3x mol
C2H6 + $\frac{7}{2}$O2 $\xrightarrow{{{t}^{o}}}$ 2CO2 + 3H2O
y mol → 2y mol
=> ${{n}_{C{{O}_{2}}}} = PT(2)$
Gọi số mol của C3H6 và C2H4 lần lượt là x và y mol
=> mhỗn hợp = 42x + 28y = 36 (1)
C3H6 + $\frac{9}{2}$O2 $\xrightarrow{{{t}^{o}}}$ 3CO2 + 3H2O
x mol → 3x mol
C2H6 + $\frac{7}{2}$O2 $\xrightarrow{{{t}^{o}}}$ 2CO2 + 3H2O
y mol → 2y mol
=> ${{n}_{C{{O}_{2}}}}=3\text{x}+2y=2,5\,mol\,\,\,\,(2)$
Từ (1) và (2) ta có hệ: \(\left\{ \begin{array}{l}42{\rm{x}} + 30y = 36\\3{\rm{x}} + 2y = 2,5\end{array} \right. = > \left\{ \begin{array}{l}x = 0,5\\y = 0,5\end{array} \right.\)
\( = > {V_{{C_3}{H_6}}} = {V_{{C_2}{H_4}}} = 0,5.22,4 = 11,2\) lít
Đốt cháy V lít etilen thu được 9 gam hơi nước. Thể tích không khí cần dùng (ở đktc), biết O2 chiếm 20% thể tích không khí?
-
A.
84,0 lít.
-
B.
16,8 lít.
-
C.
56,0 lít.
-
D.
44,8 lít
Đáp án : A
+) Tính số mol Oxi theo PT: PTHH: C2H4 + 3O2 $\xrightarrow{{{t}^{o}}}$ 2CO2 + 2H2O
+) Vì O2 chiếm 20% thể tích không khí => Vkhông khí = \(\frac{{{V_{{O_2}}}}}{{20\% }}\)
${{n}_{{{H}_{2}}O}}=\frac{9}{18}=0,5\,mol$
PTHH: C2H4 + 3O2 $\xrightarrow{{{t}^{o}}}$ 2CO2 + 2H2O
0,75 mol ← 0,5 mol
$=>{{V}_{{{O}_{2}}}}=0,75.22,4=16,8$ lít
Vì O2 chiếm 20% thể tích không khí => Vkhông khí = \(\frac{{{V_{{O_2}}}}}{{20\% }} = 84\) lít
Cho 0,448 lít (đktc) hỗn hợp khí gồm C2H4, C2H2 tác dụng hết với dung dịch brom dư, khối lượng brom đã tham gia phản ứng là 4,8 gam. Số mol khí C2H4 trong hỗn hợp ban đầu là
-
A.
0,02.
-
B.
0,01.
-
C.
0,015.
-
D.
0,005.
Đáp án : B
Gọi x, y lần lượt là số mol của etilen và axetilen => nhỗn hợp = PT (1)
Phương trình hoá học:
C2H4 + Br2 → C2H4Br2
x x x mol
C2H2 + 2Br2 → C2H2Br4
y 2y y mol
Từ \( \sum {{n_{B{{\rm{r}}_2}}} => PT(2)} \)
Số mol hỗn hợp = $\frac{{0,448}}{{22,4}}$ = 0,02 mol; ${{n}_{B{{r}_{2}}}}~=\frac{4,8}{160}=0,03\text{ }mol$
Gọi x, y lần lượt là số mol của etilen và axetilen => nhỗn hợp = x + y = 0,02 (1)
Phương trình hoá học:
C2H4 + Br2 → C2H4Br2
x x x mol
C2H2 + 2Br2 → C2H2Br4
y 2y y mol
\( = > \sum {{n_{B{{\rm{r}}_2}}} = x + 2y = 0,03\,\,\,(2)} \)
Từ (1) và (2) ta có hệ phương trình: \(\left\{ \begin{array}{l}x + y = 0,02\\x + 2y = 0,03\end{array} \right. = > \left\{ \begin{array}{l}x = 0,01\\y = 0,01\end{array} \right.\)
=> số mol C2H4 trong hỗn hợp đầu là 0,01 mol
Đốt cháy hoàn toàn 1 mol khí axetilen thì cần bao nhiêu lít không khí (các khí đo ở đktc, biết rằng oxi chiếm 20% thể tích không khí) ?
-
A.
300 lít.
-
B.
280 lít.
-
C.
240 lít.
-
D.
120 lít.
Đáp án : B
+) Tính số mol oxi theo PT: 2C2H2 + 5O2 $\xrightarrow{{{t}^{o}}}$ 4CO2 + 2H2O
+) Vì khí oxi chiếm 20% thể tích không khí => Vkhông khí = $\frac{{{V}_{{{O}_{2}}}}}{20\%}$
Phương trình đốt cháy khí axetilen:
2C2H2 + 5O2 $\xrightarrow{{{t}^{o}}}$ 4CO2 + 2H2O
1 mol → 2,5 mol
$=>{{V}_{{{O}_{2}}}}=2,5.22,4=56$ lít
Vì khí oxi chiếm 20% thể tích không khí => Vkhông khí = $\frac{56}{20\%}=280$lít
Cho brom phản ứng với benzen tạo ra brombenzen (bột sắt làm xúc tác). Tính khối lượng benzen cần dùng để điều chế 15,7 gam brombenzen. Biết hiệu suất của quá trình phản ứng là 80%.
-
A.
9,75 gam.
-
B.
6,24 gam.
-
C.
7,80 gam.
-
D.
10,53 gam
Đáp án : A
+) Tính số mol benzen theo PT : ${{C}_{6}}{{H}_{6}}+B{{r}_{2}}\xrightarrow{F\text{e}}{{C}_{6}}{{H}_{5}}Br+HBr$
+) Từ hiệu suất $H = \frac{{{n_{{C_6}{H_6}(lt)}}}}{{{n_{{C_6}{H_6}(tt)}}}}$ => tính khối lượng benzen cần dùng
${n_{{C_6}{H_5}Br}} = \frac{{15,7}}{{157}} = 0,1(mol)$
Phương trình hóa học:
${{C}_{6}}{{H}_{6}}+B{{r}_{2}}\xrightarrow{F\text{e}}{{C}_{6}}{{H}_{5}}Br+HBr$
0,1 ← 0,1 (mol)
$\begin{array}{l}H = \frac{{{n_{{C_6}{H_6}(lt)}}}}{{{n_{{C_6}{H_6}(tt)}}}} = \frac{{0,1}}{x} = \frac{{80}}{{100}}\\ \Leftrightarrow x = 0,125(mol)\\ \Rightarrow {m_{{C_6}{H_6}}} = 0,125.78 = 9,75(g)\end{array}$
Đốt cháy hoàn toàn 2,24 lít anken A trong oxi dư thu được hỗn hợp khí B. Cho B lần lượt đi qua bình 1 đựng H2SO4 đặc và bình 2 đựng Ca(OH)2 dư. Thấy khối lượng bình 1 tăng 5,4 gam, bình 2 có 30 gam kết tủa. CTPT của A là
-
A.
C2H4.
-
B.
C3H6.
-
C.
C4H8.
-
D.
C5H10
Đáp án : B
+) Từ khối lượng bình 1 tăng và khối lượng kết tủa bình 2 => số mol CO2 và H2O => CTTQ của A
+) Viết pthh: ${C_n}{H_{2n}} + \frac{{3n}}{2}{O_2} \to nC{O_2} + n{H_2}O$
=> tính n theo PT
Gọi CTPT của $A$ là ${{C}_{n}}{{H}_{2n}}$$(n\ge 2)$
${{m}_{{{H}_{2}}O}}=5,4(g)\Rightarrow {{n}_{{{H}_{2}}O}}=\frac{5,4}{18}=0,3(mol)$
${{n}_{CaC{{O}_{3}}}}=\frac{30}{100}=0,3(mol)={{n}_{C{{O}_{2}}}}$
${{n}_{A}}=\frac{2,24}{22,4}=0,1(mol)$
pthh: ${{C}_{n}}{{H}_{2n}}+\frac{3n}{2}{{O}_{2}}\to nC{{O}_{2}}+n{{H}_{2}}O$
theo pt: 1 $n$ $n$
theo đb: 0,1 0,3 0,3 (mol)
Ta có: $0,1\cdot n=0,3\cdot 1\Leftrightarrow n=3$
Vậy CTPT của $A$ là: ${{C}_{3}}{{H}_{6}}$
















